
【題目】現使用酸堿中和滴定法測定市售白醋的總酸量(g·100mL-1)。
Ⅰ.實驗步驟
(1)配制100ml待測白醋溶液:用 (填儀器名稱)量取10.00 mL食用白醋,在燒杯中用水稀釋后轉移到 (填儀器名稱)中定容,搖勻即得待測白醋溶液。
(2)用酸式滴定管取待測白醋溶液20.00 mL于錐形瓶中,向其中滴加2滴 作指示劑。
![]()
(3)讀取盛裝0.1000 mol·L-1 NaOH 溶液的堿式滴定管的初始讀數。如果液面位置如圖所示,則此時的讀數為________mL。
(4)滴定。當___________________________時,停止滴定,并記錄NaOH溶液的終讀數。重復滴定3次。
Ⅱ.實驗記錄
滴定次數實驗數據(mL) | 1 | 2 | 3 | 4 |
V(樣品) | 20.00 | 20.00 | 20.00[ | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.數據處理與討論
(1)按實驗所得數據,可得c(市售白醋)= mol·L-1;
市售白醋總酸量= g·100 mL-1。
(2)在本實驗的滴定過程中,下列操作會使實驗結果偏大的是________填寫序號)。
a.堿式滴定管在滴定時未用標準NaOH溶液潤洗
b.堿式滴定管的尖嘴在滴定前有氣泡,滴定后氣泡消失
c.錐形瓶中加入待測白醋溶液后,再加少量水
d.錐形瓶在滴定時劇烈搖動,有少量液體濺出
【答案】I.(1)酸式滴定管(或10mL移液管);100ml容量瓶;(2)酚酞;(3)0.60;(每空1分)
(4)溶液由無色恰好變為紅色(或粉紅色),并在半分鐘內不褪色;(2分,)
III.(1)0.75;4.5;(每空2分)(2)ab(2分,錯選、多選不給分,漏選給1分)
【解析】
試題分析:Ⅰ.(1)用酸式滴定管(或10mL移液管)(量取10.00mL食用白醋,在燒杯中用水稀釋后轉移到100mL 容量瓶中定容,搖勻即得待測白醋溶液;
(2)食醋與NaOH反應生成了強堿弱酸鹽,溶液呈堿性,應選擇堿性變色范圍內的指示劑酚酞;
(3)滴定管液面的讀數0.60mL;
(4)NaOH滴定食醋的終點為:溶液由無色恰好變為紅色,并在半分鐘內不褪色;
Ⅲ.(1)第1次滴定誤差明顯大,屬異常值,應舍去;3次消耗的NaOH溶液的體積為:15.00mL;15.05mL;14.95mL;則NaOH溶液的體積的平均值為15.00mL;設10mL市售白醋樣品中 CH3COOH 的物質的量濃度為x,則
CH3COOH~NaOH
1mol 1mol
0.2x 0.1000mol/L×0.015L
則c(市售白醋)=![]() =0.75mol/L
=0.75mol/L
樣品總酸量為0.75mol/L×0.2L×60g/mol×![]() =4.50g/100mL;
=4.50g/100mL;
(2)a.堿式滴定管在滴定時未用標準NaOH溶液潤洗,標準液濃度降低,造成V(標準)偏大,根據c(待測)=![]() 分析可知c(待測)偏大,a正確;b.堿式滴定管的尖嘴在滴定前有氣泡,滴定后氣泡消失,造成V(標準)偏大,根據c(待測)=
分析可知c(待測)偏大,a正確;b.堿式滴定管的尖嘴在滴定前有氣泡,滴定后氣泡消失,造成V(標準)偏大,根據c(待測)=![]() 分析可知c(待測)偏大,b正確;c.錐形瓶中加入待測白醋溶液后,再加少量水,對V(標準)無影響,根據c(待測)=
分析可知c(待測)偏大,b正確;c.錐形瓶中加入待測白醋溶液后,再加少量水,對V(標準)無影響,根據c(待測)=![]() 分析可知c(待測)不變,c錯誤;d.錐形瓶在滴定時劇烈搖動,有少量液體濺出,待測液物質的量偏小,造成V(標準)偏小,根據c(待測)=
分析可知c(待測)不變,c錯誤;d.錐形瓶在滴定時劇烈搖動,有少量液體濺出,待測液物質的量偏小,造成V(標準)偏小,根據c(待測)=![]() 分析可知c(待測)偏小,d錯誤;答案選ab。
分析可知c(待測)偏小,d錯誤;答案選ab。


科目:高中化學 來源: 題型:
【題目】下圖為元素周期表的一部分,參照元素①~⑩在表中的位置,請用化學用語作答:
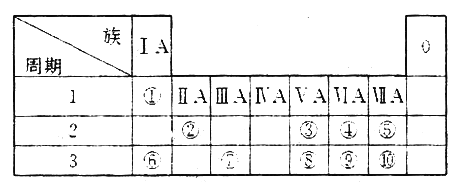
(1)⑤、⑥、⑦ 的離子半徑由大到小的順序為_________。(填離子符號)
(2)⑧、⑨、⑩的最高價含氧酸的酸性由強到弱為_______。(用化學式表示)
(3)寫出⑥在空氣中加熱生成的產物的電子式:_______。與⑧同族的砷(As)的原子結構示意圖為_____________。
(4)⑦和⑩形成的化合物的物理性質非常特殊,其的熔點為190℃(2.02×105Pa),但在180℃就開始升華。據此判斷,該是_______(填“共價化合物”或“離子化合物”) , 可以證明你的判斷正確的實驗依據是________________。
(5)表中所列元素的原子間反應最容易形成離子鍵的是_________(填元素符號)。⑧與⑩元素形成的常見分子中所有原子______(填“是”或“不是”)都滿足最外層為8電子結構。
(6)己知某些不同族元素的性質也有一定的相似性,如元素②與元素⑦的氫氧化物有相似的性質。寫出元素②的氫氧化物與NaOH溶液反應的離子方程式:______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知常溫下在溶液中可發生如下兩個離子反應:Ce4++Fe2+ = Fe3++Ce3+ Sn2++2Fe3+ = 2Fe2++Sn4+由此可以確定Fe2+、Ce3+、Sn2+三種離子的還原性由強到弱的順序是( )
A.Sn2+、Fe2+、Ce3+ B.Ce3+、Fe2+ 、Sn2+ C.Sn2+、Ce3+、Fe2+ D.Fe2+、Sn2+、Ce3+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據生活經驗,判斷下列物質按酸堿性的一定順序依次排列正確的是
A. 廁所清潔劑醋肥皂廚房清潔劑
B. 醋廁所清潔劑肥皂廚房清潔劑
C. 廁所清潔劑廚房清潔劑醋肥皂
D. 廚房清潔劑醋肥皂廁所清潔劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/L的NaOH溶液,所得溶液PH與NaOH溶液體積的關系曲線如圖所示,下列說法正確的是
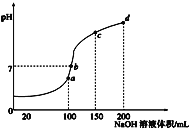
A. a、b、c、d四個點中,水的電離程度最大的是d
B. a點溶液中:c(NH3·H2O)+c(H+)=c(OH—)
C. b點溶液中:c(Na+)+c(NH4+)=2c(SO42—)
D. c點溶液中:c(Na+)= c(SO42—) +c(NH4+)+ c(NH3·H2O)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.下列變化中:①干冰氣化;②硝酸鉀熔化;③KHSO4熔融;④硫酸溶于水;⑤蔗糖溶于水;⑥HI分解。用序號填空:
(1)未破壞化學鍵的是_____________,(2)僅離子鍵被破壞的是_____________,
(3)僅共價鍵被破壞的是_____________;
Ⅱ.有下列各組物質:①石墨和足球烯C60;②126C和136C;③CH3—CH2—CH2—CH3和CH3—CH(CH3)CH3;④漂白粉和漂白液主要成分;⑤正丁烷和異庚烷;⑥乙烯和聚乙烯;⑦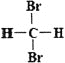 和
和 ;⑧丙烷和環丙烷。用序號填空:
;⑧丙烷和環丙烷。用序號填空:
(1)__________組兩者互為同位素,(2)__________組兩者互為同素異形體,
(3)__________組兩者屬于同系物,(4)__________組兩者互為同分異構體,
(5)__________組兩者是同一物質;
Ⅲ.化合物A的結構簡式為: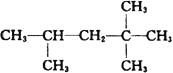 ,它是汽油燃燒品質抗震性能的參照物,用系統命名法對它命名_____________________,其中A的同分異構體中含等效氫原子種類最少的一種結構簡式為:_______________;若A是由烯烴和H2通過加成反應得到,則該烯烴的結構簡式為__________________。
,它是汽油燃燒品質抗震性能的參照物,用系統命名法對它命名_____________________,其中A的同分異構體中含等效氫原子種類最少的一種結構簡式為:_______________;若A是由烯烴和H2通過加成反應得到,則該烯烴的結構簡式為__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】處于下列狀態的物質中:①氯化鈉固體 ②干冰 ③HCl氣體 ④銅 ⑤硫酸鋇固體 ⑥蔗糖 ⑦乙醇 ⑧熔融的硝酸鉀 ⑨NaCl溶液
(1)能導電的是(填編號,下同) ;
(2)屬于電解質的是 ;
(3)屬于非電解質的是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】生產、生活離不開化學,下列說法不正確的是( )
A. 泡沫滅火器的反應原理是非氧化還原反應
B. 鋼鐵析氫腐蝕和吸氧腐蝕的速率一樣快
C. 鍋爐水垢中含有的CaSO4,可先用Na2CO3溶液處理,后用酸除去
D. 燃料電池的燃料都在負極發生反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CH3CH2CH2CH3(正丁烷)和(CH3)2CHCH3(異丁烷)的關系是
A. 同分異構體 B. 同素異形體 C. 同位素 D. 同一種物質
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com