
【題目】某工廠廢水中含1.00×10﹣2mol/L的Cr2O72﹣ , 其毒性較大.某研究性學習小組為了變廢為寶,將廢水處理得到磁性材料Cr0.5Fe1.5FeO4 , 設計了如圖實驗,下列說明正確的是( ) 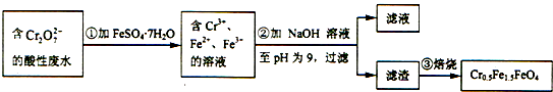
A.根據第①步反應可知還原性:Cr3+大于Fe2+
B.第②步過濾得到的濾渣中主要成分為Cr(OH)3、Fe(OH)2 , 不含Fe(OH)3
C.欲使1L該廢水中的Cr2O72﹣完全轉化為Cr0.5Fe1.5FeO4 , 理論上需要加入27.8g FeSO47H2O
D.第③步高溫焙燒過程用到的主要實驗儀器中屬于硅酸鹽質的有:酒精燈、蒸發皿、泥三角
【答案】C
【解析】解:Cr2O72﹣有較強氧化性,FeSO47H2O中Fe2+有一定的還原性,在酸性介質中發生氧化還原反應,由實驗流程可知,第①步反應中Cr2O72﹣在酸性條件下將Fe2+氧化為Fe3+ , 自身被還原為Cr3+ , 加入NaOH溶液調節溶液pH為9,得到Cr(OH)3、Fe(OH)2、Fe(OH)3 , 過濾的濾渣經焙燒得到Cr0.5Fe1.5FeO4 ,
A.第①步反應中Cr2O72﹣在酸性條件下將Fe2+氧化為Fe3+ , 自身被還原為Cr3+ , 反應離子方程式為Cr2O72﹣+14H++6Fe2+=2Cr3++6Fe3++7H2O,還原性Cr3+小于Fe2+ , 故A錯誤;
B.由題給框圖可知,Fe2+過量,加NaOH時,產生Cr(OH)3、Fe(OH)3和Fe(OH)2三種沉淀物,故B錯誤;
C.1 L廢水中含n(Cr2O72﹣)=1.00×10﹣2 mol.根據Cr原子、Fe原子守恒,可得:
Cr2O72﹣~~~4Cr0.5Fe1.5FeO4~~~10FeSO47H2O,
所以理論上n(FeSO47H2O)=10n(Cr2O72﹣)=1.00×10﹣2 mol×10=0.1 mol,
所以m(FeSO47H2O)=0.1 mol×278 g/mol=27.8 g,故C正確;
D.加入固體,應在坩堝中進行,不能用蒸發皿,故D錯誤.
故選C.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】碳酸鈰[Ce2(CO3)3]為白色粉末,難溶于水,主要用作生產鈰的中間化合物.它可由氟碳酸鈰精礦經如圖1流程制得. 
(1)如圖2是一種稀土元素鈰(Ce)在元素周期表中的信息示意圖.則鈰原子的質子數是 , 氟碳酸鈰的化學式為CeFCO3 , 該化合物中,Ce的化合價為;
(2)焙燒生成的鈰化合物為二氧化鈰(CeO2),其在酸浸時發生反應的離子方程式為;
(3)試劑X;
(4)已知298K時,Ksp[Ce(OH)4]=1×10﹣29 , Ce(OH)4的溶度積表達式為Ksp=;為了使溶液中Ce4+沉淀完全,需調節pH為以上;
(5)取某Ce(OH)4產品1.00g(質量分數為97%),加硫酸溶解后,用0.1000molL﹣1的FeSO4溶液滴定至終點(鈰被還原成Ce3+)則需要滴加標準溶液的體積mL,若用硫酸酸化后改用0.1000molL﹣1的FeCl2溶液滴定產品從而測定Ce(OH)4產品的質量分數,其它操作都正確,則測定的Ce(OH)4產品的質量分數(填“偏高”、“偏低”或“不變”).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現用0.1 mol/L的AlCl3溶液和0.1 mol/L的氫氧化鈉溶液,進行下面的實驗。
在試管中盛有上述AlCl3溶液10 mL,向其中逐滴滴入上述的NaOH溶液。
(1)加入10 mL NaOH溶液時的現象是________,加入30 mL NaOH溶液時的現象是________,加入35 mL NaOH溶液時的現象是____________________。
(2)生成沉淀質量最多時,需NaOH溶液________mL。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】光譜研究表明,易溶于水的SO2所形成的溶液中存在著下列平衡:

據此,下列判斷中正確的是( )
A.該溶液中存在著SO2分子
B.該溶液中H+濃度是SO32-濃度的2倍
C.向該溶液中加入足量的酸都能放出SO2氣體
D.向該溶液中加入過量NaOH可得到Na2SO3、NaHSO3和NaOH的混合溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.已知HClO是比H2CO3還弱的酸,HClO的電離平衡常數為2.95×10-5,H2CO3的電離平衡常數為K1=4.3×10-7和K2=5.6×10-11氯水中存在下列平衡:Cl2+H2O![]() HCl+HClO,HClO
HCl+HClO,HClO![]() H++ClO-,達平衡后
H++ClO-,達平衡后
(1)要使HClO濃度增加,可加入下列物質________(填代號)。
A.SO2 B.NaHCO3 C.HCl D.NaOH
(2)由此說明在實驗室可用排飽和食鹽水收集Cl2的理由是________________。
Ⅱ.Al(OH)3的電離方程式可表示為:H2O+AlO2-+H+![]() Al(OH)3
Al(OH)3![]() Al3++3OH-。
Al3++3OH-。
試根據平衡移動原理,解釋下列有關問題。
(1)向Al(OH)3沉淀中加入鹽酸,沉淀溶解,其原因是_________________,有關離子方程式為__________________。
(2)向Al(OH)3沉淀中加入苛性鈉溶液,沉淀溶解,其原因是________________,有關離子方程式為__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組用如圖所示裝置測定鋁鎂合金中鋁的質量分數和鋁的相對原子質量。

(1)A中試劑為________。
(2)B中發生反應的化學方程式為_______________。
(3)若實驗用鋁鎂合金的質量為a g,測得氫氣體積為b mL(已換算為標準狀況),B中剩余固體的質量為c g,則鋁的相對原子質量為____________________。
(4)實驗過程中,若未洗滌過濾所得的不溶物,則測得鋁的質量分數(用a、c表示)將________(填“偏大”、“偏小”或“不受影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32﹣、SO42﹣、NO3﹣中的幾種,若加入鋅粒,產生無色無味的氣體;若加入NaOH溶液,產生白色沉淀,且產生的沉淀量與加入的物質的量之間的關系如圖所示,下列說法正確的是( )
A.溶液中一定不含有CO32﹣ , 可能含有SO42﹣和NO3﹣
B.溶液中的陽離子只有H+、Mg2+、Al3+
C.溶液中n(NH4+)=0.2mol
D.n(H+):n(Al3+):n(Mg2+)=1:1:1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com