
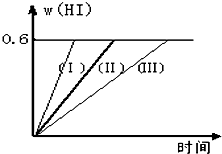
 將1mol I2(g) 和2mol H2置于2L密閉容器中,在一定溫度下發生反應:I2(g)+H2(g)?2HI(g);△H<0,并達平衡.HI的體積分數w(HI)隨時間變化如圖曲線(Ⅱ)所示:
將1mol I2(g) 和2mol H2置于2L密閉容器中,在一定溫度下發生反應:I2(g)+H2(g)?2HI(g);△H<0,并達平衡.HI的體積分數w(HI)隨時間變化如圖曲線(Ⅱ)所示:| n(I2)(剩余) |
| V |
| 1 |
| 2 |
| 1 |
| 2 |
| 0.1mol |
| 2L |
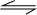 2HI(g);
2HI(g);| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


科目:高中化學 來源: 題型:
 將1mol I2(g)和2mol H2置于5L密閉容器中,在一定溫度下發生反應:I2(g)+H2(g)?2HI(g)△H<0,并達到平衡.HI的體積分數w(HI)隨時間變化如曲線(Ⅱ)所示:
將1mol I2(g)和2mol H2置于5L密閉容器中,在一定溫度下發生反應:I2(g)+H2(g)?2HI(g)△H<0,并達到平衡.HI的體積分數w(HI)隨時間變化如曲線(Ⅱ)所示:查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| H | + 4 |
| O | - 2 |
| H | + 4 |
查看答案和解析>>
科目:高中化學 來源:2010-2011學年河南省信陽市高三第二次調研考試化學試卷 題型:填空題
(18分)(1)某一反應體系中有反應物和生成物共5種物質:S、H2S、HNO3、NO、H2O,
寫出該反應的化學方程式并配平_________________________________。若反應過程中
轉移了0.3mol電子,則氧化產物的質量是____________g。
(2)同一物質呈氣態的熵值最大,液態的熵值次之,固態的熵值最小。若同溫同壓下一個化學反應生成物氣體的體積等于反應物氣體的體積就可以粗略認為該反應的熵變為0。某化學興趣小組,專門研究了氧族元素及其某些化合物的部分性質。所查資料如下:
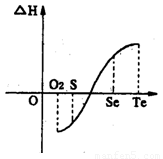
a.碲(Te)為固體,H2Te為氣體,Te和H2不能直接化合生成H2Te
b.等物質的量氧氣、硫、硒、碲與H2反應的焓變情況如圖l所示:
請回答下列問題:
H2與硫化合的反應______________熱量(填“放出”或“吸收”)。根據題目所給信息,請解釋為什么Te和H2不能直接化合_________________________________________.
(3)在復雜的反應中,要考慮反應的先后順序。已知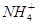 +
+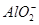 +2H2O
+2H2O Al(OH)3↓ +NH3·H2O,向含有等物質的量的
Al(OH)3↓ +NH3·H2O,向含有等物質的量的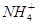 、Al3+、H+混合溶液中,慢慢滴加NaOH溶液,直至過量,并不斷攪拌,依次發生了數個離子反應;其中:
、Al3+、H+混合溶液中,慢慢滴加NaOH溶液,直至過量,并不斷攪拌,依次發生了數個離子反應;其中:
第二個離子反應的離子方程式是__________________________________.
最后—個離子反應的離子方程式是________________________________.
(4)將1mol I2(g)和2mol H2(g)置于某2L密閉容器中,在一定溫度下發生反應:H2(g)+I2(g) 2HI(g);△H<0。 并達平衡。HI的體積分數HI%隨時問變化曲線如圖2所示:
2HI(g);△H<0。 并達平衡。HI的體積分數HI%隨時問變化曲線如圖2所示:
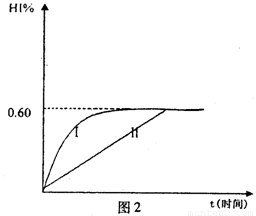
①達到平衡時,I2(g)的物質的量濃度為________mol/L.
②保持加入的反應物的物質的量不變,若改變反應條件,在某一條件下HI%的變化如曲線l所示,則該條件可能是(寫出所有的可能性)___________________________________________________________在這種條件下,平衡常數K值____________(填“增大”、“變小”、。不變”或“可能變大也可能變小”)
③若保持溫度不變,在另一相同的2L密閉容器中加入1molH2(g)和2molHI(g),發生反應達到平衡時,H2的體積分數為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
將1mol I2(g)和2mol H2(g)置于某2L密閉容器中,在一定溫度下發生反應:
I2(g)+H2(g)![]() 2HI(g); ΔH<0,并達到平衡。HI的體積分數Φ(HI)隨時間變化如圖曲線(II)所示:
2HI(g); ΔH<0,并達到平衡。HI的體積分數Φ(HI)隨時間變化如圖曲線(II)所示:
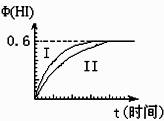
(1)達平衡時,I2(g)的物質的量濃度為 mol?L-1。
(2)若改變反應條件,在某條件下Φ(HI)的變化如曲線
(I)所示,則該條件可能是 (填入下列條件的序號)。
①恒容條件下,升高溫度
②恒容條件下,降低溫度
③恒溫條件下,縮小反應容器體積
④恒溫條件下,擴大反應容器體積
⑤恒溫、恒容條件下,加入適當催化劑
(3)若保持溫度不變,在另一相同的2L密閉容器中加入a mol I2(g)、b mol H2(g)和c mol HI(g)(a、b、c均大于0),發生反應達平衡時,HI的體積分數仍為0.60,則a、b、c的關系為 (用一個含a、b、c的代數式表示)。
(4)室溫時將0.01 mol HI氣體溶于水配成100 ml溶液,則該溶液中由水電離產生的氫離子的物質的量濃度為 mol?L-1 ;若降低溫度該溶液的pH值將 (填增大、減小或不變)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com