
現擬在實驗室里利用空氣和鎂粉為原料制取少量氮化鎂(Mg3N2)。已知實驗中可能會發生下列反應:
①2Mg+O2 2MgO;②3Mg+N2
2MgO;②3Mg+N2 Mg3N2;③2Mg+CO2
Mg3N2;③2Mg+CO2 2MgO+C;
2MgO+C;
④Mg+H2O MgO+H2↑; ⑤Mg3N2 +6H2O
MgO+H2↑; ⑤Mg3N2 +6H2O 3Mg(OH)2+2NH3↑
3Mg(OH)2+2NH3↑
可供選擇的裝置和藥品如下圖所示(鎂粉、還原鐵粉均已干燥,裝置內所發生的反應是完全的,整套裝置的末端與干燥管相連)。
回答下列問題:
(1)在設計實驗方案時,除裝置A、D、E外,還應選擇的裝置有 (填字母代號),選擇裝置D目的為_____________________________ ;
(2)通氣后,應先點燃 處的酒精燈;如果同時點燃A、F裝置的酒精燈,將會使實驗結果 (填“偏高”或“偏低”)原因
(3)請設計一個實驗,驗證產物是Mg3N2,寫出操作步驟、現象和結論:
_____________________________________________________________________
(1)BF (2分) D 目的是除去空氣中的CO2,避免反應③發生;(2分)
(2)F;(1分)偏低;(2分)如果裝置F中的還原鐵粉沒有達到反應溫度時,氧氣不能除盡,導致氧同鎂反應,而使氮化鎂中混入氧化鎂。(2分)
(3)取適量產物放入試管中,滴加蒸餾水,將潤濕的紅色石蕊試紙靠近試管口,如果試管中的溶液出現渾濁,紅色石蕊試紙變藍,則可以證明有氮化鎂生成。(2分)
解析試題分析:(1)該反應中為了得到純凈的氮化鎂,必須把影響的產物的氣體水,還有氧氣去除,裝置B是用來除去水蒸汽的,放在A之前,F可以用來除去氧氣。D 目的是除去空氣中的CO2,避免反應③發生;
(2)這一裝置中,很多人可能會考慮到F裝置是用來除去水蒸汽的,那樣的話,反應產生的氫氣怎么辦,因此這個裝置是用來除去氧氣的。如果裝置F中的還原鐵粉沒有達到反應溫度時,氧氣不能除盡,導致氧同鎂反應,而使氮化鎂中混入氧化鎂。(2分)
(3)驗證產物是Mg3N2,必須利用氮化鎂的特征反應。取適量產物放入試管中,滴加蒸餾水,將潤濕的紅色石蕊試紙靠近試管口,如果試管中的溶液出現渾濁,紅色石蕊試紙變藍,則可以證明有氮化鎂生成。
考點:氮化鎂制取的有關知識


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:實驗題
(19分)黃銅礦的主要成分是CuFeS2(硫元素顯 價,鐵元素顯+2價)。實驗室里用黃銅礦為原料制取單質銅和鐵紅(Fe2O3)的流程如下:
價,鐵元素顯+2價)。實驗室里用黃銅礦為原料制取單質銅和鐵紅(Fe2O3)的流程如下:
已知:
 =
=
(1)在實驗室中,應將黃銅礦粉末放在__________(填儀器名稱)中焙燒。
(2)將反應過程中產生的SO2和H2S通入下圖所示裝置中檢驗它們的性質。該實驗證明SO2具有_________性和__________性。
(3)欲選用下列部分裝置在實驗室中以MnO2和濃鹽酸為原料制取純凈、干燥的氯氣。 
①圓底燒瓶中發生反應的離子方程式為_________________________________________。
②按氣流方向由左到右,導管口連接順序為a→__________________________________。
③裝置連接好后,在裝藥品前,需檢驗裝置的氣密性,具體方法是__________________。
④向濾液A中通入C12,某同學取通入C12后的溶液滴加KSCN溶液,用來證明C12的氧化性比Fe3+強的結論。該實驗設計是否合理________(填“是”或“否”),請用簡要文字解釋你的理由_____________________________________________________________。
(4)若使用20 g黃銅礦粉末可制得8 gFe2O3(鐵紅),則該黃銅礦中含CuFeS2的質量分數是________ (假設各步反應均完全進行且過程中無額外物質損耗)。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
硫酸銅晶體俗稱“膽礬”,在無機化工及生產生活中有廣泛的應用。某課外研究小組的同學用粗銅粉(含有碳等雜質)設計了兩種制備膽礬的途徑,并測定了其中結晶水的含量。設計的流程如下: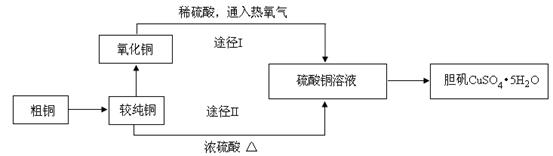
(1)“較純銅”轉化為氧化銅時,應將其置于 內進行灼燒(填寫儀器名稱)。“粗銅”表面的油脂可以用熱堿溶液洗去,原因是 。若灼燒“粗銅”,獲得的產物是混有少量銅的氧化銅。存在少量銅的可能原因是 。
a.灼燒過程中部分氧化銅被還原 b.該條件下銅無法被氧氣氧化
c.氧化銅在加熱過程中分解生成銅 d.灼燒不充分銅未被完全氧化
(2)通過途徑I實現用粗制氧化銅制取膽礬,必須進行的實驗操作步驟是:酸溶、加熱通氧氣、過濾、 、冷卻結晶、 、自然干燥。比較由粗制氧化銅制取膽礬的兩種途徑,途徑Ⅰ有明顯的兩個優點:
① 。
② 。
(3)測定膽礬晶體里結晶水的含量時,若測定的相對誤差大于零,則產生誤差的原因可能是___________。
a.加熱后容器未放入干燥器中冷卻
b.最后兩次加熱后的質量相差較大
c.加熱前稱量時容器未完全干燥
d.加熱過程中有少量濺失
(4)利用下圖裝置加熱無水硫酸銅粉末直至完全分解,A的試管中剩余黑色粉末,用帶火星的木條伸入集氣瓶D,發現木條能復燃。反應前后各裝置的質量見圖下方的表格所示。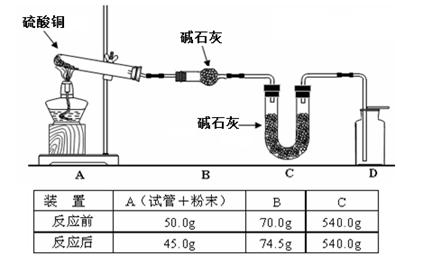
請通過計算,推斷該實驗條件下硫酸銅分解的化學方程式: 。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
某學生利用以下裝置探究噴泉實驗。其中A、F分別為硫化氫和氯氣的發生裝置,C為純凈干燥的氯氣與硫化氫反應的裝置。
請回答下列問題:
(1)裝置F中發生反應的化學方程式 。
(2)裝置A中的分液漏斗內液體a可選用 (選填以下選項的代號)
A.鹽酸 B.濃硫酸 C.稀硫酸 D.稀硝酸
(3)虛線框內應添加必要的除雜裝置,請從上圖的“備選裝置”中選擇合適裝置的編號,填入下列空格。B__________、D__________、E__________。
(4)打開K1、K2,將常溫壓下的H2S、Cl2以體積比1:1充滿燒瓶后,燒瓶中發生的反應用化學方程式表示為 ;關閉K1、K2,始終看不到燒瓶內產生“噴泉”現象,理由是: 。
(5)在操作(4)的基礎上,引發噴泉操作方法是 。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
某化學興趣小組同學展開對漂白劑亞氯酸鈉(NaClO2)的研究。
實驗Ⅰ:制取NaClO2晶體
已知:NaClO2飽和溶液在溫度低于38 ℃時析出的晶體是NaClO2·3H2O,高于38 ℃時析出的晶體是NaClO2,高于60℃時NaClO2分解成NaClO3和NaCl。現利用圖10所示裝置進行實驗。
(1)裝置③的作用是____________________。
⑵裝置②中產生ClO2的化學方程式為____;
裝置④中制備NaClO2的化學方程式為____。
(3)從裝置④反應后的溶液獲得NaClO2晶體的操作步驟為:
①減壓,55 ℃蒸發結晶;②趁熱過濾;③____________;④低于60 ℃干燥,得到成品。
實驗Ⅱ:測定某亞氯酸鈉樣品的純度。
設計如下實驗方案,并進行實驗:
①準確稱取所得亞氯酸鈉樣品m g于燒杯中,加入適量蒸餾水和過量的碘化鉀晶體,再滴入適量的稀硫酸,充分反應(已知:ClO2-+4I-+4H+=2H2O+2I2+Cl-);將所得混合液配成250 mL待測溶液。
②移取25.00 mL待測溶液于錐形瓶中,加幾滴淀粉溶液,用c mol·L-1 Na2S2O3標準液滴定,至滴定終點。重復2次,測得平均值為V mL(已知:I2+2S2O32-=2I-+S4O62-)。
⑷達到滴定終點時的現象為________________。
⑸該樣品中NaClO2的質量分數為____________(用含m、c、V的代數式表示)。
⑹在滴定操作正確無誤的情況下,此實驗測得結果偏高,原因用離子方程式表示為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
實驗室以空氣(O2體積分數20%)為原料,在無碳、無水的環境下,用下圖A裝置制備臭氧(3O2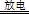 2O3)。
2O3)。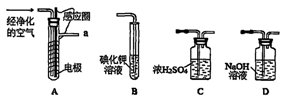
(1)空氣通入A裝置之前,應先后通過上述裝置中的 、 (填裝置序號)。
(2)臭氧與碘化鉀溶液反應為:2KI+O3+H2O=2KOH+I2+O2。將a處氣體通入裝置B,溶液中的現象為 。
(3)為測定O2轉化為O3的轉化率,將裝置B中的溶液全部轉入另一容器中,加入CC14,經萃取、分液、蒸餾、冷卻、稱重,得I2固體0.254g。
①萃取操作所用玻璃儀器的名稱 。
②若實驗時通入空氣1.12L(標準狀況),O2的轉化率為 。
③測定時需在A、B裝置間連接裝置D,原因是 。
(4)工業上分離O3和O2,可將混合氣體液化后再分離,下列分離方法合理的是 (填序號)。
A.過濾 B.分餾 C.分液 D.萃取
(5)臭氧可用于含CN一堿性電鍍廢水的處理。第i步:CN一轉化為OCN-;第ii步:OCN一繼續轉化為CO32一及兩種單質氣體。若第ii步轉化時,O3與OCN-物質的質量之比為3∶2,該步反應的離子方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
氫化鈣固體是登山運動員常用的能源提供劑。某興趣小組擬選用如下裝置制備氫化鈣。
回答下列問題:
(1)檢查裝置E氣密性的操作方法是 。
(2)利用上述裝置制取氫化鈣時按氣流方向連接順序為i→___→___→___→ → → →a(填儀器接口的字母編號)。
(3)根據完整的實驗裝置進行實驗,實驗步驟如下:檢查裝置氣密性后,裝入藥品;打開分液漏斗活塞;__________________(請按正確的順序填入下列步驟的標號)。
| A.加熱反應一段時間 | B.收集氣體并檢驗其純度 |
| C.關閉分液漏斗活塞 | D.停止加熱,充分冷卻 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
堿式碳酸銅是一種用途廣泛的化工原料。工業上可用酸性刻蝕廢液(主要含有Cu2+、Fe2+、Fe3+、H +、Cl-)制備,其制備過程如下:
Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物 質 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 開始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
用下圖裝置測定水中氫、氧元素的質量比,其方法是分別測定通氫氣前后玻璃管的質量差和U形管的質量差,實驗測得m(H):m(O)>1:8。下列對導致這一結果的原因的分析中,一定錯誤的是( )
| A.Ⅰ、Ⅱ裝置之間缺少干燥裝置 |
| B.Ⅲ裝置后缺少干燥裝置 |
| C.Ⅱ裝置中玻璃管內有水冷凝 |
| D.CuO沒有全部被還原 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com