
(14分)X、Y、Z、Q、R是五種短周期元素,原子序數依次增大。X、Y兩元素最高正價與最低負價之和均為0;Q與X同主族;Z、R分別是地殼中含量最高的非金屬元素和金屬元素。請回答下列問題:
(1)五種元素原子半徑由大到小的順序是(寫元素符號)
(2)X與Y能形成多種化合物,其中既含極性鍵又含非極性鍵,且相對分子質量最小的物質(寫分子式)
(3)由以上某些元素組成的化合物A、B、C、D有如下轉化關系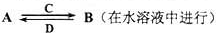
其中C是溶于水顯酸性的氣體;D是淡黃色固體。
寫出C的結構式 ;D的電子式 。
①如果A、B均由三種元素組成,B為兩性化合物,且不溶于水,則由A轉化為B的離子方程式為 。
②如果A由三種元素組成,B由四種元素組成,A、B溶液均顯堿性。用離子方程式表示A溶液顯堿性的原因 。
A、B濃度均為0.1mol/L等體積的混合溶液中,離子濃度由大到小的順序為 。
(1)Na>Al>C>O>H (2)C2H2 (3) 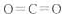
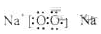
①AlO2-+2H2O+CO2=Al(OH)3↓+HCO3- 或2 AlO2-+3 H2O+CO2="2" Al(OH) 3 ↓+CO32-
②CO32-+H2O HCO3-+OH-, c(Na+)> c(HCO3-)> c(CO32-)> c(OH-) >c(H+)
HCO3-+OH-, c(Na+)> c(HCO3-)> c(CO32-)> c(OH-) >c(H+)
解析試題分析:X、Y、Z、Q、R是五種短周期元素,原子序數依次增大, Z、R分別是地殼中含量最高的非金屬元素和金屬元素,則Z為氧元素、R為Al元素;X、Y兩元素最高正價與最低負價之和均為0,且Q與X同主族,因為最高正價與最低負價之和為0的元素可能為H、C、Si,所以X為氫元素,Q為Na元素,Y為碳元素。
(1)同周期自左而右原子半徑逐漸減小,電子層越多,原子半徑越大,故原子半徑由大到小的順序為:Na>Al>C>O>H。
(2)H與C形成多種化合物,屬于烴類物質,其中既含極性鍵又含非極性鍵,且相對分子質量最小是C2H2。
(3)C是溶于水顯酸性的氣體,則C為CO2,D是淡黃色固體,則D為Na2O2,則:
CO2的結構式為O=C=O,Na2O2的電子式為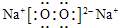 ,
,
①如果A、B均由三種元素組成,B為兩性不溶物,結合轉化關系可知,A為偏鋁酸鈉、B為氫氧化鋁,偏鋁酸根與二氧化碳、水反應生成氫氧化鋁與碳酸根或碳酸氫根,反應離子方程式為:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3- 或2 AlO2-+3 H2O+CO2="2" Al(OH) 3 ↓+CO32-
如果A由三種元素組成,B由四種元素組成,A、B溶液均顯堿性,結合轉化關系可知,A為碳酸鈉、B為碳酸氫鈉,溶液中碳酸根水解CO32-+H2O HCO3-+OH-, 破壞水的電離平衡,溶液呈堿性;碳酸鈉、碳酸氫鈉均為0.1mol?L-1的混合溶液中,鈉離子濃度最大,碳酸根、碳酸氫根水解,溶液呈堿性,碳酸根的水解程度大于碳酸氫根,故離子濃度由大到小的順序是c(Na+)> c(HCO3-)> c(CO32-)> c(OH-) >c(H+)。
HCO3-+OH-, 破壞水的電離平衡,溶液呈堿性;碳酸鈉、碳酸氫鈉均為0.1mol?L-1的混合溶液中,鈉離子濃度最大,碳酸根、碳酸氫根水解,溶液呈堿性,碳酸根的水解程度大于碳酸氫根,故離子濃度由大到小的順序是c(Na+)> c(HCO3-)> c(CO32-)> c(OH-) >c(H+)。
考點:本題考查元素的推斷、化學用語、元素周期律、化學鍵與結構、離子方程式書寫、離子濃度比較。


科目:高中化學 來源: 題型:單選題
已知甲、乙、丙、X是4種中學化學中常見的物質,其轉化關系符合下圖。則甲和X不可能是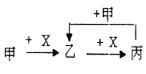
A.甲:Na、X:O2 B.甲:NaOH溶液、X:CO2溶液
C.甲:C、X:O2 D.甲:AlCl3溶液、X:NaOH溶液
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下圖是一些中學常見的物質之間的轉化關系(其中部分反應產物省略),其中A和B常溫下都是氣體,且水溶液都有漂白性;I是一種金屬單質; F、M、N均為難溶于水的白色沉淀,其中M和N不溶于稀硝酸; C和D是兩種常見的強酸。請回答下列問題: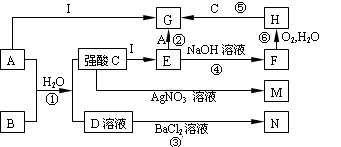
(1)寫出物質B和M的化學式:B. ,M ;
(2)寫出反應②的離子方程式: ;
(3)寫出反應⑥的化學方程式: ;
(4)在反應①②③④⑤⑥中,屬于氧化還原反應的有: 。(填編號)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在下列物質轉化關系中,反應的條件和部分產物已略去。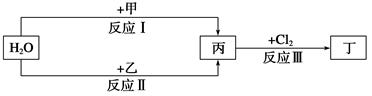
回答下列問題:
(1)若甲、乙是兩種常見金屬,反應Ⅲ是工業制鹽酸的反應。
①反應Ⅰ中,甲在通常條件下和水劇烈反應,除丙外,還生成一種焰色反應為黃色的物質,則工業上生產甲的一般方法是________(填字母)。
A.熱分解法 B.熱還原法 C.電解法
②反應Ⅱ中,乙與H2O在高溫下反應,除丙外,還生成一種有磁性的物質,則反應Ⅱ的化學方程式是______________________________________。
③通過比較反應Ⅰ、Ⅱ的反應條件,可得出甲的金屬性比乙的金屬性________(填“強”或“弱”),比較二者金屬性強弱的依據還可以是(寫出一種即可)__________________。
(2)若甲、乙是化合物,且反應Ⅲ是工業制漂白粉的反應。
①反應Ⅲ的化學方程式是__________________________________________________。
②反應Ⅰ的另一種產物為有機物,則該有機物的電子式是______________。
③在飽和氯水中加塊狀石灰石,能制得較濃HClO溶液,同時放出一種氣體。其反應的離子方程式是______________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2014年全運會在遼寧舉辦,其開幕式就是一場焰火盛宴。
(1)焰火利用了部分金屬元素特征的________反應,該反應屬于________(填“物理”或“化學”)變化。
(2)如圖所示的五元環代表A、B、C、D、E五種化合物,圓圈交叉部分指兩種化合物含有一種相同元素,五種化合物由五種短周期元素組成,每種化合物僅含兩種元素。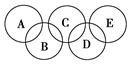
圖中A是沼氣的主要成分,B、E分子中所含電子數均為18,B不穩定,具有較強的氧化性,其稀溶液是醫療上廣泛使用的消毒劑,E分子結構的球棍模型為 ,C與純堿在高溫下的反應是工業制玻璃的主要反應之一,D中所含兩種元素的原子個數比為3∶4,電子總數之比為3∶2。根據以上信息回答下列問題:
,C與純堿在高溫下的反應是工業制玻璃的主要反應之一,D中所含兩種元素的原子個數比為3∶4,電子總數之比為3∶2。根據以上信息回答下列問題:
①B的水溶液呈弱酸性,其主要的電離方程式可表示為________________,D的化學式是________。
②A、B、E中均含有的一種元素符號為________。
③C與純堿反應的化學方程式為____________________________________。
④液態B與液態E反應可生成一種單質和一種常見液體,1 mol B參加反應放出熱量Q kJ,其反應的熱化學方程式為________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下圖是由一些常見元素組成的單質及其化合物之間的轉化關系圖。常溫常壓下,D、F均為無色無味的氣體,B是最常見的無色液體,A是由單質C在D中燃燒生成的淡黃色固體;G是一種紅褐色沉淀,且G、H、I、J中都含有同一種元素(反應中生成的部分物質已略去)。請回答下列問題: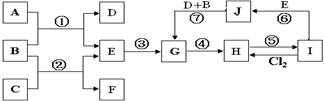
從反應②的實驗現象可以得出物質C具有的某些物理性質有(寫兩點): 。
(2)J暴露在空氣中的現象是 。
(3)①--⑦的反應中屬于非氧化還原反應的有 。
(4)反應①的化學方程式為 。
(5)將115g甲酸(HCOOH)完全燃燒后的產物通過足量的固體A中,固體A將增重 g。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知A~G有如圖所示的轉化關系(部分生成物已略去),其中A、G為單質,D是能使濕潤的紅色石蕊試紙變藍色的氣體,E、F均能與NaOH溶液反應。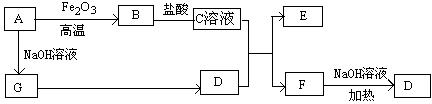
請回答下列問題:
(1)寫出F的電子式:
(2)①C溶液與D反應的離子方程式為
②F溶液與NaOH溶液共熱反應的化學方程式為
(3)①請用離子方程式解釋C溶液為何顯酸性
②F溶液中離子濃度由大到小的順序為
(4)將5.4gA投入200mL 2.0mol/L某溶液中有G單質產生,且充分反應后有金屬剩余,則該溶液可能是 (填代號)
A.HNO3溶液 B.H2SO4溶液 C.NaOH溶液 D.HCl溶液
(5)將1molN2和3molG及催化劑充入容積為2L的某密閉容器中進行反應,已知該反應為放熱反應。平衡時,測得D的物質的量濃度為a mol/L。
①如果反應速率v(G)=1.2mol/(L·min),則v(D)= mol/(L·min)
②在其他條件不變的情況下,若起始時充入0.5molN2和1.5molG達到平衡后,D的物質的量濃度 (填“大于”、“小于”或“等于”)a/2 mol/L。
③該條件下的平衡常數為 (用含a的代數式表示)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E是中學常見的幾種化合物,A、B是氧化物,元素X、Y的單質是生活中常見的金屬,相關物質間的關系如下圖所示。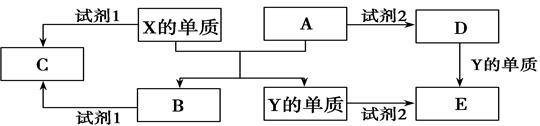
回答下列問題:
(1)X的單質與A反應的化學方程式是________________________________。
(2)若C溶液顯堿性,則試劑1是 ____溶液(寫化學式);若C溶液顯酸性,則顯酸性的原因是(用離子方程式表示) 。
(3)若試劑1和試劑2均是稀硫酸。
①檢驗物質D的溶液中金屬離子的方法是 ;
②寫出D→E反應的離子方程式 ;
③某高效凈水劑是由Y(OH)SO4聚合得到的。工業上以E、稀硫酸和亞硝酸鈉(NaNO2)為原料來制備Y(OH)SO4,反應中有NO生成,該反應的化學方程式是: 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知A~F六種常見物質中,B是空氣的主要成分之一,其他均是常見的化合物,其中E是一種常見的溶劑,F是一種溫室氣體。它們之間的轉化關系如圖所示。下列說法中正確的是 ( )。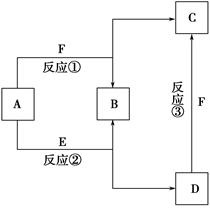
| A.化合物A是一種堿性氧化物 |
| B.圖中①②③三個反應均為氧化還原反應 |
| C.化合物D是一種強堿 |
| D.化合物C的水溶液呈酸性 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com