
【題目】稀土元素是指元素周期表中原子序數為57到71的15種鑭系元素,以及與鑭系元素化學性質相似的鈧(Sc)和釔(Y)共17種元素。稀土元素有“工業維生素”的美稱,如今已成為極其重要的戰略資源。
(1)鈧(Sc)為21號元素,位于周期表的_____區,基態原子價電子排布圖為_______。
(2)離子化合物Na3[Sc(OH)6]中,存在的化學鍵除離子鍵外還有_______。
(3)Sm(釤)的單質與l,2-二碘乙烷可發生如下反應:Sm +ICH2CH2I→SmI2+CH2=CH2。
ICH2CH2I中碳原子雜化軌道類型為______, lmol CH2=CH2中含有的σ鍵數目為______。常溫下l,2-二碘乙烷為液體而乙烷為氣體,其主要原因是__________。
(4) PrO2(二氧化鐠)的晶體結構與CaF2相似,晶飽中Pr(鐠)原子位于面心和頂點。則PrO2(二氧化鐠)的晶胞中有________個氧原子。
(5)Ce(鈰)單質為面心立方晶體,其晶胞參數a=516pm。晶胞中Ce(鈰)原子的配位數為_______,列式表示Ce(鈰)單質的密度:________g/cm3(用NA表示阿伏伽德羅常數的值,不必計算出結果)
【答案】 d 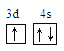 共價鍵和配位鍵 sp3 3.01×1024或5NA 二碘乙烷的相對分子質量較大,分子間作用力較強,沸點相對較高。 8 12
共價鍵和配位鍵 sp3 3.01×1024或5NA 二碘乙烷的相對分子質量較大,分子間作用力較強,沸點相對較高。 8 12 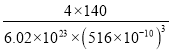 或
或
【解析】(1)鈧為21號元素,核外電子層排布為2、8、9、2,電子排布式為1s22s22p63s23p63d14s2,則鈧元素位于周期表的d區,基態原子價電子排布圖為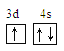 ;
;
(2)離子化合物 Na3[Sc(OH)6]中含有羥基與Sc的配位鍵,羥基中的氫氧元素之間的共價鍵;
(3)在ICH2CH2I分子中碳原子只形成了單鍵,有四個單鍵,故碳原子雜化軌道類型為sp3;1個CH2=CH2分子中含有5個σ鍵,故1mol CH2=CH2中含有的σ鍵數目為5NA,由于二碘乙烷的相對分子質量較大,分子間作用力較強,沸點相對較高,所以常溫下1,2-二碘乙烷為液體而乙烷為氣體;
(4)在晶胞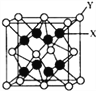 中,Y為鐠原子,X為氧原子,可以看到氧原子在晶胞的內部,故此晶胞中應有8個氧原子;
中,Y為鐠原子,X為氧原子,可以看到氧原子在晶胞的內部,故此晶胞中應有8個氧原子;
(5)Ce(鈰)單質為面心立方晶體,以晶胞頂點的鈰原子為例,與之距離最近的鈰原子分布在經過該頂點的所有立方體的面心上,這樣的面有12個,晶胞中鈰原子位于頂點和面心,數目為8×1/8+6×1/2=4,該晶胞體積為a3,該晶胞的質量為4M/NA,根據ρ=![]() 可知,密度為4M/NA×a3gcm-3,即為
可知,密度為4M/NA×a3gcm-3,即為![]() =
=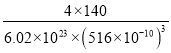 g/cm3。
g/cm3。


 手拉手全優練考卷系列答案
手拉手全優練考卷系列答案科目:高中化學 來源: 題型:
【題目】某小組同學利用原電池裝置探究物質的性質。
資料顯示:原電池裝置中,負極反應物的還原性越強,或正極反應物的氧化性越強,原電池的電壓越大。 |
(1)同學們利用下表中裝置進行實驗并記錄。
裝置 | 編號 | 電極A | 溶液B | 操作及現象 |
| Ⅰ | Fe | pH=2的 H2SO4 | 連接裝置后,石墨表面產生無色氣泡;電壓表指針偏轉 |
Ⅱ | Cu | pH=2的H2SO4 | 連接裝置后,石墨表面無明顯現象;電壓表指針偏轉,記錄讀數為a |
①同學們認為實驗Ⅰ中鐵主要發生了析氫腐蝕,其正極反應式是_________。
②針對實驗Ⅱ現象:甲同學認為不可能發生析氫腐蝕,其判斷依據是_________;乙同學認為實驗Ⅱ中應發生吸氧腐蝕,其正極的電極反應式是_________。
(2)同學們仍用上述裝置并用Cu和石墨為電極繼續實驗,探究實驗Ⅱ指針偏轉原因及影響O2氧化性的因素。
編號 | 溶液B | 操作及現象 |
Ⅲ | 經煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆蓋,連接裝置后,電壓表指針微微偏轉,記錄讀數為b |
Ⅳ | pH=2的H2SO4 | 在石墨一側緩慢通入O2并連接裝置,電壓表指針偏轉,記錄讀數為c;取出電極,向溶液中加入數滴濃Na2SO4溶液混合后,插入電極,保持O2通入,電壓表讀數仍為c |
Ⅴ | pH=12的NaOH | 在石墨一側緩慢通入O2并連接裝置,電壓表指針偏轉,記錄讀數為d |
①丙同學比較實驗Ⅱ、Ⅲ、Ⅳ的電壓表讀數為:c>a>b,請解釋原因是_________。
②丁同學對Ⅳ、Ⅴ進行比較,其目的是探究對O2氧化性的_________影響。
③實驗Ⅳ中加入Na2SO4溶液的目的是_________。
④為達到丁同學的目的,經討論,同學們認為應改用右圖裝置對Ⅳ、Ⅴ重復進行實驗,其設計意圖是_________;重復實驗時,記錄電壓表讀數依次為c′、d′,且c′>d′,由此得出的結論是_________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知X、Y、Z都是短周期元素,它們的原子序數依次遞增,X原子的電子層數與它的核外電子總數相等,而Z原子的最外層電子數是次外層的3倍,Y和Z可以形成兩種以上氣態化合物,則下列說法錯誤的是
A. Y和Z可以組成元素質量比為7:16的化合物
B. X和Y可以組成原子個數比分別為3:l和2:l的兩種化合物
C. 由X、Y、Z三種元素中任意兩種組成的具有10電子的微粒多于2種
D. X、Y、Z只能組成一種鹽,其中X、Y、Z原子個數比為4:2:3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】苯是工業上常用的化工原料,可以用于合成安息香酸芐酯和高分子化合物G (部分反應條件略去),流程如下所示,請回答下列問題:
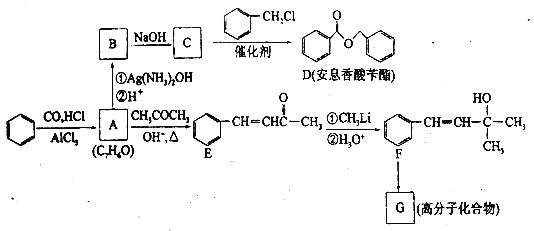
(1)A的化學名稱是________,B中的官能團名稱是________。
(2)E分子中最多可能有_____個碳原子共平面;G的結構簡式為_________;
(3)C生成D的反應類型為___________。
(4)A生成E的化學方程式為_________________。
(5)H是D的同分異構體,分子中含有酯基,有兩個苯環且不直接相連,符合上述條件的結構有_______種,其中核磁共振氫譜有6組峰,且面積比為3:2:2:2:2:1的同分異構體的結構簡式為_______(寫出一種即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在標準狀況下,將某X氣體V L溶于水中,得到12mol·L-1的溶液500mL,則氣體的體積V是( )
A.134.4L B.67.2L C.44.8L D.537.6L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示:A、B、C、D是初中化學中常見的不同類別的物質,已知A、B是空氣中的兩種氣體,“![]() ”表示兩種物質在一定條件下可相互轉變。
”表示兩種物質在一定條件下可相互轉變。
![]()
依據給出的信息推斷并回答下列問題:
(1)自然界B可通過_______________轉化為A;
(2)B物質的一種用途是____________________;
(3)D物質所屬的類別是____________________;
(4)C轉化為B的微觀實質是_______________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com