
分析 (1)依據配制溶液體積選擇合適的容量瓶;依據C=$\frac{1000ρω}{M}$計算濃硫酸物質的量濃度;依據溶液稀釋過程中溶質的物質的量不變計算需要濃硫酸的體積;
(2)用濃硫酸配制一定物質的量濃度溶液一般步驟:計算、量取、稀釋、移液、洗滌、定容、搖勻、裝瓶、貼標簽,據此選擇使用儀器;
(3)分析操作對溶質的物質的量和溶液體積的影響,依據C=$\frac{n}{V}$進行誤差分析;
解答 解:(1)需要配制450mL 1mol•L-1硫酸溶液,應選擇500mL容量瓶;質量分數為98%、密度為1.84g•cm-3的濃硫酸物質的量濃度C=$\frac{1000×1.84×98%}{98}$=18.4mol/L,設需要濃硫酸體積為V,則依據溶液稀釋過程中溶質的物質的量不變得:18.4mol/L×V=500mL×1mol/L,解得V=27.2mL;
故答案為:27.2 500;
(2)用濃硫酸配制一定物質的量濃度溶液一般步驟:計算、量取、稀釋、移液、洗滌、定容、搖勻、裝瓶、貼標簽依次用到的儀器:量筒、燒杯、玻璃棒、容量瓶、膠頭滴管、細口試劑瓶、標簽紙,所以正確的順序為:⑤④②⑥⑦⑧⑨;
故答案為:⑤④②⑥⑦⑧⑨;
(3)①用以稀釋硫酸的燒杯未洗滌,導致部分溶質損耗,溶質的物質的量偏小,溶液濃度偏低;
②未經冷卻趁熱將溶液注入容量瓶中,冷卻后,溶液體積偏小,溶液濃度偏高;
③定容時觀察液面俯視,導致溶液體積皮偏小,溶液濃度偏高;
故答案為:①偏低 ②偏高 ③偏高.
點評 本題考查了一定物質的量濃度溶液的配制,明確配制原理及操作步驟是解題關鍵,注意誤差分析的方法和技巧.


 津橋教育計算小狀元系列答案
津橋教育計算小狀元系列答案科目:高中化學 來源: 題型:解答題
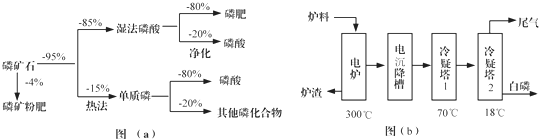
| 熔點/℃ | 沸點/℃ | 備注 | |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 難溶于水、有還原性 |
| SiF4 | -90 | -86 | 易水解 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
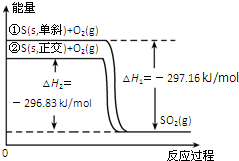
| A. | 單斜硫轉化為正交硫的反應是吸熱反應 | |
| B. | 正交硫比單斜硫穩定 | |
| C. | 相同物質的量的正交硫比單斜硫所含有的能量高 | |
| D. | ①表示斷裂1mol O2中的共價鍵所吸收的能量比形成lmolSO2中的共價鍵所放出的能量少297.16 kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
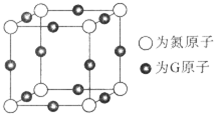 A、B、C、D、E、F、G是前四周期(除稀有氣體)原子序數依次增大的七種元素,A的原子核外電子只有一種運動狀態;B、C的價電子層中未成對電子數都 是2;B、C、D同周期;E核外的s、p能級的電子總數相;F與E同周期且第一電離能比E小;G的+1價離子(G+)的各層電子全充滿.回答下列問題:(相關問題用元素符號表示)
A、B、C、D、E、F、G是前四周期(除稀有氣體)原子序數依次增大的七種元素,A的原子核外電子只有一種運動狀態;B、C的價電子層中未成對電子數都 是2;B、C、D同周期;E核外的s、p能級的電子總數相;F與E同周期且第一電離能比E小;G的+1價離子(G+)的各層電子全充滿.回答下列問題:(相關問題用元素符號表示)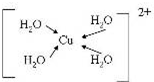 (配位鍵用→標出).
(配位鍵用→標出).查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com