
| A. | NH3中氮原子為sp2雜化,而CH4中碳原子是sp3雜化 | |
| B. | NH3中N原子形成三個雜化軌道,CH4中C原子形成4個雜化軌道 | |
| C. | NH3分子中有一對未成鍵的孤對電子,它對成鍵電子的排斥作用較強 | |
| D. | NH3分子中有三個σ鍵,而甲烷分子中有四個σ鍵 |
分析 NH3中N原子成3個σ鍵,有一對未成鍵的孤對電子,雜化軌道數為4,采取sp3型雜化雜化,孤對電子對成鍵電子的排斥作用較強,氨氣分子空間構型是三角錐形;CH4分子中C原子采取sp3型雜化雜化,雜化軌道全部用于成鍵,碳原子連接4個相同的原子,為正四面體構型.
解答 解:價層電子對數=σ 鍵個數+$\frac{1}{2}$(a-xb),a指中心原子價電子個數,x指配原子個數,b指配原子形成穩定結構需要的電子個數,氨氣分子中,NH3中N原子成3個σ鍵,有一對未成鍵的孤對電子,價層電子對數=3+$\frac{1}{2}$(5-3×1)=4,所以采取sp3雜化,孤對電子對成鍵電子的排斥作用較強,N-H之間的鍵角小于109°28′,所以氨氣分子空間構型是三角錐形;
CH4分子中C原子雜化軌道數=δ鍵數+孤對電子對數=4+0=4,所以采取sp3雜化,雜化軌道全部用于成鍵,碳原子連接4個相同的原子,C-H之間的鍵角相等為109°28′,故CH4為正四面體構型,
故選C.
點評 本題考查了分子空間構型的判斷,注意理解價層電子對互斥理論與雜化軌道理論,題目難度中等.


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案科目:高中化學 來源: 題型:解答題
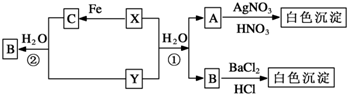
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②③⑥ | B. | ①③⑥ | C. | ①④⑤ | D. | ②③④⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
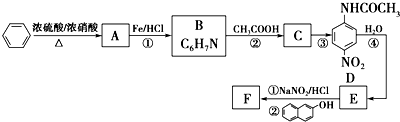
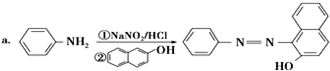
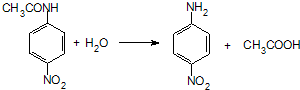 .
.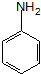 ;設計反應②和④的目的是保護氨基不被氧化.
;設計反應②和④的目的是保護氨基不被氧化.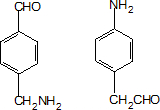 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
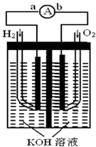 氫氧燃料電池是符合綠色化學理念的新型發電裝置.如圖為電池示意圖,該電池電極表面鍍一層細小的鉑粉,鉑吸附氣體的能力強,性質穩定,請回答:
氫氧燃料電池是符合綠色化學理念的新型發電裝置.如圖為電池示意圖,該電池電極表面鍍一層細小的鉑粉,鉑吸附氣體的能力強,性質穩定,請回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 12C和14C互為同位素 | |
| B. | 乙醇與二甲醚(CH3-O-CH3)互為同分異構體 | |
| C. | H2O與D2O互為同位素 | |
| D. | 紅磷與白磷互為同素異形體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
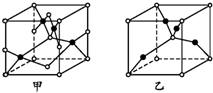 已知A、B、C、D、E五種元素的原子序數依次增大,其中A原子所處的周期數、族序數都與其原子序數相等;B原子核外電子有6種不同的運動狀態;D原子L電子層上有2對成對電子;E+原子核外有3層電子且各層均處于全滿狀態.
已知A、B、C、D、E五種元素的原子序數依次增大,其中A原子所處的周期數、族序數都與其原子序數相等;B原子核外電子有6種不同的運動狀態;D原子L電子層上有2對成對電子;E+原子核外有3層電子且各層均處于全滿狀態. .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com