
【題目】CO2的轉化和重整受到越來越多的關注,它是有效應對全球氣候變化、促進低碳社會構建的重要方法。
(1)熱化學轉化法。
CO2催化加氫合成CH4,其過程中主要發生下列反應:
反應Ⅰ:CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-890.3 kJ·mol-1
反應Ⅱ:CO(g)+H2O (g)=CO2(g)+H2(g);ΔH=+2.8 kJ·mol-1
反應Ⅲ:2CO(g)+O2(g)=2CO2(g);ΔH=-566.0 kJ·mol-1
則反應CO2(g)+4H2(g)=CH4(g)+2H2O(g) 的ΔH=________kJ·mol-1。
(2)CO2催化還原法。
圖1表示的是利用CO2的“直接電子傳遞機理”。在催化劑銅的表面進行轉化。當有1 mol CO2反應時,直接傳遞的電子物質的量為________mol。
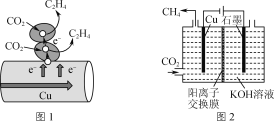
(3)CO2電化學催化重整法。
①圖2表示以KOH溶液作電解質溶液進行電解的示意圖,CO2在Cu電極上可以轉化為CH4,該電極反應的方程式為______________________,電解一段時間后,陽極區溶液pH減小,其原因是__________________。
②CO2與CH4在催化劑作用下合成乙酸,反應的化學方程式為________。
(4)CO2與丙烯通過金屬雜多酸鹽[CoxH(3-2x)PW12O40] 催化合成甲基丙烯酸。
①研究發現金屬雜多酸鹽中x對CO2轉化率的影響如圖3所示,由圖3得出催化效果最好的金屬雜多酸鹽化學式是________。
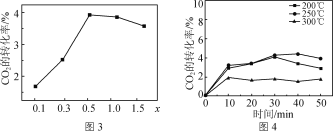
②催化劑在溫度不同時對CO2轉化率的影響如圖4所示,300 ℃催化效果遠不如200 ℃ 和250 ℃的原因為__________________________________。
【答案】-252.9 6 CO2+8e-+6H2O=CH4+8OH- OH-在陽極被氧化生成O2 CH4+CO2![]() CH3COOH [Co0.5H2PW12O40]或[CoH4P2W24O80] 溫度過高,可能會導致催化劑失活
CH3COOH [Co0.5H2PW12O40]或[CoH4P2W24O80] 溫度過高,可能會導致催化劑失活
【解析】
(1)根據蓋斯定律可知-反應Ⅰ-4×反應Ⅱ+2×反應Ⅲ即可得到CO2(g)+4H2(g)=CH4(g)+2H2O(g),據此計算ΔH;
(2)由圖1可知CO2在催化劑銅的表面進行轉化最終生成的產物是C2H4,根據發生的氧化還原反應確定傳遞的電子的量;
(3)①由圖2可知,Cu與電源的負極相連,為陰極,陰極發生了還原反應;在陽極區OH-在被氧化生成O2;
②CO2與CH4在催化劑作用下發生化合反應生成乙酸;
(4)①由圖3可知,當x=0.5時,CO2的轉化率最大,催化效果最好,由此可確定金屬雜多酸鹽化學式;
②當處于過高的溫度時,催化劑會失去催化活性。
(1)根據蓋斯定律可知-反應Ⅰ-4×反應Ⅱ+2×反應Ⅲ即可得到CO2(g)+4H2(g)=CH4(g)+2H2O(g),ΔH=-(-890.3 kJ·mol-1)-4×(2.8 kJ·mol-1)+2×(-566.0 kJ·mol-1)=-252.9 kJ·mol-1;
(2)由圖1可知CO2在催化劑銅的表面進行轉化最終生成的產物是C2H4,根據發生的氧化還原反應可的關系:2CO2~C2H4~12e-,因此當有1 mol CO2反應時,直接傳遞的電子物質的量為6mol;
(3)①由圖2可知,Cu與電源的負極相連,為陰極,陰極發生了還原反應,電極反應為:CO2+8e-+6H2O=CH4+8OH-;OH-在陽極被氧化生成O2,因此陽極區溶液的pH減小;
②CO2與CH4在催化劑作用下發生化合反應生成乙酸,反應方程式為:CH4+CO2![]() CH3COOH;
CH3COOH;
(4)①由圖3可知,當x=0.5時,CO2的轉化率最大,催化效果最好,因此金屬雜多酸鹽化學式為Co0.5H2PW12O40或CoH4P2W24O80;
②當處于過高的溫度時,催化劑會失去催化活性,因此300 ℃催化效果遠不如200 ℃和250 ℃。


 口算題卡加應用題集訓系列答案
口算題卡加應用題集訓系列答案科目:高中化學 來源: 題型:
【題目】(1)在常溫下的0.05 mol·L-1硫酸溶液中,c(H+)=_______mol·L-1,水電離出的c(H+)=___________mol·L-1,水電離出的c(OH-)=_________ mol·L-1。
(2)某溫度下,純水的c(H+)=2×10-7 mol·L-1,則此時c(OH-)為_____________mol·L-1。若溫度不變,滴入稀鹽酸使c(H+)=5×10-4 mol·L-1,則溶液中c(OH-)為_______________mol·L-1,此時溫度_______(填“高于”、“低于”或“等于”)25 ℃。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在給定條件下,下列選項所示的物質間轉化均能實現的是( )
A.Na(s)![]() Na2O(s)
Na2O(s)![]() NaOH(aq)
NaOH(aq)
B.Al2O3(s)![]() AlCl3(aq)
AlCl3(aq)![]() Al(s)
Al(s)
C.CaSO4(s)![]() CaCO3(s)
CaCO3(s)![]() Ca(NO3)2(aq)
Ca(NO3)2(aq)
D.Fe2O3(s)![]() Fe(s)
Fe(s)![]() Fe2(SO4)3(aq)
Fe2(SO4)3(aq)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】萜類化合物廣泛存在于動植物體內,關于下列萜類化合物的說法正確的是( )

A. a和b都屬于芳香族化合物
B. a和c分子中所有碳原子均處于同一平面上
C. a、b和c均能使酸性KMnO4溶液褪色
D. b和c均能與新制的Cu(OH)2反應生成紅色沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖為氫氧燃料電池原理示意圖,按照此圖的提示,下列敘述不正確的是
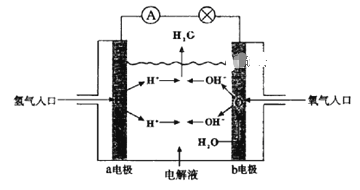
A. a電極是負極
B. 氫氧燃料電池是一種具有應用前景的綠色電源
C. b電極的電極反應為:4OH--4e-=2H2O+O2↑
D. 氫氧燃料電池是一種不需要將還原劑和氧化劑全部儲藏在電池內的新型發電裝置
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一氯甲烷等鹵代烴跟苯的反應如圖所示,(無機小分子產物略去)。下列說法正確的是

A. 該反應屬于化合反應
B. b的二氯代物有6種結構
C. 1mol b加氫生成飽和烴需要6molH2
D. C5H11Cl的結構有8種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. lmol 該有機物( )最多能與4mol 氫氣加成
)最多能與4mol 氫氣加成
B. 乙醛和丙烯醛(![]() )不是同系物,它們與氫氣充分反應后的產物也不是同系物
)不是同系物,它們與氫氣充分反應后的產物也不是同系物
C. 乳酸薄荷醇酯( )僅能發生水解、氧化、消去反應
)僅能發生水解、氧化、消去反應
D.  分子中至少有9個碳原子處于同一平面上
分子中至少有9個碳原子處于同一平面上
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對 的表述不正確的是
的表述不正確的是
A. 該物質能發生酯化反應,氧化反應。
B. 1 mol該物質最多消耗Na、NaOH、NaHCO3的物質的量之比為2:2:1
C. 該物質遇FeCl3溶液顯色,1mol該物質最多能與含1mol Br2的溴水發生取代反應
D. 該物質有7種不同環境的氫原子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室模擬合成![]() 和CH3CH2CH2Br的方法如圖1。
和CH3CH2CH2Br的方法如圖1。
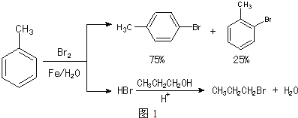
已知:甲苯和液溴在有少量水存在時也能反應(如圖2):

實驗室模擬合成對溴甲苯和1-溴丙烷的流程和相關數據如表:
物質 | 甲苯 | 1-丙醇 | 1-溴丙烷 | 對溴甲苯 | 鄰溴甲苯 |
沸點(℃) | 110.8 | 97.2 | 71 | 184.3 | 181.7 |
(1)實驗室存放液溴的試劑瓶需密閉,同時瓶中要加入____,以減少溴的揮發.寫出甲苯和液溴反應生成對溴甲苯的化學方程式___。
(2)反應裝置如圖3所示:
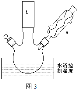
①圖中玻璃儀器a的名稱是____,方塊b中為某玻璃儀器,其名稱是___。
②三頸燒瓶中開始加入了甲苯、鐵粉和水。加入的適量水的作用是:易于控制溫度和____,加熱攪拌操作中加入濃硫酸,完成1-丙醇的取代反應,濃硫酸的作用是____。
(3)操作I的名稱是___,操作Ⅲ的名稱是___。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com