
| m |
| M |
| 1.1×10-10 |
| 1×10-6 |
| 0.5825g |
| 233g/mol |
| 5 |
| 2 |
| 25mL |
| 100mL |


 培優好卷單元加期末卷系列答案
培優好卷單元加期末卷系列答案科目:高中化學 來源: 題型:
| A、汽車尾氣中有NOx,主要是汽油不充分燃燒引起的 |
| B、日用鋁制品表面覆蓋著氧化膜,對金屬起保護作用 |
| C、大氣中CO2含量的增加會導致溫室效應加劇 |
| D、NO2或SO2都會導致酸雨的形成 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、① | B、②③④ |
| C、③④ | D、①②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:
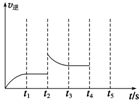 已知合成氨的反應為N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ?mol-1.
已知合成氨的反應為N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ?mol-1.查看答案和解析>>
科目:高中化學 來源: 題型:
A、 制取少量蒸餾水 |
B、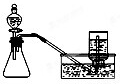 用銅和濃硝酸混合制取少量NO2 |
C、 比較MnO2、Cl2、I2的氧化性 |
D、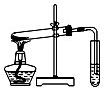 探究NaHCO3的熱穩定性 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、9.0L | B、13.5L |
| C、10.7L | D、16.8L |
查看答案和解析>>
科目:高中化學 來源: 題型:

| A、與鄰羥基苯甲酸互為同分異構體,苯環上一氯代物僅有2種且能發生銀鏡反應的酚類化合物共有3種 |
| B、用酸性KMnO4溶液直接氧化鄰羥基苯甲醛可實現反應① |
| C、反應②中加入過量的NaHCO3有利提高阿司匹林的產率 |
| D、1mol阿司匹林最多可以和2molNaOH反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、含氮、磷化合物的生活污水大量排放可使水體富營養化,造成潮汐 |
| B、各國工業大量排放二氧化硫是全球氣候變暖的主要原因 |
| C、劣質裝修材料中的甲醛、苯、氡氣等對人體有害 |
| D、廢舊電池中的汞、鎘、鉛等重金屬鹽對土壤和水源會造成污染 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com