
下列離子方程式正確的是
A.以石墨作電極電解CuCl2溶液:2Cl-+2H2O=2OH-+Cl2↑十H2↑
B.雙氧水加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O
C.Na2O2溶于水產生O2:Na2O2+H2O=2Na++2OH-+O2↑
D.Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O
科目:高中化學 來源:2015-2016學年河北省高二上12月月考化學試卷(解析版) 題型:選擇題
鋼鐵在潮濕的空氣中會被腐蝕,發生的原電池反應為:2Fe+2H2O+O2=2Fe2++4OH-。以下說法正確的是
A.負極發生的反應為:Fe-2e-==Fe2+
B.正極發生的反應為:2H2O+O2+2e-==4OH-
C.原電池是將電能轉變為化學能的裝置
D.鋼柱在水下部分比在空氣與水交界處更容易腐蝕
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高一上學期12月月考化學試卷(解析版) 題型:選擇題
設NA為阿伏加德羅常數的數值,下列說法正確的是
A.Na2O2與水反應時,1 mol Na2O2轉移1 mol電子
B.78gNa2O2含有陰、陽離子總數是4NA
C.1mo1•L﹣1的AlC13溶液中,C1﹣離子的數目為3 NA
D.5.6 g鐵與足量鹽酸反應轉移的電子數為0.3 NA
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江西省高一上學期12月月考化學試卷(解析版) 題型:選擇題
下列各組中的兩物質相互反應時,產物不隨反應條件(溫度、反應物用量比等 )改變而改變的是
)改變而改變的是
A.Na和O2 B.Ca(OH)2和CO2 C.NaOH和HCl D.Na2CO3和HCl
查看答案和解析>>
科目:高中化學 來源:2016屆福建省閩粵聯合體高三上學期第三次聯考化學試卷(解析版) 題型:選擇題
下列有關離子檢驗的操作和實驗結論都正確的是
選項 | 實驗操作及現象 | 實驗結論 |
A | 向某溶液中加入氯化鋇溶液,有白色沉淀生成,再加鹽酸酸化,沉淀不溶解 | 該溶液中一定含有SO42- |
B | 濃硫酸滴入蔗糖中,攪拌得黑色蓬松的固體并有刺激性氣味 | 該過程中濃硫酸僅體現吸水性和脫水性 |
C | 在酒精燈上加熱鋁箔,鋁箔熔化,但不滴落,好像有一層膜兜著 | 鋁易被氧化;鋁的熔點比氧化鋁低 |
D | 向某溶液中加入稀鹽酸,產生能使澄清石灰水變渾濁的無色氣體 | 該溶液中一定含有CO32- |
查看答案和解析>>
科目:高中化學 來源:2016屆山東省臨沂市高三上學期期中考試化學試卷(解析版) 題型:填空題
運用元素周期律研究元素及其化合物的性質具有重要的意義。
I.部分短周期主族元素的最高價氧化物對應的水化物(濃度均為0.01mol.L-1)溶液的PH和原子序數的關系如下圖所示。
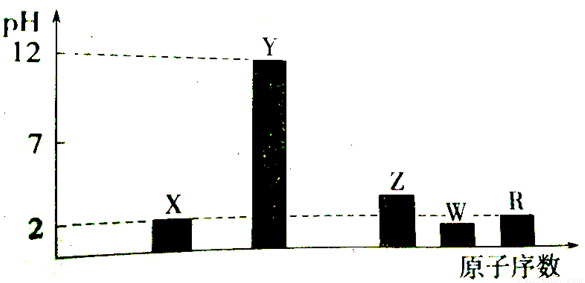
(1)元素R在周期表中的位置是 。
(2)元素Y和W形成的Y2W2型化合物中含有化學鍵的類型為 。
(3)測定Z元素最高價氧化物對應水化物溶液物質的量濃度的方法為 。
II.短周期元素C、O、S能形成多種化合物,如CO2、CS2、COS等
(1)下列能說明碳、硫兩種元素非金屬性相對強弱的是 (填序號)
A.相同條件下水溶液的PH:Na2CO3 >Na2SO4
B.酸性:H2SO3 >H2CO3
C.CS2中碳元素為+4價,硫元素為-2價
(2)羰基硫(COS)可作為一種熏蒸劑,能防止某些昆蟲、線蟲的危害,其分子結構和CO2相似
①羰基硫(COS)的電子式為: 。
②羰基硫(COS)用氫氧化鈉溶液處理及利用的過程如下:

已知A是一種正鹽,則A的化學式為 ;若氣體a為單質,反應 II的離子方程式為 。
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省高三上1月階段測理綜化學試卷(解析版) 題型:選擇題
設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.實驗室所制得的1.7gNH3中含有的電子數為0.1NA
B.標準狀況下2.24LHF中含有HF分子數為0.1NA
C.1L0.1 mol•L-1NaHSO4溶液中含有的陽離子數目為0.1NA
D.0.1mol氯酸鉀與足量鹽酸反應生成氯氣轉移電子數為0.5NA
查看答案和解析>>
科目:高中化學 來源:2016屆浙江省金麗衢十二校高三上學期第一次聯考化學試卷(解析版) 題型:選擇題
石墨烯可看作將石墨的層狀結構一層一層地剝開得到的單層碳原子;石墨炔是平面網狀結構的全碳分子,具有優良的化學穩定性和半導體性能;將氫氣氫化到石墨烯排列的六角晶格中,使每個碳原子都增加一個氫原子可得最薄的絕緣新材料石墨烷。下列有關說法中正確的是
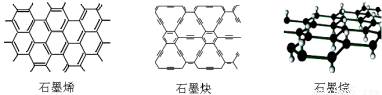
A.石墨烯、石墨炔和石墨烷互為同素異形體
B.12g石墨烯完全轉變為石墨烷需氫氣11.2L
C.石墨炔可作半導體材料,有望替代二氧化硅
D.石墨炔孔徑略大于H2分子的直徑,因此它是理想的H2提純薄膜
查看答案和解析>>
科目:高中化學 來源:2016屆黑龍江省高三上期末理綜化學試卷(解析版) 題型:填空題
研究CO2的利用對促進低碳社會的構建具有重要的意義。
(1)已知拆開1 mol H2、1 mol O2和液態水中1 mol O—H鍵使之成為氣態原子所需的能量分別為436 kJ、496 kJ和462 kJ;CH3OH(g)的燃燒熱為627 kJ·mol-1。
則CO2(g)+3H2(g)=CH3OH(g)+H2O(l) ∆H= kJ·mol-1
(2)將燃煤廢氣中的CO2轉化為二甲醚的反應原理為:
2CO2(g)+6H2(g)  CH3OCH3(g)+3H2O(l)
CH3OCH3(g)+3H2O(l)
①該反應平衡常數表達式K= 。
②已知在某壓強下,該反應在不同溫度、不同投料比時,CO2的轉化率如圖所示。該反應的∆H 0,(填“>”或“<”)。若溫度不變,減小反應投料比[n(H2)/n(CO2)],則K將 (填“增大”、“減小”或“不變”)。

③某溫度下,向體積一定的密閉容器中通入CO2(g)與H2(g)發生上述反應,當下列物理量不再發生變化時,能表明上述可逆反應達到化學平衡的是 。
A.二氧化碳的濃度 B.容器中的壓強
C.氣體的密度 D.CH3OCH3與H2O的物質的量之比
(3)向澄清的石灰水中通入CO2至溶液中的Ca2+剛好完全沉淀時,則溶液中c(CO32 -)= 。[已知:Ksp(CaCO3)=2.8×10-9]
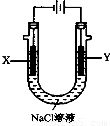
(4)以甲醚、空氣、氫氧化鉀溶液為原料的燃料電池為電源,以石墨為電極電解500 mL滴有酚酞的NaCl溶液,裝置如圖所示:請寫出電解過程中Y 電極附近觀察到的現象 ;當燃料電池消耗2.8L O2(標準狀況下)時,計算此時:NaCl溶液的pH= (假設溶液的體積不變,氣體全部從溶液中逸出)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com