
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
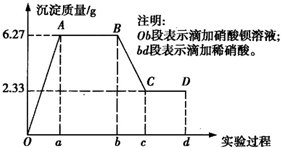 某化學研究性學習小組對某無色水樣的成分進行檢驗,已知該水樣中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO
某化學研究性學習小組對某無色水樣的成分進行檢驗,已知該水樣中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO2- 3 |
2- 4 |
查看答案和解析>>
科目:高中化學 來源: 題型:

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 (2011?泰州一模)某化學研究性學習小組為探究某品牌花生油中不飽和脂肪酸的含量,進行了如下實驗:
(2011?泰州一模)某化學研究性學習小組為探究某品牌花生油中不飽和脂肪酸的含量,進行了如下實驗:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com