
| 選項 | 實驗操作 | 現象 | 結論 |
| A | 向稀硝酸溶液中加入過量鐵粉充分反應后,滴加KSCN溶液 | 溶液變為血紅色 | 稀硝酸具有氧化性能將Fe氧化成Fe3+ |
| B | 向AgNO3溶液中滴加過量氨水 | 溶液澄清 | Ag+與NH3•H2O能大量共存 |
| C | 向裝有Fe(NO3)2溶液的試管中加入稀H2SO4 | 在管口觀察到紅棕色氣體 | HNO3分解成了NO2 |
| D | 向某溶液中滴加濃NaOH溶液,將濕潤紅色石蕊試紙置于試管口 | 試紙變藍 | 該溶液中存在NH4+ |
| A. | A | B. | B | C. | C | D. | D |
分析 A.稀硝酸溶液中加入過量鐵粉充分反應后,生成硝酸亞鐵;
B.AgNO3溶液中滴加過量氨水,生成銀氨溶液;
C.裝有Fe(NO3)2溶液的試管中加入稀H2SO4,發生氧化還原反應生成鐵離子、NO;
D.滴加濃NaOH溶液,將濕潤紅色石蕊試紙置于試管口,試紙變藍,可知生成氣體為氨氣.
解答 解:A.稀硝酸溶液中加入過量鐵粉充分反應后,生成硝酸亞鐵,則滴加KSCN溶液,無現象,故A錯誤;
B.AgNO3溶液中滴加過量氨水,生成銀氨溶液,溶液澄清,可知Ag+與NH3•H2O反應生成絡離子不能大量共存,故B錯誤;
C.裝有Fe(NO3)2溶液的試管中加入稀H2SO4,發生氧化還原反應生成鐵離子、NO,管口NO被氧化為NO2,故C錯誤;
D.滴加濃NaOH溶液,將濕潤紅色石蕊試紙置于試管口,試紙變藍,可知生成氣體為氨氣,則該溶液中存在NH4+,故D正確;
故選D.
點評 本題考查化學實驗方案的評價,為高頻考點,把握物質的性質、發生的反應及現象、離子的檢驗為解答的關鍵,側重分析與實驗能力的考查,注意元素化合物與實驗的結合及實驗的評價性分析,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 氯化銅溶液與鋅粒反應:Cu2++Zn=Zn2++Cu | |
| B. | 稀 H2SO4與鐵粉反應:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 鐵與氯化鐵溶液反應:Fe+Fe3+=2Fe2+ | |
| D. | 碳酸鈣與鹽酸反應:CO32-+2H+=H2O+CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 未冷卻就轉移、定容 | B. | 容量瓶原有少量蒸餾水 | ||
| C. | 定容時俯視刻度線觀察液面 | D. | 量筒取濃鹽酸時,俯視讀數 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 電解原理在化學工業中有廣泛應用.如圖表示一個電解池,裝有電解液a;X、Y是兩塊電極板,通過導線與直流電源相連.請回答以下問題:
電解原理在化學工業中有廣泛應用.如圖表示一個電解池,裝有電解液a;X、Y是兩塊電極板,通過導線與直流電源相連.請回答以下問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
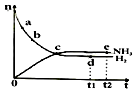 合成氨工業對國民經濟和社會發展具有重要的意義.對于密閉容器中的反應:
合成氨工業對國民經濟和社會發展具有重要的意義.對于密閉容器中的反應:| A. | 點d(t1時刻)和點e(t2時刻)處n(N2)不一樣 | |
| B. | 點c處反應達到平衡 | |
| C. | 點a的正反應速率比點b的大 | |
| D. | 其他條件不變,773 K下反應至t1時刻,n(H2)比圖中d點的值小 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
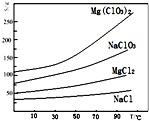 氯酸鎂[Mg(ClO3)2]常用作催熟劑、除草劑等,實驗室用鹵塊(主要成分為MgCl2•6H2O,含有MgSO4、FeCl2等雜質)制備少量Mg(ClO3)2•6H2O的流程如下:
氯酸鎂[Mg(ClO3)2]常用作催熟劑、除草劑等,實驗室用鹵塊(主要成分為MgCl2•6H2O,含有MgSO4、FeCl2等雜質)制備少量Mg(ClO3)2•6H2O的流程如下:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①⑤③⑦⑥④② | B. | ①⑤⑦③④⑥② | C. | ①⑦③⑤⑥④② | D. | ①⑦③④⑥⑤② |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com