
【題目】綠礬是含有一定量結晶水的硫酸亞鐵,在工農業生產中具有重要的用途。某化學興趣小組對綠礬的一些性質進行探究。
回答下列問題:
(1)在試管中加入少量綠礬樣品,加水溶解,滴加___溶液,溶液顏色無明顯變化,由此可知樣品中無Fe3+。
(2)為測定綠礬中結晶水含量,稱石英玻璃管(帶開關K1和K2)(設為裝置A)的質量,記為m1g。將樣品裝入石英玻璃管中,再次稱其質量,記為m2g。按如圖連接好裝置進行實驗。
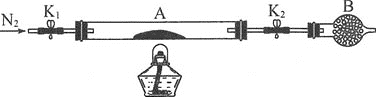
①儀器B的名稱是___。
②將下列實驗操作步驟正確排序___(填字母);重復上述操作步驟,直至A質量不變,記為m3g。
a.點燃酒精燈,加熱 b.熄滅酒精燈 c.關閉K1和K2 d.打開K1和K2,緩緩通入N2 e.稱量A f.冷卻至室溫
③根據實驗記錄,計算綠礬化學式,結晶水數目x=___。若實驗時按a、d次序操作,則使x___(填偏大偏小或無影響)。
(3)為探究硫酸亞鐵的分解產物,將(2)中已質量不變的裝置A接入如圖所示的裝置中,打開K1和K2,緩緩通入N2,加熱。實驗后反應管中殘留固體為紅色粉末。
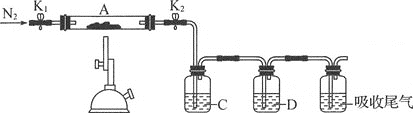
①C、D中的溶液依次為___(填字母),可觀察到C、D中有氣泡冒出。
a.品紅 b.NaOH C.BaCl2 d.Ba(NO3 )2 e.濃硫酸
②寫出硫酸亞鐵高溫分解反應的化學方程式:___。
【答案】KSCN (球形)干燥管 dabfce ![]() 偏小 c、a 2FeSO4
偏小 c、a 2FeSO4![]() Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
【解析】
(1)綠礬是FeSO4·7H2O,Fe2+與SCN-混合不顯血紅色,Fe3+與SCN-混合出現血紅色,據此分析;
(2)①根據儀器的特點判斷儀器的名稱;
②實驗時,為避免Fe2+被氧化,應先通入氮氣,冷卻水注意關閉開關,防止氧氣的進入;
③加熱綠礬,綠礬失去結晶水,即結晶水的質量為(m2-m3)g,FeSO4的質量為(m3-m1)g,a、d次序操作,造成FeSO4被氧化,據此分析;
(3)FeSO4高溫分解可生成Fe2O3、SO2、SO3,C為BaCl2溶液,用于檢驗SO3,D為品紅,用于檢驗SO2,據此分析。
(1)在試管中加入少量綠礬樣品,加水溶解。滴加KSCN溶液,溶液顏色無明顯變化,說明溶液中不存在鐵離子;
(2)![]() 據圖所示可知,儀器B的名稱是:球形干燥管;
據圖所示可知,儀器B的名稱是:球形干燥管;
![]() 將下列實驗操作步驟正確排序:打開
將下列實驗操作步驟正確排序:打開![]() 和
和![]() ,緩緩通入
,緩緩通入![]() 以趕盡裝置中的空氣;點燃酒精燈,加熱使綠礬失去結晶水;熄滅酒精燈停止實驗;冷卻至室溫;關閉
以趕盡裝置中的空氣;點燃酒精燈,加熱使綠礬失去結晶水;熄滅酒精燈停止實驗;冷卻至室溫;關閉![]() 和
和![]() 防止水蒸氣進入裝置A內;稱量A;故實驗操作步驟正確排序為:dabfce;
防止水蒸氣進入裝置A內;稱量A;故實驗操作步驟正確排序為:dabfce;
![]() 根據實驗記錄,
根據實驗記錄,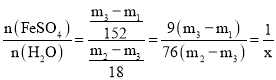 ,綠礬化學式中結晶水數目
,綠礬化學式中結晶水數目![]() ,若實驗時按先點燃酒精燈加熱,再打開
,若實驗時按先點燃酒精燈加熱,再打開![]() 和
和![]() ,則A中固體會與空氣先反應,加熱過程中硫酸亞鐵被空氣氧化為硫酸鐵,導致
,則A中固體會與空氣先反應,加熱過程中硫酸亞鐵被空氣氧化為硫酸鐵,導致![]() 增大,使x偏小;
增大,使x偏小;
(3)![]() 受熱分解可產生二氧化硫或三氧化硫,實驗C中的溶液氯化鋇檢驗吸收是否有三氧化硫,不能用硝酸鋇,因為能將二氧化硫氧化、D中的溶液為品紅用來檢驗二氧化硫的存在;
受熱分解可產生二氧化硫或三氧化硫,實驗C中的溶液氯化鋇檢驗吸收是否有三氧化硫,不能用硝酸鋇,因為能將二氧化硫氧化、D中的溶液為品紅用來檢驗二氧化硫的存在;
![]() 因為D中所盛的試劑為品紅溶液,觀察到溶液褪色,則說明產物中有二氧化硫和三氧化硫,根據氧化還原反應的原理,則生成物有氧化鐵,所以硫酸亞鐵高溫分解反應的化學方程式:
因為D中所盛的試劑為品紅溶液,觀察到溶液褪色,則說明產物中有二氧化硫和三氧化硫,根據氧化還原反應的原理,則生成物有氧化鐵,所以硫酸亞鐵高溫分解反應的化學方程式:![]() 。
。


 探究與鞏固河南科學技術出版社系列答案
探究與鞏固河南科學技術出版社系列答案科目:高中化學 來源: 題型:
【題目】已知:[FeCl4(H2O)2]-為黃色,下列實驗所得結論不正確的是( )
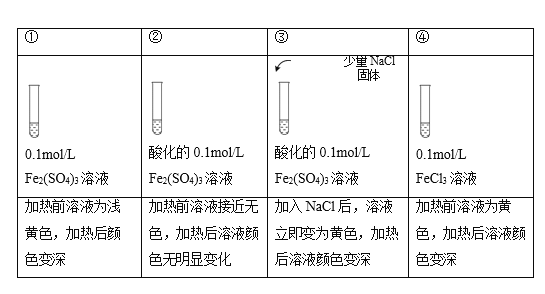
注:加熱為微熱,忽略體積變化。
A.實驗①中,Fe2(SO4)3溶液顯淺黃色原因是Fe3+水解產生了少量Fe(OH)3
B.實驗②中,酸化對Fe3+水解的影響程度大于溫度的影響
C.實驗③中,存在可逆反應: Fe3+ + 4Cl-+ 2H2O ![]() [FeCl4(H2O)2]-
[FeCl4(H2O)2]-
D.實驗④,可證明升高溫度,Fe3+水解平衡正向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室制備1,2-二溴乙烷,可用足量的乙醇先制備乙烯,再用乙烯和少量的溴制備1,2-二溴乙烷,裝置如下圖所示:
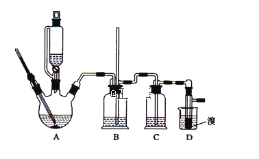
有關數據列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
狀態 | 無色液體 | 無色液體 | 無色液體 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸點/℃ | 78.5 | 132 | 34.6 |
熔點/℃ | -130 | 9 | -116 |
回答下列問題:
(1)寫出由乙醇制備乙烯的化學方程式______________________________,乙烯制備1,2-二溴乙烷的化學方程式_______________________________。
(2)在此制備實驗中,要盡可能迅速地把反應溫度提高到170℃左右,其最主要目的是___________;(填正確選項前的字母)
a.引發反應 b.加快反應速度
c.防止乙醇揮發 d.減少副產物乙醚生成
(3)在裝置A中除了濃硫酸和乙醇外,還應加入_____,其目的是_______裝置A中生成副產物乙醚的化學反應方程式 ___________________。
(4)實驗室制取乙烯,常因溫度過高而使乙醇和濃H2SO4反應生成少量的二氧化硫,為了驗證二氧化硫的存在并除去二氧化硫對后續反應的干擾,某同學在A和D之間加入了B、C兩個裝置,其中B和C中可分別盛放 ________________,
a.酸性KMnO4和水 b.品紅和NaOH溶液
c.酸性KMnO4和NaOH溶液d.品紅和酸性KMnO4
(5)將1,2-二溴乙烷粗產品置于分液漏斗中加水,振蕩后靜置,產物應在_____層(填“上”、“下”);若產物中有少量副產物乙醚。可用_______的方法除去。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 物質結構與性質
物質結構與性質![]() VA族元素單質及其化合物在工農業生產中有重要用途。回答下列問題:
VA族元素單質及其化合物在工農業生產中有重要用途。回答下列問題:
![]() 基態As原子的核外電子排布式為
基態As原子的核外電子排布式為![]() ________,有________個未成對電子。
________,有________個未成對電子。
![]() 元素周期表中,與P緊鄰的4種元素中電負性最大的是________(填元素符號
元素周期表中,與P緊鄰的4種元素中電負性最大的是________(填元素符號![]() 。Si、P、S三種元素的第一電離能由大到小的順序是________。
。Si、P、S三種元素的第一電離能由大到小的順序是________。
![]() 銨鹽大多不穩定,
銨鹽大多不穩定,![]() F、
F、![]() 中,較易分解的是________,原因是________。
中,較易分解的是________,原因是________。
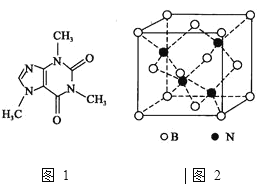
![]() 咖啡因對中樞神經有興奮作用,其結構簡式如圖1。常溫下,咖啡因在水中的溶解度為
咖啡因對中樞神經有興奮作用,其結構簡式如圖1。常溫下,咖啡因在水中的溶解度為![]() ,加適量水楊酸鈉
,加適量水楊酸鈉![]() 可使其溶解度增大,其原因可能是________,分子中氮原子的雜化類型有________。
可使其溶解度增大,其原因可能是________,分子中氮原子的雜化類型有________。
![]() 氮化硼、氮化鋁、氮化鎵的結構類似于金剛石,熔點如表中所示:
氮化硼、氮化鋁、氮化鎵的結構類似于金剛石,熔點如表中所示:
物質 | BN | AIN | GaN |
熔點 | 3000 | 2200 | 1700 |
![]() 試從結構的角度分析它們熔點不同的原因________。
試從結構的角度分析它們熔點不同的原因________。
![]() 的晶胞結構如圖2所示,晶體中一個B原子周圍距離最近的N原子有________個;若B、N的原子半徑分別為
的晶胞結構如圖2所示,晶體中一個B原子周圍距離最近的N原子有________個;若B、N的原子半徑分別為![]() 和
和![]() ,密度為
,密度為![]() ,阿伏加德羅常數值為
,阿伏加德羅常數值為![]() ,則BN晶胞中原子的體積占晶胞體積的百分率為________。
,則BN晶胞中原子的體積占晶胞體積的百分率為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學探究Cu與NO的反應,查閱資料:①Cu與NO反應可生成CuO和N2,②酸性條件下,NO或NO2–都能與MnO4–反應生成NO3–和Mn2+
(1)實驗室利用Cu和稀HNO3制備NO,寫出反應的化學方程式_____________。
(2)選用如圖所示裝置完成Cu與NO的實驗。(夾持裝置略) 實驗開始前,向裝置中通入一段時間的N2。回答下列問題:
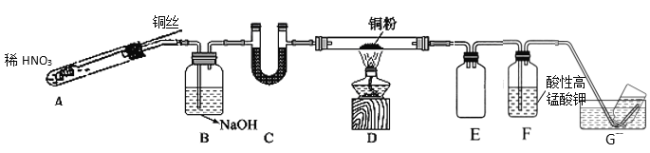
①使用銅絲的優點是_____________________裝置E的作用為_______________。
②裝置C中盛放的藥品可能是_________;
③裝置D中的現象是_______________;裝置F中反應的離子方程式是_______________。
(3)測定NaNO2和NaNO3 混合溶液中NaNO2的濃度。 取25.00mL混合溶液于錐形瓶中,用0.1000mol·L-1酸性KMnO4溶液進行滴定,實驗所得數據如下表所示:
滴定次數 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液體積/mL | 20.90 | 20.12 | 20.00 | 19.88 |
①第一次實驗數據出現異常,造成這種異常的原因可能是_________(填字母代號)。
a.錐形瓶洗凈后未干燥
b.酸式滴定管用蒸餾水洗凈后未用標準液潤洗
c.滴定終點時仰視讀數
d.酸性KMnO4溶液中含有其他氧化性試劑
e.錐形瓶洗凈后用待測液潤洗
②酸性KMnO4溶液滴定亞硝酸鈉溶液的離子方程式為___________________。
③NaNO2 的物質的量濃度為__________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在2 L密閉容器中,800℃時反應2NO(g)+O2(g)![]() 2NO2(g)體系中,n(NO)隨時間的變化如表:
2NO2(g)體系中,n(NO)隨時間的變化如表:
時間/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反應________(填“是”或“不是”)可逆反應。
(2)如圖所示,表示NO2變化曲線的是______。用O2表示從0~2s內該反應的平均速率v=________。

(3)能說明該反應已達到平衡狀態的是________(填序號)。
a.v(NO2)=2v(O2)
b.容器內壓強保持不變
c.v逆(NO)=2v正(O2)
d.容器內密度保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,向容積為2 L的密閉容器中充入一定量的氣體A和氣體B,發生反應: 2A(g)+B(g) ![]() 2C(g),反應過程中測定部分數據見下表(表中t1<t2),下列說法正確的是
2C(g),反應過程中測定部分數據見下表(表中t1<t2),下列說法正確的是
反應時間/min | n(A)/mol | n(B)/mol |
0 | 0.10 | 0.060 |
t1 | 0.012 | |
t2 | 0.016 |
A.在0~t1 min內的平均反應速率為v(C)=![]() molL-1min-1
molL-1min-1
B.其他條件不變,起始時向容器中充入0.10 mol C和0.010 mol B,平衡時n(A)=0.012 mol
C.保持其他條件不變,升高溫度,平衡時c(A)=0.0070 molL-1,則反應的ΔH<0
D.相同溫度下,起始時向容器中充入0.15mol A和0.090mol B,平衡時A轉化率小于88%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A(C2H2)是基本有機化工原料。由A制備聚乙烯醇縮丁醛和順式異戊二烯的合成路線(部分反應條件略去)如下所示:

回答下列問題:
(1)A的名稱是_______,B含有的官能團是_______________。
(2)①的反應類型是____________,⑦的反應類型是________________。
(3)C和D的結構簡式分別為______________、_________________。
(4)異戊二烯分子中最多有________個原子共平面,順式聚異戊二烯的結構簡式為___________。
(5)寫出與A具有相同官能團的異戊二烯的所有同分異構體__________(填結構簡式)。
(6)參照異戊二烯的上述合成路線,設計一條由A和乙醛為起始原料制備1,3-丁二烯的合成路線___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向絕熱恒容密閉容器中通入SO2和NO2,一定條件下使反應![]() 達到平衡,正反應速率隨時間變化的示意圖如下所示。
達到平衡,正反應速率隨時間變化的示意圖如下所示。
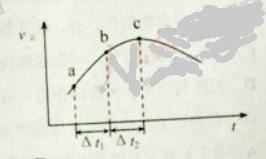
A. 反應在c 點達到平衡狀態
B. 反應物濃度:![]() 點小于
點小于![]() 點
點
C. 反應物的總能量低于生成物的總能量
D. ![]() 時,SO2的轉化率:
時,SO2的轉化率:![]() 段小于
段小于![]() 段
段
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com