
| A、以X濃度變化表示的反應速率為0.001mol/(L?S) | ||
B、將容器體積變為20L,Z的平衡濃度變為原來的
| ||
| C、若壓強增大1倍,則物質Y的轉化率增大1倍 | ||
| D、若升高溫度,X的濃度增大,則該反應的△H>0 |
| ||
| 60s |


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
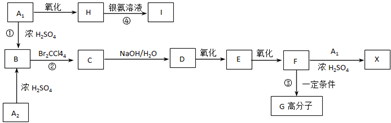
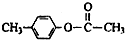 、
、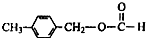 外,其余的結構簡式:
外,其余的結構簡式:查看答案和解析>>
科目:高中化學 來源: 題型:
 “潔凈煤技術”研究在世界上相當普遍,科研人員通過向地下煤層氣化爐中交替鼓入空氣和水蒸氣的方法,連續產出了熱值高達122500~16000kJ?m-3的煤炭氣,其主要成分是CO和H2.CO和H2可作為能源和化工原料,應用十分廣泛.
“潔凈煤技術”研究在世界上相當普遍,科研人員通過向地下煤層氣化爐中交替鼓入空氣和水蒸氣的方法,連續產出了熱值高達122500~16000kJ?m-3的煤炭氣,其主要成分是CO和H2.CO和H2可作為能源和化工原料,應用十分廣泛.查看答案和解析>>
科目:高中化學 來源: 題型:
| 一定條件 |
| A、2 min時,c(SO2)=0.6 mol?L-1 |
| B、用O2表示4 min內的反應速率為0.1 mol?(L?min)-1 |
| C、再向容器中充入1 mol SO3,達到新平衡,n(SO2):n(O2)=2:1 |
| D、4 min后,若升高溫度,平衡向逆方向移動,平衡常數K減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、向某無色溶液中加入BaCl2溶液產生不溶于稀HNO3的白色沉淀,說明原溶液中一定有SO42- |
| B、向某無色溶液中加入鹽酸,有無色無味的氣體產生,則說明原溶液中一定有CO32- |
| C、向某溶液中滴加KSCN溶液,溶液不變紅,再滴加氯水,變紅,說明原溶液一定有Fe2+ |
| D、將某溶液進行焰色反應時,火焰呈黃色,則溶液中一定無K+ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 催化劑 |
| △ |
| A、0.24 mol?L-1 |
| B、0.28 mol?L-1 |
| C、0.32 mol?L-1 |
| D、0.26 mol?L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:
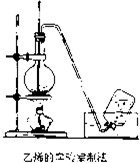 實驗室制取乙烯的裝置如圖所示,請根據圖示回答下列問題:
實驗室制取乙烯的裝置如圖所示,請根據圖示回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com