
【題目】利用鈦白粉廠廢酸(主要含硫酸、Fe3+、Fe2+、TiO2+、Al3+)制備過二硫酸銨[(NH4)2S2O8],同時回收TiO(OH)2的簡要流程如下: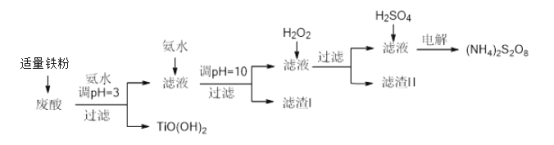
已知:i.部分離子完全生成氫氧化物沉淀的pH:
金屬離子 | TiO2+ | Fe3+ | Fe2+ | Al3+ |
開始沉淀的PH | 1.2 | 1.9 | 7.0 | 3.2 |
沉淀完全的pH | 2.8 | 3.1 | 9.4 | 4.7 |
ii.pH>7時,Fe2+部分生成Fe(II)氨絡離子[Fe(NH3)2]2+。
請回答下列問題:
(1)加入適量鐵的作用是______________________________________。
(2)生成TiO(OH)2的化學方程式是________________________________。
(3)濾渣I、濾渣Ⅱ中均含有的物質的化學式是___________________________。
(4)加入H2O2的目的是氧化除掉Fe(II)氨絡離子[Fe(NH3)2]2+,配平下列離子方程式:
2[Fe(NH3)2]2+ +____________+4H2O +H2O2 =___________ + 4NH3·H2O 。
(5)常溫下,電解液中含硫微粒主要存在形式與pH的關系如下圖所示。
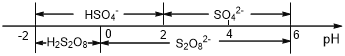
在陽極放電的離子主要為HSO4-,陽極區(qū)電解質溶液的pH范圍為___________________________________
(6)已知Ksp[Al(OH)3]=3.2×10-34 ,當pH=10 時,求溶液中c(Al3+)=______________
(7)25℃,pH=3的(NH4)2SO4溶液中,計算2c(SO42-)- c(NH4+) =_______mol/L(列式即可)。
【答案】將Fe3+ 還原到Fe2+,避免Fe3+ 和TiO2+ 同時沉淀 TiOSO4+2 NH3·H2O=(NH4)2SO4 +TiO(OH)2↓ Fe(OH)3 4OH- 2Fe(OH)3 0≤pH≤2 3.2×10-22 10-3-10-11
【解析】
加入適量Fe粉,將廢酸(主要含硫酸、Fe3+、Fe2+、TiO2+、Al3+)中的Fe3+轉化為Fe2+除去,得到含有Fe2+、TiO2+、Al3+的酸性溶液,加入氨水調節(jié)pH=3,使TiO2+轉化為TiO(OH)2沉淀以回收,過濾,濾液中含(NH4)2SO4、FeSO4和Al2(SO4)3溶液,再加氨水調節(jié)溶液pH=10,過濾除去氫氧化鋁(濾渣I),還有部分Fe(OH)2沉淀生成,少量的氫氧化亞鐵被氧氣氧化生成Fe(OH)3,得到(NH4)2SO4和[Fe(NH3)2]SO4溶液,加入H2O2氧化除去[Fe(NH3)2]SO4,反應為2[Fe(NH3)2]2++4OH-+4H2O+H2O2=2Fe(OH)3+4NH3·H2O,過濾除去Fe(OH)3(濾渣II),得到(NH4)2SO4溶液,H2SO4酸化后電解生成(NH4)2S2O8,以此解答該題。
(1)根據題給部分離子完全生成氫氧化物沉淀的pH,加入適量Fe,可將Fe3+還原為Fe2+,避免Fe3+和TiO2+同時沉淀;
(2)生成TiO(OH)2的化學方程式為TiOSO4+2NH3·H2O=TiO(OH)2↓+(NH4)2SO4;
(3)由以上分析可知濾渣Ⅰ、濾渣Ⅱ均含有的物質的化學式為Fe(OH)3;
(4)H2O2有強氧化性,能氧化生成[Fe(NH3)2]2+生成Fe(OH)3沉淀,反應的離子方程式為2[Fe(NH3)2]2++4OH-+4H2O+H2O2=2Fe(OH)3+4NH3·H2O;
(5)根據圖中電解液中含硫微粒主要存在形式與pH的關系,陽極放電的離子主要是HSO4-,則陽極區(qū)電解質溶液的pH范圍應控制在0≤pH≤2;
(6)已知Ksp[Al(OH)3]=3.2×10-34 ,當pH=10 時,c(OH-)=10-4mol/L,則溶液中c(Al3+)=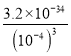 mol/L=3.2×10-22 mol/L;
mol/L=3.2×10-22 mol/L;
(7)25℃,pH=3的(NH4)2SO4溶液中,電荷守恒c(H+)+c(NH4+)=2c(SO42-)+c(OH-),則2c(SO42-)-c(NH4+)= c(H+)- c(OH-)=(10-3-10-11)mol/L。


科目:高中化學 來源: 題型:
【題目】下列離子方程式正確的是( )
A.向FeCl2溶液中通入Cl2:Fe2+Cl2═Fe3++2C1-
B.醋酸溶液與水垢中的CaCO3反應:CaCO3+2H+═Ca2++H2O+CO2
C.向小蘇打溶液中滴加鹽酸;CO32-+2H+═H2O+CO2
D.向NH4Cl溶液中滴入燒堿溶液并加熱:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.如圖所示的是探究金屬腐蝕條件的實驗裝置圖,請分析實驗并回答下列問題:

(1)若起始時甲、乙、丙3套裝置的導管中液面高度相同,過一段時間后液面最高的是________。
(2)通過甲、乙裝置的對比說明鋼鐵中碳的含量越________(填“高”或“低”),鋼鐵越易腐蝕。
(3)乙裝置中發(fā)生電化學腐蝕時正極的電極反應式為_________________________________。
Ⅱ.利用化學反應:2FeCl3+Cu=2FeCl2+CuCl2,請你選擇合適的電極材料和電解質溶液,設計一個原電池。可供選擇的電極材料:鐵棒、銅棒、石墨棒。可供選擇的電解質溶液:CuCl2溶液、FeCl2溶液、FeCl3溶液。
請?zhí)顚懴铝锌瞻祝?/span>
(1)選擇________作正極材料,________作負極材料;選擇________作電解質溶液。
(2)寫出有關的電極反應式:正極:__________________;負極:_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】M表示摩爾質量,NA表示阿伏加德羅常數,Vm表示氣體摩爾體積,ω表示溶質的質量分數,ρ(單位為gcm-3)表示溶液的密度。下列說法中不正確的是( )
A.根據摩爾質量和阿伏加德羅常數可以計算得出某氣體分子的質量:![]()
B.根據氣體摩爾體積和阿伏加德羅常數可以計算得出該條件下某氣體分子的大小:![]()
C.根據摩爾質量和氣體摩爾體積可以計算得出該條件下某氣體的密度:![]()
D.根據溶質的質量分數、摩爾質量和溶液的密度可以計算出某溶液的物質的量濃度:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于原子序數的說法正確的是
A. 原子序數是按照元素在周期表中的順序給元素所編的號碼
B. 元素的原子序數一定等于其原子相對質量
C. 元素的原子序數一定等于其最外層電子數
D. 元素的原子序數一定等于其核內中子數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:①A的產量通常用來衡量一個國家的石油化工水平;②2CH3CHO+O2![]() 2CH3COOH。現以A為主要原料合成化合物E,其合成路線如圖1所示。回答下列問題:
2CH3COOH。現以A為主要原料合成化合物E,其合成路線如圖1所示。回答下列問題:

(1)寫出下列物質的官能團名稱:B:____________________;D:____________________。
(2)反應④的化學方程式為________________________________________________,反應類型:________。
(3)某學習小組設計物質B催化氧化的實驗裝置如下,根據圖2裝置回答問題。

①裝置甲錐形瓶中盛放的固體藥品可能為________(填字母)。
A.Na2O2 B.KClC.Na2CO3 D.MnO2
②實驗過程中,丙裝置硬質玻璃管中發(fā)生反應的化學方程式為_______________________________。
③物質B的催化氧化產物與葡萄糖具有相同的特征反應,將所得的氧化產物滴加到新制氫氧化銅懸濁液中加熱,現象為______________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用“化學計量在實驗中的應用”的相關知識進行填空。
(1)要使NH3與CH4含相同數目的H原子,則NH3和CH4的物質的量之比為______。
(2)在一定的溫度和壓強下,1體積 X2(g)跟3體積Y2(g)化合生成2體積化合物,則該化合物的化學式是________。
(3)將50 mL 0.1 mol·L![]() 的NaCl和100 mL 0.05 mol·L
的NaCl和100 mL 0.05 mol·L![]() CaCl2溶液混合后,若溶液的體積為二者體積之和,則混合溶液中c(Cl-)為________。
CaCl2溶液混合后,若溶液的體積為二者體積之和,則混合溶液中c(Cl-)為________。
(4)三種正鹽的混合溶液中含有0.2 mol Na+、0.25 mol Mg2+、0.4 mol Cl-、SO42-,則n(SO42-)為_________。
(5)有等體積的NaCl、CaCl2、AlCl3三種溶液,分別與足量的AgNO3溶液反應,若生成沉淀的質量相等,則三種溶液中所含溶質的物質的量濃度之比為_____________。
(6)標準狀況下,NH3與CH4組成的混合氣體的密度為0.75g/L,該混合氣體的平均摩爾質量為_____________,NH3的體積分數為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.質子數相同而中子數不同的同一種元素的不同原子互為同素異形體
B.鐵是人體必需微量元素中含量最多的一種
C.在水溶液中能導電的物質一般是電解質,如HCl、H2O 、NH3、CH3COOH、NaOH、AgCl都是電解質
D.元素周期表中每一個縱列為一個族
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A元素的一種單質是重要的半導體材料,含A元素的一種化合物C可用于制造高性能的現代通訊材料—光導纖維,C與燒堿反應生成含A元素的化合物D。
(1)易與C發(fā)生化學反應的酸是________,反應的化學方程式是_______________ 。
(2)將C與純堿混合,在高溫熔融時發(fā)生化學反應也可生成D,同時還生成B的最高價氧化物E;將E與D在足量的水中混合后,又發(fā)生化學反應生成含A的化合物F。
①寫出生成D和F的化學反應方程式:____________________、__________________。
②要將純堿在高溫下熔化,下列坩堝中不可選用的是________。
A.普通玻璃坩堝 B.石英玻璃坩堝 C.瓷坩堝 D.鐵坩堝
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com