
 工業上可利用CO或CO2來生產燃料甲醇.已知甲醇制備的有關化學反應以及在不同溫度下的化學反應平衡常數如下所示:
工業上可利用CO或CO2來生產燃料甲醇.已知甲醇制備的有關化學反應以及在不同溫度下的化學反應平衡常數如下所示:| 化學反應 | 平衡 常數 | 溫度/℃ | ||
| 500 | 700 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.34 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 1.70 | 2.52 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | |||
分析 (1)依據反應②的平衡常數隨溫度變化判斷反應能量變化;
(2)平衡常數是利用生成物平衡濃度冪次方乘積除以反應物平衡濃度冪次方乘積,結合反應①+②得到反應③,可得平衡常數K3=K1×K2;
(3)計算濃度商和平衡常數比較分析判斷反應進行方向;
(4)依據影響化學反應速率的因素和影響平衡移動的因素及根據平均摩爾質量=$\frac{總質量}{總物質的量}$進行判斷.
解答 解:(1)反應②CO2(g)+H2(g)?CO(g)+H2O(g)的平衡常數隨溫度升高增大,說明平衡正向進行,正反應是吸熱反應;
故答案為:吸熱;
(2)平衡常數是利用生成物平衡濃度冪次方乘積除以反應物平衡濃度冪次方乘積,結合反應①+②得到反應③,可得平衡常數K3=K1•K2;
故答案為:K1•K2;
(3)500℃時,測得反應③在某時刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的濃度分別為0.1mol•L-1、0.8mol•L-1、0.3mol•L-1、0.15mol•L-1,Q=$\frac{0.3×0.15}{0.{8}^{3}×0.1}$=0.88<K=2.5,則此時v正>v逆;
故答案為:>;
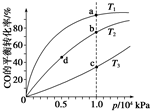
(4)A.根據反應①中溫度與K的關系,可推斷該反應為放熱反應,升溫,平衡左移,CO的轉化率減小,所以T3>T2>T1,A錯誤;
B.反應速率v(c)>v(a),v(b)>v(d),B錯誤;
C.溫度越高,平衡常數越小,壓強對平衡常數無影響,所以K(a)>K(c),K(b)=K(d),C正確;
D.升溫,平衡左移,平均摩爾質量減小,加壓,平衡右移,平均摩爾質量增大,所以M(a)>M(c),M(b)>M(d),D正確,
故選CD.
點評 本題考查了化學平衡、反應速率影響因素分析判斷,平衡常數計算應用,掌握反應特征和平衡移動原理是關鍵,題目難度中等.


 培優三好生系列答案
培優三好生系列答案 優化作業上海科技文獻出版社系列答案
優化作業上海科技文獻出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | 它們單質的熔、沸點隨核電荷數的增加逐漸降低 | |
| B. | 元素的非金屬性隨核電荷數的增加逐漸減小 | |
| C. | 它們原子的氧化性隨核電荷數的增加逐漸增強 | |
| D. | 它們氫化物的穩定性隨核電荷數的增加逐漸增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應物濃度減小,反應速率減小 | |
| B. | 反應物濃度增加,反應速率增加 | |
| C. | 溫度升高,反應速率增加 | |
| D. | 熱水對反應起催化作用,從而加快了反應速率 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 類比對象 | 結論 | |
| A | Cl2+H2O$\frac{\underline{\;\;△\;\;}}{\;}$HCl+HClO | I2+H2O$\frac{\underline{\;\;△\;\;}}{\;}$HI+HIO |
| B | C+2CuO$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+CO2↑ | C+SiO2$\frac{\underline{\;高溫\;}}{\;}$Si+CO2↑ |
| C | Na2O+H2O=2NaOH | CuO+H2O=Cu(OH)2 |
| D | Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO | Ca(ClO)2+SO2+H2O=CaSO3↓+2HClO |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃硫酸具有脫水性 | B. | 濃硫酸具有吸水性 | ||
| C. | 鹽酸具有揮發性 | D. | 氣體的溶解度的隨溫度升高而降低 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 它能使酚酞試液變紅色 | |
| B. | 氨水極易揮發出氨 | |
| C. | 氨與水結合生成的一水合氨(NH3•H2O)只有小部分電離成NH4+和OH- | |
| D. | 溶于水的氨大部分以NH3分子形式存在 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 該化合物僅含碳、氫兩種元素 | B. | 該化合物中碳、氫原子個數比為1:4 | ||
| C. | 無法確定該化合物是否含有氧元素 | D. | 此有機物的最簡式為CH4O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 圖1所示裝置用于Cu和濃H2SO4反應制取少量的SO2氣體 | |
| B. | 圖2所示裝置用于除去碳酸氫鈉固體中的少量碳酸鈉 | |
| C. | 圖3所示裝置配制100mL0.1mol•L-1的硫酸 | |
| D. | 圖4所示裝置用于分離出溴苯 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com