
| A. | 當△H為“-”時,表示該反應為吸熱反應 | |
| B. | 化學反應的反應熱只與反應體系的始態和終態有關,而與反應的途徑無關 | |
| C. | 反應熱的大小與反應物所具有的能量和生成物所具有的能量無關 | |
| D. | 已知:C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5 kJ/mol,碳的燃燒熱為110.5 kJ/mol |
分析 A.△H為“-”時,為放熱反應;
B.焓變與始態和終態有關,與反應的途徑無關;
C.反應能量變化與反應物、生成物的總能量相對大小有關;
D.CO不是穩定氧化物.
解答 解:A.△H為“-”時,為放熱反應,△H為“+”時,表示該反應為吸熱反應,故A錯誤;
B.焓變與始態和終態有關,與反應的途徑無關,反應體系的始態和終態決定反應的能量變化,故B正確;
C.反應熱的大小與反應物所具有的能量和生成物所具有的能量有關,故C錯誤;
D.CO不是穩定氧化物,生成二氧化碳時的能量變化可確定燃燒熱,故D錯誤;
故選B.
點評 本題考查反應熱與焓變,為高頻考點,把握焓變與反應物、生成物的能量關系為解答的關鍵,側重分析與應用能力的考查,注意燃燒熱的判斷,題目難度不大.


科目:高中化學 來源: 題型:實驗題
| 可能影響因素 | 實驗操作 | 預期現象和結論 |
| ①溶液的酸性 | 取少量0.5mol•L-1Fe(NO3)3于試管中,加入幾滴3.0mol•L-1HNO3. | 現象:棕黃色溶液顏色變淺; 結論:酸性增強抑制Fe3+水解. |
| ②溶液的濃度 | 取10mL0.5mol•L-1 Fe(NO3)3于燒杯中,用pH計測得pH1.另取90mL蒸餾水加入燒杯,充分攪拌,再測得pH2. | 現象:pH2-pH1<1(或正確表達) 結論:稀釋促進水解(或平衡右移) |
| ③溶液的溫度 | 取少量0.5mol•L-1Fe(NO3)3于試管中,用酒精燈加熱一段時間,觀察溶液顏色 | 現象:加熱后溶液顏色變深 結論:升高溫度促進Fe3+水解 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 已知:P4(白磷,s)═4P(紅磷,s)△H<0,則白磷比紅磷穩定 | |
| B. | 由CH3CH2CH2CH3(g)+$\frac{13}{2}$O2(g)═4CO2(g)+5H2O(g)△H=-2658 kJ•mol-1可知正丁烷的標準燃燒熱為2658 kJ•mol-1 | |
| C. | OH-(aq)+H+(aq)═H2O(l)△H=-57.3 kJ•mol-1,故1 mol醋酸與1 mol NaOH完全反應,放出的熱量為57.3 kJ•mol-1 | |
| D. | 已知:2CO(g)+O2(g)═2CO2(g)△H=-566 kJ•mol-1 N2(g)+O2(g)═2NO(g)△H=+180 kJ•mol-1 則2CO(g)+2NO(g)═N2(g)+2CO2(g)△H=-746 kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 從反應開始到達到平衡,所需時間tM>tN | |
| B. | 平衡時cM(I2)=c N(I2) | |
| C. | 平衡時I2 蒸氣在混合氣體中的體積分數:M>N | |
| D. | HI的平衡分解率αM=αN |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
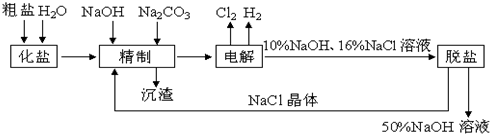
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | -183 kJ•mol-1 | B. | +183 kJ•mol-1 | C. | -862 kJ•mol-1 | D. | +862 kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分解反應均為吸熱反應 | |
| B. | lmol 酸與lmol 堿恰好中和時所放出的熱量叫中和熱 | |
| C. | 若S ( s )+O2 (g)=SO2(g)△H1,S(g)+O2(g)=SO2(g)△H2;△H1>△H2 | |
| D. | 已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ/mol,則氫氣的燃燒熱為241.8 kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4 L水中含有的水分子數為NA | |
| B. | 常溫常壓下,46 g NO2和N2O4的混合氣體中含有的氧原子數為2NA | |
| C. | 1mol/L的Ba(NO3)2溶液中含NO3-離子數為2NA | |
| D. | 分子數為NA的CO和N2的混合氣體的體積約為22.4 L,質量為28 g |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com