
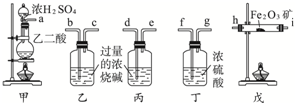
分析 做實驗題首先明確實驗目的,本題不僅要求模擬煉鐵原理的過程,還要檢測氧化鐵的純度.同時,作為還原劑的CO需純凈、干燥,所以首先要用氫氧化鈉溶液除雜,再用濃硫酸干燥,然后再利用氫氧化鈉溶液吸收煉鐵反應以后生成的CO2,通過稱量吸收CO2前后的溶液質量,計算氧化鐵的純度,
(1)根據要得到純凈干燥的一氧化碳,首先要通過澄清石灰水除去一氧化碳中的二氧化碳,然后通過濃硫酸除去一氧化碳中的水分進行解答.
(2)根據裝置乙和丙中都盛有氫氧化鈉溶液,但乙和丙裝置的不同,乙裝置是用來除去一氧化碳中二氧化碳的,丙裝置是用來檢驗并吸收二氧化碳的進行解答;
(3)根據防止生成的鐵被氧氣氧化,所以實驗結束時,先熄滅戊處酒精燈,還必須從甲處排出一些混合氣體直至試管冷卻進行解答;
解答 解:(1)要得到純凈干燥的一氧化碳,首先要通過氫氧化鈉溶液除去一氧化碳中的二氧化碳,然后通過濃硫酸除去一氧化碳中的水分,通過氧化鐵反應后通過氫氧化鈉溶液吸收剩余二氧化碳氣體,因此裝置連接順序應是a b c f g h i d
故答案為:a b c f g h i d;
(2)裝置乙和丙中都盛有氫氧化鈉溶液,但乙和丙裝置的不同點在于乙裝置是用來除去一氧化碳中二氧化碳的,丙裝置是用來檢驗并吸收二氧化碳的,故填除去CO中的CO2雜質 吸收反應以后生成的CO2,
故答案為:除去CO中的CO2雜質 吸收反應以后生成的CO2;
(3)防止生成的鐵被氧氣氧化,所以實驗結束時,先熄滅戊處酒精燈,還必須從甲處排出一些混合氣體直至試管冷卻,防止生成的鐵被氧氣氧化;
故答案為:作保護氣,并確保生成的CO2完全被氫氧化鈉溶液吸收.
點評 本題是一道綜合實驗題,關健是搞清實驗原理及每一裝置及試劑的作用,連接好實驗裝置,氣體除雜和干燥、氣體性質升溫掌握是解題關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 處理廢棄物 | B. | 治理污染點 | C. | 減少有毒物排放 | D. | 杜絕污染源 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 第一次剩余4.8 g金屬為銅和鐵 | |
| B. | 稀硝酸的物質的量濃度為1.0 mol•L-1 | |
| C. | 原混合物中銅和鐵各0.075 mol | |
| D. | 再加入上述100 mL稀硝酸,又得到標準狀況下1.12 L NO |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
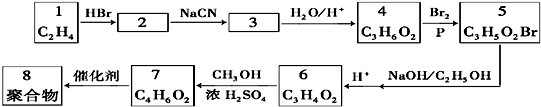

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二元弱酸酸式鹽NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) | |
| B. | 一定量的(NH4)2SO4與NH3•H2O混合的酸性溶液中:c(NH4+)>2c(SO42-) | |
| C. | 物質的量濃度均為0.01mol/L的CH3COOH和CH3COONa的溶液等體積混合后溶液中 c(CH3COOH)+c(CH3COO-)=0.02 mol/L | |
| D. | 物質的量濃度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中c(NH4+):①>③>② |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 16 g CH4與18 g NH4+所含的質子數均為10NA | |
| B. | 將15.6 g Na2O2投入到足量水中,反應后溶液中的氧原子數為0.4NA | |
| C. | 在1 L 0.1 mol•L-1的碳酸鈉溶液中,陰離子總數一定大于0.1NA | |
| D. | 2 mol NO和1 mol O2混合,所得氣體的分子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 室溫下,將1.000mol•L-1鹽酸滴入20.00mL 1.000mol•L-1氨水中,溶液pH和溫度隨加入鹽酸體積變化曲線如圖所示.下列有關說法不正確的是( )
室溫下,將1.000mol•L-1鹽酸滴入20.00mL 1.000mol•L-1氨水中,溶液pH和溫度隨加入鹽酸體積變化曲線如圖所示.下列有關說法不正確的是( )| A. | a點水的離子積Kw=1.0×10-14 | |
| B. | b點:c(NH4+)+c(H+)=c(Cl-)+c(OH-) | |
| C. | c點:c(Cl-)=c(NH4+) | |
| D. | d點后,溶液溫度略下降的主要原因是NH3•H2O電離吸熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| Y | Z | ||
| X | W |
| A. | 原子半徑:X<Y<Z | |
| B. | 最高價氧化物的水化物的酸性:Y<W | |
| C. | 原子序數:X>W>Z>Y | |
| D. | Z、Y的單質均可與H2反應,且反應的劇烈程度:Y>Z |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com