
【題目】I.25℃時,往25ml氫氧化鈉標準溶液中逐滴加入0.2 mol·L-1的一元酸HA溶液,pH變化曲線如下圖所示:

(1)該氫氧化鈉溶液的物質的量濃度為________mol·L-1。
(2)A點對應酸的體積為12.5ml,則所得混合溶液中由水電離出的c(OH-)=_______ mol·L-1。
(3)HA是________酸(選填“強”、“弱”)。NaA的水溶液顯________性(選填“酸”、“堿”),原因是:________(用離子方程式表示)。
(4)在B點所得混合溶液中,c(Na+) 、c(A-)、c(H+)、c(OH-)由大到小的順序是_________。
(5)在C點所得混合溶液中,下列說正確的是:___________。
A.HA的電離程度小于NaA的水解程度
B.離子濃度由大到小的順序是c(Na+) >c(A-)>c(H+)> c(OH-)。
C.c(Na+) +c(H+)=c(A─) +c(OH-)
D.c(HA)+c(A-)=0.2mol·L-1
Ⅱ.在25 ℃的條件下,某些弱酸的電離平衡常數。
化學式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ka1=5.9×10-2 Ka2=6.4×10-5 |
(1)溫度、濃度相同的CH3COOH和HClO溶液,水的電離程度前者________ 后者(填“>”“=”或“<”)。
(2)相同溫度下,pH相同的NaClO和CH3COOK兩種溶液中,c(CH3COOK)________c(NaClO) (填“>”“=”或“<”),[c(Na+)-c(ClO-)]_______[c(K+)-c(CH3COO-)](填“>”“=”或“<”)。
(3)在25 ℃的條件下,向0.1 mol·L-1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此時溶液pH=________。
【答案】 0.1 1×10-4 弱 堿 A-+H2O![]() HA+OH- c(Na+) =c(A-)>c(H+)=c(OH-) C < > = 5
HA+OH- c(Na+) =c(A-)>c(H+)=c(OH-) C < > = 5
【解析】試題分析:I.(1)根據起點溶液的PH=13計算氫氧化鈉溶液的物質的量濃度;(2)25ml 0.1 mol·L-1氫氧化鈉溶液中逐滴加入12.5ml 0.2 mol·L-1的一元酸HA溶液,恰好反應生成NaA,A點溶液的PH=10,說明NaA水解促進水電離;(3)根據圖像,氫氧化鈉溶液與一元酸HA溶液恰好完全反應時,溶液PH=10,說明NaA是強堿弱酸鹽,A-水解。(4)根據電荷守恒、溶液呈中性判斷B點所得混合溶液中,c(Na+) 、c(A-)、c(H+)、c(OH-)的大小順序;(5)25ml 0.1 mol·L-1氫氧化鈉溶液中逐滴加入25ml 0.2 mol·L-1的一元酸HA溶液,所得混合溶液中含有等濃度的NaA、HA;Ⅱ.(1)根據弱酸的弱酸的電離平衡常數,醋酸的酸性大于次氯酸,溫度、濃度相同的CH3COOH和HClO溶液,醋酸電離出氫離子濃度大于次氯酸,醋酸對水的電離抑制作用強;(2)醋酸的酸性大于次氯酸, NaClO比 CH3COOK更易水解;根據電荷守恒[c(Na+)-c(ClO-)]= c(OH-) -c(H+)、[c(K+)-c(CH3COO-)] = c(OH-) -c(H+);(3)在25 ℃,醋酸Ka=1.8×10-5, 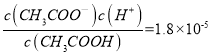 ,帶入c(CH3COOH)∶c(CH3COO-)=5∶9,得c(H+)=10-5。
,帶入c(CH3COOH)∶c(CH3COO-)=5∶9,得c(H+)=10-5。
解析:I.(1)25℃時,起點溶液的PH=13, ![]() ,
, ![]() ,所以氫氧化鈉溶液的物質的量濃度為0.1 mol·L-1;(2)25ml 0.1 mol·L-1氫氧化鈉溶液中逐滴加入12.5ml 0.2 mol·L-1的一元酸HA溶液,恰好反應生成NaA,A點溶液的PH=10,溶液中
,所以氫氧化鈉溶液的物質的量濃度為0.1 mol·L-1;(2)25ml 0.1 mol·L-1氫氧化鈉溶液中逐滴加入12.5ml 0.2 mol·L-1的一元酸HA溶液,恰好反應生成NaA,A點溶液的PH=10,溶液中![]() ,
, ![]() , NaA水解促進水電離,由水電離出的
, NaA水解促進水電離,由水電離出的![]() ;(3)根據圖像,氫氧化鈉溶液與一元酸HA溶液恰好完全反應時,溶液PH=10,說明NaA是強堿弱酸鹽,HA是弱酸,NaA的水溶液顯堿性,A-水解的方程式是A-+H2O
;(3)根據圖像,氫氧化鈉溶液與一元酸HA溶液恰好完全反應時,溶液PH=10,說明NaA是強堿弱酸鹽,HA是弱酸,NaA的水溶液顯堿性,A-水解的方程式是A-+H2O![]() HA+OH-;(4)根據電荷守恒c(Na+)+c(H+)=c(A-)+c(OH-),B點溶液呈中性c(H+)=c(OH-),所以B點所得混合溶液中,離子的大小順序是c(Na+) =c(A-)>c(H+)=c(OH-);(5)25ml 0.1 mol·L-1氫氧化鈉溶液中逐滴加入25ml 0.2 mol·L-1的一元酸HA溶液,所得混合溶液中含有等濃度的NaA、HA;C點溶液呈酸性,NaA水解程度小于HA,故A錯誤;C點溶液呈酸性,NaA水解程度小于HA,C點溶液離子濃度由大到小的順序是c(A-)>c(Na+) >c(H+)> c(OH-),故B錯誤;根據電荷守恒c(Na+) +c(H+)=c(A─) +c(OH-),故C正確;根據物料守恒c(HA)+c(A-)=0.1mol·L-1,故D錯誤。Ⅱ.(1)溫度、濃度相同的CH3COOH和HClO溶液,醋酸電離出氫離子濃度大于次氯酸,醋酸對水的電離抑制作用強,水電離的氫離子CH3COOH<HClO;(2)醋酸的酸性大于次氯酸, NaClO比 CH3COOK更易水解,所以相同溫度下,pH相同的NaClO和CH3COOK兩種溶液中,c(CH3COOK)>c(NaClO);根據電荷守恒[c(Na+)-c(ClO-)]= c(OH-) -c(H+)、[c(K+)-c(CH3COO-)] = c(OH-) -c(H+),溶液PH相同,所以[c(Na+)-c(ClO-)]=[c(K+)-c(CH3COO-)];在25 ℃,醋酸Ka=1.8×10-5,
HA+OH-;(4)根據電荷守恒c(Na+)+c(H+)=c(A-)+c(OH-),B點溶液呈中性c(H+)=c(OH-),所以B點所得混合溶液中,離子的大小順序是c(Na+) =c(A-)>c(H+)=c(OH-);(5)25ml 0.1 mol·L-1氫氧化鈉溶液中逐滴加入25ml 0.2 mol·L-1的一元酸HA溶液,所得混合溶液中含有等濃度的NaA、HA;C點溶液呈酸性,NaA水解程度小于HA,故A錯誤;C點溶液呈酸性,NaA水解程度小于HA,C點溶液離子濃度由大到小的順序是c(A-)>c(Na+) >c(H+)> c(OH-),故B錯誤;根據電荷守恒c(Na+) +c(H+)=c(A─) +c(OH-),故C正確;根據物料守恒c(HA)+c(A-)=0.1mol·L-1,故D錯誤。Ⅱ.(1)溫度、濃度相同的CH3COOH和HClO溶液,醋酸電離出氫離子濃度大于次氯酸,醋酸對水的電離抑制作用強,水電離的氫離子CH3COOH<HClO;(2)醋酸的酸性大于次氯酸, NaClO比 CH3COOK更易水解,所以相同溫度下,pH相同的NaClO和CH3COOK兩種溶液中,c(CH3COOK)>c(NaClO);根據電荷守恒[c(Na+)-c(ClO-)]= c(OH-) -c(H+)、[c(K+)-c(CH3COO-)] = c(OH-) -c(H+),溶液PH相同,所以[c(Na+)-c(ClO-)]=[c(K+)-c(CH3COO-)];在25 ℃,醋酸Ka=1.8×10-5, 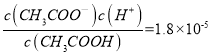 ,帶入c(CH3COOH)∶c(CH3COO-)=5∶9,得c(H+)=10-5,所以PH=5。
,帶入c(CH3COOH)∶c(CH3COO-)=5∶9,得c(H+)=10-5,所以PH=5。


科目:高中化學 來源: 題型:
【題目】實驗室里要配制400mL0.2mol/L的硫酸鈉溶液。實驗步驟如下:
A.在天平上稱出_______g硫酸鈉固體,把它放在燒杯里,用適量的蒸餾水溶解。
B.把得到的溶液冷卻后小心地沿著__________注入_______________ 中。
C.用少量蒸餾水洗滌燒杯和玻璃棒2~3次,每次洗滌液也小心轉入容量瓶中。
D.繼續向容量瓶中加蒸餾水至液面距刻度l~2cm處,改用________小心滴加蒸餾水至溶液凹液面底部與刻度線水平相切。
E.將瓶塞塞緊,充分搖勻。
F.將配好的溶液倒入試劑瓶中,貼上標簽,并洗滌容量瓶。
(1) 請填寫上述空白處。
(2) 下列情況會使所配溶液濃度偏低的是___________(填序號)。

a.某同學定容時觀察液面的情況如圖所示
b.沒有進行上述的操作步驟C
c.搖勻后發現液面低于刻度線
d.B操作時將少量液體灑到外面
e.容量瓶用前內壁沾有水珠
(3) 如果實驗室用18mol/L的濃硫酸配制3. 6mol·L-1的稀硫酸250mL。計算所需濃硫酸的體積為___________mL,在實驗時應用_________量取濃硫酸。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗是化學研究的基礎。下列關于各實驗裝置的敘述正確的是( )

A. 裝置①常用于分離互不相溶的液體混合物
B. 裝置②可用于吸收NH3或HCl氣體,并防止倒吸
C. 裝置④可用于干燥、收集氯化氫,并吸收多余的氯化氫
D. 裝置③可用于收集H2、CO2、Cl2、NH3等氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用含少量銀和鋅的粗銅做陽極,純銅片做陰極,CuSO4溶液做電解液,電解一段時間后,陽極質量減少了x g,則( )
A. 電解液質量增加x g B. 陰極質量增加x g
C. 陰極質量增加a g,a>x D. 陰極質量增加b g,b<x
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組同學設計如圖裝置:


回答下列問題:
(1)乙中銅片為________極 (填“正”或“負”),其電極反應式為________。
(2)一段時間后,將甲和乙兩池溶液混合,加入H2O2和一定量稀硫酸后,有Fe(OH)3沉淀出現,但沒有Cu(OH)2沉淀出現,此時溶液中c(Fe3+)=2.6×10-18 mol·L-1,求溶液中Cu2+的最大物質的量濃度________。(寫出計算步驟)(已知2Fe2++H2O2+2H+=2Fe3++2H2O,Ksp[Fe(OH)3]=2.6×10-39,Ksp[Cu(OH)2]=2.2×10-20)。
(3)丙中電源的A極為________極(填“正”或“負”)。
(4)若丙池盛放足量的CuSO4溶液:
①在丙池鐵棒這極的現象是________。
②在丙池中陽極的電極反應是________。
(5)若丙池中盛放滴加少量酚酞的足量的飽和NaCl溶液1L(假設溶液體積電解前后無變化)。
①丙池通電一段時間后,________極附近溶液呈紅色(填Fe或C),總反應的離子方程式:________。
②25℃時,當丙池中有0.1mol電子發生轉移時切斷電源,則理論上標準狀況下共有________ L氣體生成。此時溶液的pH為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,通過下列反應可實現燃煤煙氣中硫的回收:SO2(g)+2CO(g)![]() 2CO2(g)+S(l) ΔH<0,若反應在恒容的密閉容器中進行,下列有關說法正確的是( )
2CO2(g)+S(l) ΔH<0,若反應在恒容的密閉容器中進行,下列有關說法正確的是( )
A. 平衡前,隨著反應的進行,容器內壓強始終不變
B. 平衡時,其他條件不變,分離出硫,正反應速率加快
C. 平衡時,其他條件不變,升高溫度可提高SO2的轉化率
D. 其他條件不變,使用不同催化劑,該反應的平衡常數不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組制取氯氣并進行氯氣的性質實驗,其裝置如圖所示,回答下列問題:
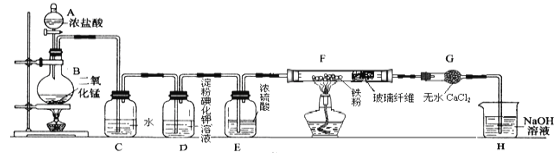
(1)儀器A的名稱是 ______,實驗中制備氯氣的反應方程式為 ____________________。
(2)C中發生反應的化學方程式為 ______ .若將干燥的有色布條放入C中,觀察到的現象是 ______,原因是 ___________________________。
(3)實驗中觀察到D溶液變藍色,查資料得知淀粉碘化鉀溶液是淀粉和碘化鉀(KI)的混合溶液,寫出D裝置中發生反應的離子方程式______________________。
(4)F中氯氣與鐵粉反應制備無水三氯化鐵,查資料知該化合物呈棕紅色、易吸水潮解, 100℃左右時升華.雙通管F中玻璃纖維(不參與反應)的作用是 ______ ;在F和H裝置之間安裝G裝置的目的是____。
(5)H中NaOH溶液的作用是 _______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某校課外活動小組為了探究銅與稀硝酸反應產生的是NO氣體,設計了如下實驗。實驗裝置如圖所示(已知NO、NO2能與NaOH溶液反應):

(1)設計裝置A的目的是________________________________________,為達此目的應進行的操作____________________________________________________________________________;A中反應的化學方程式是_________________________________________________________。
(2)在(1)中的操作后將裝置B中銅絲插入稀硝酸,并微熱之,觀察到裝置B中的現象是_______;B中反應的離子方程式是_________________________________________________________。
(3)裝置E和F的作用是__________________________________________________________,為實現此目的,操作方法是_______________________________________________________。
(4)D裝置的作用是_______________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應“P4(s)+3NaOH(aq)+3H2O(l)=3NaH2PO2(aq)+PH3(g) ΔH>0”制得的NaH2PO2可用于化學鍍鎳。下列說法正確的是

A. P4分子中P原子均滿足8電子穩定結構
B. 反應中NaOH作還原劑
C. 該反應能自發進行,則ΔS<0
D. 反應中生成1 mol NaH2PO2,轉移電子數目為3×6.02×1023
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com