
|
反應CO(g)+H2O(g)
此時反應中正、逆反應速率的關系式是 | |
| [ ] | |
A. |
v (正)>v(逆) |
B. |
v (正)<v(逆) |
C. |
v (正)=v(逆) |
D. |
無法判斷 |
科目:高中化學 來源: 題型:
CO和H2可作為能源和化工原料,應用十分廣泛。
(1)已知:C(s)+O2 (g) ===CO2(g) △H1= —393.5kJ·mol-1
2H2(g)+O2(g)=== 2H2O(g) △H2= —483.6kJ·mol-1
C(s)+H2O(g)=== CO(g)+H2(g) △H3= +131.3kJ·mol-1
則反應CO(g)+H2(g) +O2(g)=== H2O(g)+CO2(g)的△H= kJ·mol-1 。
標準狀況下的煤炭氣(CO、H2)33.6L與氧氣反應生成CO2和H2O,反應過程中轉移______mol電子。
(2)熔融碳酸鹽燃料電池(MCFS),是用煤氣(CO+H2)作負極燃氣,空氣與CO2的混合氣為正極助燃氣,用一定比例的Li2CO3和Na2CO3低熔點混合物做電解質,以金屬鎳(燃料極)為催化劑制成的。負極的電極反應式為 ;
則該電池的正極反應式是 。
(3)密閉容器中充有10 mol CO與20mol H2,在催化劑作用下反應生成甲醇:CO(g)+2H2(g)CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如下圖所示。
①若A、B兩點表示在某時刻達到的平衡狀態,此時在A點時容器的體積為10L,則該溫度下的平衡常數K= ;此時在B點時容器的體積VB 10L(填“大于”、“小于”或“等于”)。
②若A、C兩點都表示達到的平衡狀態,則自反應開始到達平衡狀態所需的時間tA tC(填“大于”、“小于”或“等于”)。
③在不改變反應物用量情況下,為提高CO轉化率可采取的措施是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
(14分)CO和H2可作為能源和化工原料,應用十分廣泛。
(1)已知:C(s)+O2 (g) ===CO2(g)△H1=﹣393.5kJ·mol-1
2H2(g)+O2(g)=== 2H2O(g)△H2=﹣483.6kJ·mol-1
C(s)+H2O(g)=== CO(g)+H2(g) △H3=+131.3kJ·mol-1
則反應CO(g)+H2(g) +O2(g)=== H2O(g)+CO2(g)的△H= kJ·mol-1。標準狀況下的煤炭氣(CO、H2)33.6L與氧氣反應生成CO2和H2O,反應過程中轉移 mol電子。
(2)熔融碳酸鹽燃料電池(MCFS),是用煤氣(CO+H2)作負極燃氣,空氣與CO2的混合氣為正極助燃氣,用一定比例的Li2CO3和Na2CO3低熔點混合物做電解質,以金屬鎳(燃料極)為催化劑制成的。負極的電極反應式為:CO+H2-4e-+2CO32-→3CO2+H2O;則該電池的正極反應式是: 。
(3)密閉容器中充有10 mol CO與20mol H2,在催化劑作用下反應生成甲醇:CO(g)+2H2(g)CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如下圖所示。
①若A、B兩點表示在某時刻達到的平衡狀態,此時在A點時容器的體積為10L,則該溫度下的平衡常數K= ;此時在B點時容器的體積VB 10L(填“大于”、“小于”或“等于”)。
②若A、C兩點都表示達到的平衡狀態,則自反應開始到達平衡狀態所需的時間tA tC(填“大于”、“小于”或“等于”)。
③在不改變反應物用量情況下,為提高CO轉化率可采取的措施是 。
查看答案和解析>>
科目:高中化學 來源:2010年山東省威海市高三第二次模擬考試(理科綜合)化學部分 題型:填空題
(14分)CO和H2可作為能源和化工原料,應用十分廣泛。
(1)已知:C(s)+O2 (g) ===CO2(g) △H1=﹣393.5kJ·mol-1
2H2(g)+O2(g)=== 2H2O(g) △H2=﹣483.6kJ·mol-1
C(s)+H2O(g)=== CO(g)+H2(g) △H3=+131.3kJ·mol-1
則反應CO(g)+H2(g)+O2(g)=== H2O(g)+CO2(g)的△H= kJ·mol-1。標準狀況下的煤炭氣(CO、H2)33.6L與氧氣反應生成CO2和H2O,反應過程中轉移 mol電子。
(2)熔融碳酸鹽燃料電池(MCFS),是用煤氣(CO+H2)作負極燃氣,空氣與CO2的混合氣為正極助燃氣,用一定比例的Li2CO3和Na2CO3低熔點混合物做電解質,以金屬鎳(燃料極)為催化劑制成的。負極的電極反應式為:CO+H2-4e-+2CO32-→3CO2+H2O;則該電池的正極反應式是: 。
(3)密閉容器中充有10 mol CO與20mol H2,在催化劑作用下反應生成甲醇:CO(g)+2H2(g) CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如下圖所示。
CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如下圖所示。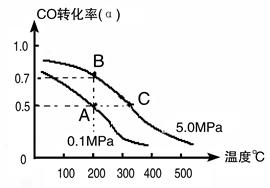
①若A、B兩點表示在某時刻達到的平衡狀態,此時在A點時容器的體積為10L,則該溫度下的平衡常數K= ;此時在B點時容器的體積VB 10L(填“大于”、“小于”或“等于”)。
②若A、C兩點都表示達到的平衡狀態,則自反應開始到達平衡狀態所需的時間tA tC(填“大于”、“小于”或“等于”)。
③在不改變反應物用量情況下,為提高CO轉化率可采取的措施是 。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年遼寧省高三上學期第三次月考化學試卷 題型:填空題
CO和H2可作為能源和化工原料,應用十分廣泛。
(1)已知:C(s)+O2 (g) ===CO2(g) △H1=﹣393.5kJ·mol-1
2H2(g)+O2(g)=== 2H2O(g) △H2=﹣483.6kJ·mol-1
C(s)+H2O(g)=== CO(g)+H2(g) △H3= +131.3kJ·mol-1
則反應CO(g)+H2(g) +O2(g)=== H2O(g)+CO2(g)的△H= 。
標準狀況下的煤炭氣(CO、H2)336L與氧氣反應生成CO2和H2O,反應過程中轉移 mol電子。
(2)熔融碳酸鹽燃料電池(MCFS),是用煤氣(CO+H2)作負極燃氣,空氣與CO2的混合氣為正極助燃氣,用一定比例的Li2CO3和Na2CO3低熔點混合物做電解質,以金屬鎳(燃料極)為催化劑制成的。負極的電極反應式為:CO+H2-4e-+2CO32-===3CO2+H2O;則該電池的正極反應式是: 。
(3)密閉容器中充有1 mol CO與2mol H2,在催化劑作用下反應生成甲醇:CO(g)+2H2(g) CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如下圖所示。
CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如下圖所示。

①若A、B兩點表示在某時刻達到的平衡狀態,此時在A點時容器的體積為10L,則該溫度下的平衡常數K= ;此時在B點時容器的體積VB 10L(填“大于”、“小于”或“等于”)。
②若A、C兩點都表示達到的平衡狀態,則自反應開始到達平衡狀態所需的時間tC tA(填“大于”、“小于”或“等于”)。
③在不改變反應物用量情況下,為提高CO轉化率可采取的措施是 。(寫出兩點即可)
查看答案和解析>>
科目:高中化學 來源:2010年山東省威海市高三第二次模擬考試(理科綜合)化學部分 題型:填空題
(14分)CO和H2可作為能源和化工原料,應用十分廣泛。
(1)已知:C(s)+O2 (g) ===CO2(g) △H1=﹣393.5kJ·mol-1
2H2(g)+O2(g)=== 2H2O(g) △H2=﹣483.6kJ·mol-1
C(s)+H2O(g)=== CO(g)+H2(g) △H3=+131.3kJ·mol-1
則反應CO(g)+H2(g) +O2(g)=== H2O(g)+CO2(g)的△H= kJ·mol-1 。標準狀況下的煤炭氣(CO、H2)33.6L與氧氣反應生成CO2和H2O,反應過程中轉移 mol電子。
(2)熔融碳酸鹽燃料電池(MCFS),是用煤氣(CO+H2)作負極燃氣,空氣與CO2的混合氣為正極助燃氣,用一定比例的Li2CO3和Na2CO3低熔點混合物做電解質,以金屬鎳(燃料極)為催化劑制成的。負極的電極反應式為:CO+H2-4e-+2CO32-→3CO2+H2O;則該電池的正極反應式是: 。
(3)密閉容器中充有10 mol CO與20mol H2,在催化劑作用下反應生成甲醇:CO(g)+2H2(g) CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如下圖所示。
CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如下圖所示。

①若A、B兩點表示在某時刻達到的平衡狀態,此時在A點時容器的體積為10L,則該溫度下的平衡常數K= ;此時在B點時容器的體積VB 10L(填“大于”、“小于”或“等于”)。
②若A、C兩點都表示達到的平衡狀態,則自反應開始到達平衡狀態所需的時間tA tC(填“大于”、“小于”或“等于”)。
③在不改變反應物用量情況下,為提高CO轉化率可采取的措施是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com