
在2L密閉容器內,800℃時反應:2NO(g)+O2(g)![]() 2NO2(g)體系中,n(NO)隨時間的變化如表:
2NO2(g)體系中,n(NO)隨時間的變化如表:
| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01. | 0.008 | 0.007 | 0.007 | 0.007 |
 ⑴寫出該反應的平衡常數表達式:K= 。
⑴寫出該反應的平衡常數表達式:K= 。
已知:![]() >
>![]() ,則該反應是 熱反應。
,則該反應是 熱反應。
⑵右圖中表示NO2的變化的曲線是 。
用O2表示從0~2s內該反應的平均速率v= 。
⑶能說明該反應已達到平衡狀態的是 。
a.v(NO2)=2v(O2) b.容器內壓強保持不變
c.v逆 (NO)=2v正 (O2) d.容器內密度保持不變
⑷ 為使該反應的反應速率增大,且平衡向正反應方向移動的是 。
a.及時分離除NO2氣體 b.適當升高溫度
c.增大O2的濃度 d.選擇高效催化劑
⑴K=c2(NO2)/c2 (NO) c(O2) 放熱
⑵b 1.5×10-3mol·L-1·s-1
⑶b c
⑷c
(1)由根據平衡常數的公式進行書寫。由![]() >
>![]() 說明降低溫度,平衡向正反應方向,可知正反應為放熱反應。
說明降低溫度,平衡向正反應方向,可知正反應為放熱反應。
(2)NO2的起始濃度為c(NO2)=0,2s時c(NO2)可根據圖表中n(NO)變化量求解,c(NO2)=(0.02-0.008)mol/2=0.006mol/L,故答案選b。由圖表可求0~2s內v(NO)=(0.02-0.008)mol/2L.2s=0.003 mol·L-1·s-1,故v(O2)= 1.5×10-3mol·L-1·s-1.
(3)a:在任意狀態下,都存在這樣的速率關系,故不能作為平衡狀態的標志。
b:因該反應為氣體體積不等的反應,故壓強不變可作平衡狀態的標志。
c:由v逆 (NO)=2v正(O2),可推出v逆 (NO)= v正(NO),說明已達平衡狀態。
d.由于平衡體系中全是氣體,容器體積固定,故任意狀態下密度不變,故d錯。
(4)及時分離除NO2氣體,只能使平衡向正反應移動,不能增大反應速率,故a錯;因該反應為放熱反應,升溫雖使反應速率增大,但平衡向逆反應方向移動,故b錯;催化劑只能增大反應速率,不能改變化學平衡的移動的方向,故d錯。


科目:高中化學 來源: 題型:
| 時間/s | 0 | 1 | 2 | 3 | 4 |
| n(A)/mol | 2.0 | 1.0 | 0.8 | 0.8 | 0.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| N2+3H2?2NH3 | ||||
| 溫度 | 25℃ | 200℃ | 400℃ | 600℃ |
| 平衡常數K | 5×108 | 650 | 0.507 | 0.01 |
查看答案和解析>>
科目:高中化學 來源: 題型:
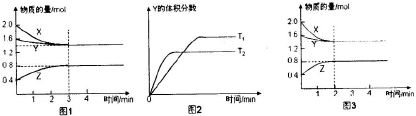
| A、反應進行的前3min內,用X表示的反應速率V(X)=0.1mol/(L?min) | B、平衡時容器內的壓強為反應前的0.8倍 | C、保持其他條件不變,升高溫度,反應的化學平衡常數K減小 | D、若改變反應條件,使反應進程如圖3所示,則改變的條件是增大壓強 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
| 時間/s | 0 | 1 | 2 | 3 | 4 |
| n(A)/mol | 2.0 | 1.0 | 0.8 | 0.8 | 0.8 |
查看答案和解析>>
科目:高中化學 來源:2011-2012學年北京市門頭溝區育園中學高二(下)期末化學試卷(解析版) 題型:填空題
| 時間/s | 1 | 2 | 3 | 4 | |
| n(A)/mol | 2.0 | 1.0 | 0.8 | 0.8 | 0.8 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com