
【題目】NA代表阿伏加德羅常數的值。下列說法正確的是( )
A.足量MnO2和100mL6mol/L濃鹽酸反應產生Cl2的分子數為0.15NA
B.100mL1molFeCl3溶液中所含Fe3+的數目為0.1NA
C.48g正丁烷和10g異丁烷的混合物中碳碳單鍵的數目為3NA
D.密閉容器中,2molSO2和1molO2催化反應后分子總數為2NA
【答案】C
【解析】
A.100mL 6molL-1濃鹽酸中含有氯化氫0.1L×6molL-1=0.6mol,MnO2+4HCl![]() MnCl2+Cl2↑+2H2O,完全反應0.6mol氯化氫可以生成0.15mol氯氣,由于稀鹽酸不與二氧化錳反應,所以生成的氯氣的物質的量小于0.15mol,產生的氯氣分子數小于0.15NA,故A錯誤;
MnCl2+Cl2↑+2H2O,完全反應0.6mol氯化氫可以生成0.15mol氯氣,由于稀鹽酸不與二氧化錳反應,所以生成的氯氣的物質的量小于0.15mol,產生的氯氣分子數小于0.15NA,故A錯誤;
B.Fe3+為弱堿陽離子,水溶液中部分水解,故100 mL 1 molL-1FeCl3溶液中所含Fe3+數目小于0.1NA,故B錯誤;
C.正丁烷和異丁烷只是碳架不同,含有的碳碳單鍵均為3條,所以48g正丁烷和10g異丁烷,即混合物的物質的量為![]() =1mol,所以48g正丁烷和10g異丁烷的混合物中碳碳單鍵數目為3NA,故C正確;
=1mol,所以48g正丁烷和10g異丁烷的混合物中碳碳單鍵數目為3NA,故C正確;
D.SO2和O2的催化反應為可逆反應,反應不可能完全進行,所以密閉容器中,反應生成三氧化硫的物質的量小于2mol,則反應后氣體總物質的量大于2mol,反應后分子總數大于2NA,故D錯誤;
故選C。


 課時訓練江蘇人民出版社系列答案
課時訓練江蘇人民出版社系列答案科目:高中化學 來源: 題型:
【題目】已知:①A的產量通常用來衡量一個國家的石油化工水平;②2CH3CHO+O2![]() 2CH3COOH。現以A為主要原料合成化合物E,其合成路線如圖1所示。回答下列問題:
2CH3COOH。現以A為主要原料合成化合物E,其合成路線如圖1所示。回答下列問題:

(1)寫出下列物質的官能團名稱:B:____________________;D:____________________。
(2)反應④的化學方程式為________________________________________________,反應類型:________。
(3)某學習小組設計物質B催化氧化的實驗裝置如下,根據圖2裝置回答問題。

①裝置甲錐形瓶中盛放的固體藥品可能為________(填字母)。
A.Na2O2 B.KClC.Na2CO3 D.MnO2
②實驗過程中,丙裝置硬質玻璃管中發生反應的化學方程式為_______________________________。
③物質B的催化氧化產物與葡萄糖具有相同的特征反應,將所得的氧化產物滴加到新制氫氧化銅懸濁液中加熱,現象為______________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】滴有酚酞的Ba(OH)2溶液顯紅色,在上述溶液中分別滴加X溶液后有下列現象。下列說法不正確的是
序號 | 裝置 | X溶液 | 現象 |
I |
| 鹽酸 | 溶液紅色褪去,無沉淀,燈泡亮度沒有明顯變化 |
II | Na2SO4 | 溶液紅色不變,有白色沉淀生成,燈泡亮度沒有明顯變化 | |
III | H2SO4 | 溶液紅色褪去,有白色沉淀生成,燈泡逐漸變暗 |
A. 實驗I中溶液紅色褪去,說明發生了反應H+ + OH- =H2O
B. 實驗II中溶液紅色不變,且燈泡亮度沒有明顯變化,說明溶液中依然存在有大量的Na+與OH-
C. 實驗III中溶液紅色褪去,有白色沉淀生成,燈泡逐漸變暗,說明發生了反應Ba2+ + 2OH- + 2H+ + SO42- == BaSO4↓+ 2H2O
D. 將實驗II中Na2SO4溶液換成CuSO4溶液,現象與原實驗II中的現象相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列比較中,正確的是:
A. 常溫下,pH=11的Na2CO3溶液中,水電離出的c(OH-)=1.0×10-3molL-1
B. 同溫度同物質的量濃度時,HF比HCN易電離,則NaF溶液的pH比NaCN溶液的大
C. 物質的量濃度相等的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-)
D. 加熱蒸干AlCl3溶液可得到AlCl3固體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物I是一種醫藥合成中間體,實驗室以芳香烴A為原料制備I的路線如下(部分反應條件已省略):
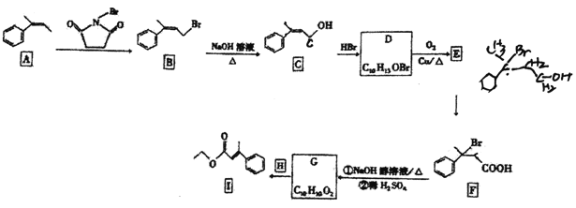
已知:RCH=CH2+HBr![]() RCH2CH2Br。回答下列問題:
RCH2CH2Br。回答下列問題:
(1)X的分子式為C8H8,且X與A互為同系物,則X的化學名稱是 ______。
(2)B生成C的反應類型是_____, B、C含有的相同的官能團名稱是 _____。
(3)碳原子上連有4個不同原子或基團時,該碳原子為手性碳原子。寫出D的結構簡式,并用星號![]() 標出其中的手性碳原子_____。
標出其中的手性碳原子_____。
(4)寫出D—E 的化學反應方程式:_________。
(5)G的結構簡式是 ______。
(6)Y與C是同分異構體,Y中含苯環,且苯環上有2個取代基,Y能發生銀鏡反應,其核磁共振氫譜中有5組峰,且峰面積之比為6:2:2:1:1,則Y的結構簡式為 _______。
(7)丙二酸(HOOCCH2COOH)主要用作醫藥合成中間體、電鍍拋光劑等。結合題目信息,設計以丙烯(CH3CH=CH2) 和![]() 為原料制備丙二酸的合成路線______(無機試劑任選)。
為原料制備丙二酸的合成路線______(無機試劑任選)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】螺[2,2]戊烷的結構簡式如圖。下列關于該化合物的說法錯誤的是( )

A.與環戊烯互為同分異構體B.二氯代物超過兩種
C.所有碳原子不共平面D.與丙烷互為同系物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】完成下列各題:
現有下列七種物質:①液態氯化氫;②小蘇打;③純堿粉末;④葡萄糖;⑤氫氧化鉀;⑥氫氧化鐵膠體;⑦硫酸鐵溶液;
(1)上述七種物質中,屬于電解質的有_______,屬于非電解質的有____。
(2)有兩種物質在水溶液中可發生反應,離子方程式為:H++OH-=H2O,該反應的化學方程式為______________。
(3)除去③中少量②的方法是_______,化學方程式為________________。
(4)現有100mL⑦溶液中含Fe3+5.6g,則溶液中SO42-的物質的量濃度是______。
(5)若在⑥中緩慢加入①的水溶液,產生的現象是_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】把在空氣中久置的鋁片 5.0 g投入盛有500mL0.5mol·L-1硫酸溶液的燒杯中,該鋁片與硫酸反應產生氫氣的速率v與反應時間t可用如下圖的坐標曲線來表示,下列推論錯誤的是( )
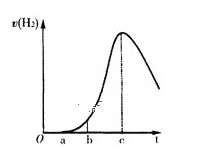
A.t由0→a段不產生氫氣是因為表面的氧化物隔離了鋁和硫酸溶液
B.t由b→c段產生氫氣的速率增加較快的主要原因之一是反應放熱溫度升高
C.t=c時反應處平衡狀態
D.t>c產生氫氣的速率降低主要原因是溶液中c(H+)降低
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z是三種常見元素的單質,甲、乙是兩種常見的化合物,這些單質和化合物之間存在如圖所示的轉化關系(反應條件略)。下列說法不正確的是( )
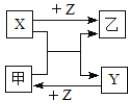
A.甲、乙兩種化合物只能通過化合反應得到
B.X既可以是金屬元素也可以是非金屬元素
C.乙在常溫下,既可以是氣態也可以是液態、固態
D.若X、Y是非金屬元素,則非金屬性X比Y強
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com