
【題目】實驗室欲用NaOH固體配制0.1molL﹣1的NaOH溶液500mL:
(1)本實驗必須用到的儀器有天平、藥匙、玻璃棒、燒杯、膠頭滴管、還有____.
(2)要完成本實驗該同學應稱出______g NaOH.
(3)在配制過程中,其他操作都是正確的,下列操作對濃度無影響的是__(填代號).
①沒有洗滌燒杯和玻璃棒 ②轉移溶液時不慎有少量灑到容量瓶外面 ③容量瓶不干燥,含有少量蒸餾水 ④ 定容后塞上瓶塞反復搖勻,靜置后,液面低于刻度線,再加水至刻度線.
【答案】500mL容量瓶 2.0 ③
【解析】
(1)根據實驗操作的步驟以及每步操作需要儀器確定反應所需儀器;
(2)根據m=cvM計算所需NaOH的質量;
(3)分析操作對溶質的物質的量或對溶液的體積的影響,根據c=![]() 分析判斷。
分析判斷。
(1)用NaOH固體配制0.1 molL﹣1的NaOH溶液500mL必須用到的儀器有天平、藥匙、玻璃棒、燒杯、膠頭滴管、還有500mL容量瓶;
故答案為:500mL容量瓶;
(2)要完成本實驗該同學應稱量NaOH固體的質量為0.5L×0.1mol/L×40g/mol=2.0g;
故答案為:2.0;
(3)①沒有洗滌燒杯和玻璃棒,溶質減少,濃度偏低;
②轉移溶液時不慎有少量灑到容量瓶外面,溶質減少,濃度偏低;
③容量瓶不干燥,含有少量蒸餾水無影響,符合題意;
④定容后塞上瓶塞反復搖勻,靜置后,液面低于刻度線,再加水至刻度線,溶液體積增加,濃度偏低。
故答案為:③。


科目:高中化學 來源: 題型:
【題目】G常用于有機合成和藥物制造,一種合成G的路線如下,請回答相關問題。
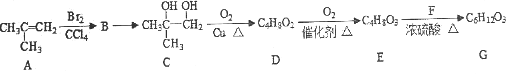
已知:①RCH2Br![]() RCH2OH;
RCH2OH;
②RCHO![]() RCOOH;
RCOOH;
③G分子中含有羥基。
(1)請用系統命名法給A命名_________________。
(2)A→B反應類型為__________。B→C反應試劑和反應條件是_______________。
(3)D分子中官能團名稱為___________________。
(4)C→D反應的化學反應方程式為________________________________________。
(5)E→G反應的化學反應方程式為________________________________________。
(6)滿足下列條件的E的同分異構體還有______種(不包括E),其中核磁共振氫譜中有四組峰,面積比為3:3:1:1的同分異構體的結構簡式為_____________。
①與碳酸鈉溶液反應有氣體產生,②分子中無![]() 結構。
結構。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化合物有碳、氫、氧三種元素組成,其紅外光譜圖有C-H鍵、O-H鍵、C-O鍵的振動吸收,該有機物的相對分子質量是60,則該有機物的結構簡式是( )
A. CH3CH2OCH3 B. CH3CH(OH)CH3
C. CH3CH2CH2OH D. CH3CH2CHO
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在標準狀況下,下列物質所占體積最大的是(NA表示阿伏加德羅常數)( )
A.18gH2OB.NA個氮氣分子C.44.8L HCLD.含有5NA個氫原子的H2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在同溫同壓下,對于等質量的SO2和CO2兩種氣體,求其下列各項比值。
(1)摩爾質量比___________;
(2)密度比___________;
(3)物質的量比___________;
(4)體積比為___________;
(5)分子數比___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素周期表長周期共有18個縱行,從左到右排為18列,即堿金屬是第1列,稀有氣體是第18列。按這種規定,下列說法正確的是( )
A. 第9列元素中沒有非金屬
B. 第15列元素的原子最外層的電子排布是ns2np5
C. 最外層電子排布為ns2的元素一定在第2列
D. 第11、12列為d區的元素
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有34 g 某氣體,它的摩爾質量為17g.mol-1。則:
(1)該氣體為_____________mol
(2)該氣體所含分子數為_________ NA
(3)該氣體在標準狀況下的體積為_________ L
(4) ________g H2O中的氧原子數目與保準狀況22.4LCO2中的氧原子數目相同。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉻是人體必需元素,如含量不足會影響糖類和脂類的代謝,過高則會引起急性中毒。工業上往往采取下列循環工藝防止鉻的污染:

完成下列填空:
(1)含Cr2O72-離子的廢水在酸性條件下用Fe3O4處理,反應的離子方程式如下,配平該離子反應方程式:
_____Cr2O72-+Fe3O4+H+→Cr3++Fe3++H2O
(2)工業上處理含Cr2O72-的廢水時,一般將劇毒的Cr2O72-轉化為Cr3+,以碳為陰極,鐵作陽極,電解處理含NaCl、Cr2O72-的酸性廢水。寫出電極反應:陽極_____________________ 陰極_______________________;用鐵做陽極的目的是:_____________________
(3)反應⑤是可逆反應,在Na2CrO4溶液中加入稀硫酸,溶液由黃色逐漸變成橙色,寫出該反應的離子方程式:______________________
(4)已知Ag2CrO4和AgCl的Ksp分別為9.0×10-12、1.56×10-10,向含有相同濃度的Na2CrO4和NaCl的混合溶液中逐滴加入硝酸銀溶液,首先生成的沉淀是__________
(5)向上述反應后的溶液中加入堿溶液,讓廢水的pH升至8~10,控制適當的溫度,使產物中的金屬陽離子全部轉變為沉淀。回收所得的Cr(OH)3,經處理后又可轉變成K2Cr2O7。純凈的K2Cr2O7常用于準確測定Na2S2O3溶液的物質的量濃度,方法如下:① Cr2O72- +6I- + 14H+ →3I2 + 2Cr3+ + 7H2O ② 2S2O32- + I2→S4O62- + 2I- ,準確稱取純凈的K2Cr2O7 0.294g ,配成溶液,用Na2S2O3溶液滴定,消耗Na2S2O3溶液25.00mL。則Na2S2O3溶液的物質的量濃度為_____________________(保留四位有效數字)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將固體X投入過量的Y中,能生成白色沉淀并放出一種無色氣體,該氣體能燃燒,不易溶于水,則X和Y分別可能是( )
A.鈉和氯化鋁溶液B.鋁和燒堿溶液C.過氧化鈉和氯化亞鐵D.鋅和稀硫酸
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com