
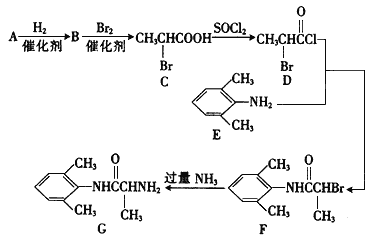
【題目】室安卡因(G)是一種抗心律失常藥物,可由下列路線合成:
I.(1)己知A是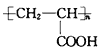 的單體,則A中所含官能團的名稱是____________。
的單體,則A中所含官能團的名稱是____________。
(2)寫出B的結構簡式并用系統命名法給C命名: B:_____________, C的名稱:____________。
(3)L是E的同分異構體,L分子中含有苯環,且苯環上一氯代物只有兩種,則L所有可能的結構簡式有![]() 、__________________。
、__________________。
(4)F →G的反應類型是_______________。
(5)下列關于室安卡因(G)的說法正確的是____________。
a.能發生加成反應 b.能使酸性高錳酸鉀溶液褪色
c.能與鹽酸反應生成鹽 d.屬于氨基酸
(6)寫出C與足量NaOH醇溶液共熱時反應的化學方程式:______________。
II. H是C的同系物,其核磁共振氫譜有兩個峰。按如下路線,由H可合成高聚物V:
![]()
(7)H的結構簡式為_________________;N→Q的反應類型為________________。
(8)寫出Q→V的反應方程式:________________。
【答案】 羧基、碳碳雙鍵 CH3CH2COOH 2-溴丙酸 ![]() 取代反應 a、b、c
取代反應 a、b、c ![]()
![]() 消去反應
消去反應 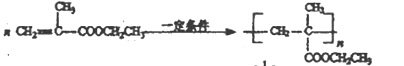
【解析】A是![]() 的單體,則A的結構簡式為:CH2=CHCOOH,A和和氫氣發生加成反應生成B,B的結構簡式為CH3CH2COOH,B和溴發生取代反應生成C,C為CH3CHBrCOOH,C發生取代反應生成D,D和E發生取代反應生成F,F發生取代反應生成G,則
的單體,則A的結構簡式為:CH2=CHCOOH,A和和氫氣發生加成反應生成B,B的結構簡式為CH3CH2COOH,B和溴發生取代反應生成C,C為CH3CHBrCOOH,C發生取代反應生成D,D和E發生取代反應生成F,F發生取代反應生成G,則
(1)A的結構簡式為:CH2=CHCOOH,A中官能團名稱是碳碳雙鍵和羧基;(2)B的結構簡式為CH3CH2COOH,C的結構簡式為CH3CHBrCOOH,C的名稱是2-溴丙酸;(3)L是E的向分異構體,L分子中含有苯環且苯環上一氯代物只有兩種,則L分子中苯環上有兩類氫原子,取代基處于對位位置,則L所有可能的結構簡式有![]() 、
、![]() ;(4)根據F和G結構簡式的差異性知,F和氨氣發生取代反應生成G;(5)G中含有氨基、羰基、苯環,則a.G中含有羰基和苯環,所以能發生加成反應,a正確;b.G連接苯環的碳原子上含有氫原子,所以能被高錳酸鉀氧化生成羧酸,所以能使酸性高錳酸鉀溶液褪色,b正確;c.G中含有氨基,所以能與鹽酸反應生成鹽,c正確;d.G中不含羧基,不屬于氨基酸,d錯誤;答案選abc;(6)C與足量NaOH醇溶液共熱發生的反應涉及兩個方面,一是消去溴化氫分子的反應,二是酸堿中和反應,故1molC消耗2molNaOH,所以其反應方程式為
;(4)根據F和G結構簡式的差異性知,F和氨氣發生取代反應生成G;(5)G中含有氨基、羰基、苯環,則a.G中含有羰基和苯環,所以能發生加成反應,a正確;b.G連接苯環的碳原子上含有氫原子,所以能被高錳酸鉀氧化生成羧酸,所以能使酸性高錳酸鉀溶液褪色,b正確;c.G中含有氨基,所以能與鹽酸反應生成鹽,c正確;d.G中不含羧基,不屬于氨基酸,d錯誤;答案選abc;(6)C與足量NaOH醇溶液共熱發生的反應涉及兩個方面,一是消去溴化氫分子的反應,二是酸堿中和反應,故1molC消耗2molNaOH,所以其反應方程式為![]() ;(7)H是C的同系物,H的相對分子質量是167,H的碳原子個數=(1678016×2+1)/14=4,其核磁共振氫譜有兩個峰,則H的結構簡式為(CH3)2CBrCOOH,H發生酯化反應生成N,N的結構簡式為(CH3)2CBrCOOCH2CH3,N和氫氧化鈉的醇溶液發生消去反應生成Q,Q的結構簡式為CH2=C(CH3)COOCH2CH3,Q發生加聚反應生成V,V的結構簡式為
;(7)H是C的同系物,H的相對分子質量是167,H的碳原子個數=(1678016×2+1)/14=4,其核磁共振氫譜有兩個峰,則H的結構簡式為(CH3)2CBrCOOH,H發生酯化反應生成N,N的結構簡式為(CH3)2CBrCOOCH2CH3,N和氫氧化鈉的醇溶液發生消去反應生成Q,Q的結構簡式為CH2=C(CH3)COOCH2CH3,Q發生加聚反應生成V,V的結構簡式為 。(8)Q→V的反應方程式為
。(8)Q→V的反應方程式為 。
。


 全能測控期末小狀元系列答案
全能測控期末小狀元系列答案科目:高中化學 來源: 題型:
【題目】除去括號內雜質所用試劑和方法均正確的是
A.乙酸乙酯(乙酸):飽和碳酸鈉溶液、分液
B.苯(環己烯):溴水、分液
C.苯(苯酚):溴水、過濾
D.乙烷(乙烯):酸性高錳酸鉀溶液、洗氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】五種短周期元素A、B、C、D、E的性質及結構信息如下:
① 原子半徑A>B>C>D>E;
② 五種元素之間形成的常見的四種分子如下:
甲 | 乙 | 丙 | 丁 | |
比例模型 |
|
|
|
|
組成元素 | D、E | B、E | A、D、E | C、E |
電子總數 | 10 | 18 | 26 | 10 |
請根據上述信息回答下列問題:
(1)A元素的單質與物質甲發生反應的離子方程式為__________,其化學反應平衡常數的表達式為_______。
(2)戊與乙互為同系物,有五種同分異構體,戊的分子式為_____,己與乙具有相同的電子數,與甲含有的元素種類相同,己分子的結構式為_______。
(3)C與E元素組成的CE3與液氮可組成燃料電池,產物均為無污染的物質,可用于驅動潛艇,燃料電池裝置如下圖所示。該電池的負極反應式為_____。電池工作時OH-向_____移動(填“正極”或“負極”)。
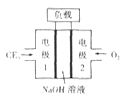
(4)B與D組成的一種物質在自然界中可循環,循環時其與CaCO3反應。已知Ksp(CaCO3)=2.8×10-9,現將CaCl2溶液與Na2CO3溶液等體積混合,若Na2CO3溶液的濃度為2×10-4mol/L,則生成沉淀的最小濃度為__________(忽略混合前后溶液的體積變化)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C三只燒杯中,依次分別盛有NaOH溶液、KSCN溶液、煮沸的蒸餾水,各滴入FeCl3溶液,試根據實驗現象分別回答以下問題:
(1)分別寫出三只燒杯中形成分散系的名稱:
A________,B________,C________。
(2)寫出C中形成分散系的化學方程式:_____________________________________。
(3)若不用化學試劑鑒別,寫出鑒別B、C分散系的兩種簡單方法:
①______________________________________________________,
②________________________________________________________。
(4)向C中逐滴加入稀H2SO4,現象為________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于原子結構的表述中,正確的是( )
A.L能層含軌道數共有8個
B.在基態K原子中,核外電子占據最高能級符合為N
C.電子云輪廓圖半徑隨能層序數增加而增大
D.根據洪特規則每個軌道最多容納2個自旋狀態相反的電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯氣是一種重要的工業原料。工業上利用反應3Cl2+2NH3===N2+6HCl檢查氯氣管道是否漏氣。下列說法錯誤的是( )
A. 若管道漏氣遇氨就會產生白煙
B. 該反應利用了Cl2的強氧化性
C. 該反應中HCl是氧化產物
D. 生成1molN2有6mol電子轉移
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯堿工業以電解精制飽和食鹽水的方法制取氯氣、氫氣、燒堿和氯的含氧酸鹽等系列化工產品。下圖是離子交換膜法電解食鹽水的示意圖,圖中的離子交換膜只允許陽離子通過。完成下列填空:

(1)電解飽和食鹽水的化學方程式是_______________。
(2)離子交換膜的作用為:__________、___________。
(3)精制飽和食鹽水從圖中______位置補充,氫氧化鈉溶液從圖中_____位置流出(選填“a”、“b”、“c”或“d”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉍元素可表示為 83Bi,在元素周期表中相對原子質量標示為209.0,下列說法正確的是
A. Bi元素的質量數是209
B. Bi元素最高價氧化物的化學式為Bi2O3
C. Bi原子最高價氧化物的水化物酸性比硝酸的要強
D. Bi元素位于元素周期表第六周期第ⅤA族
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國最新報導的高超導體中,鉈(Tl)是其中之一,已知位于第六周期第ⅢA族,關于鉈的說法,可能錯誤的是:
A. 是銀白色金屬 B. Tl(OH)3有兩性
C. 與稀鹽酸反應生成鹽酸鹽 D. 鉈的金屬性強于鋁的金屬性
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com