
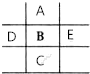
 如圖是元素周期表的一部分,已知A、B、C、D、E5種原子核外共有85個電子,其中只有C元素原子次外層電子數(shù)為18,則B元素是( )
如圖是元素周期表的一部分,已知A、B、C、D、E5種原子核外共有85個電子,其中只有C元素原子次外層電子數(shù)為18,則B元素是( )| A. | 鋁 | B. | 鎂 | C. | 磷 | D. | 硫 |
分析 C元素原子次外層電子數(shù)為18,C原子核外有四個電子層,處于第四周期,則A處于第二周期,B、D、E處于第三周期,A,B,C,D,E五種元素原子核外共有85個電子,令B的核外電子數(shù)為x,則D核外電子數(shù)為x-1,E核外電子數(shù)為x+1,A核外電子數(shù)為x-8,C核外電子數(shù)為x+18,列方程計算x的值,進而確定各元素解答.
解答 解:C元素原子次外層電子數(shù)為18,C原子核外有四個電子層,處于第四周期,則A處于第二周期,B、D、E處于第三周期,A,B,C,D,E五種元素原子核外共有85個電子,令B的核外電子數(shù)為x,則D核外電子數(shù)為x-1,E核外電子數(shù)為x+1,A核外電子數(shù)為x-8,C核外電子數(shù)為x+18,
則:x-1+x+x+1+x-8+x+18=85,解得x=15,故B為P元素,
故選C.
點評 本題考查了元素周期表的應用和元素推斷,題目難度不大,注意理解掌握同主族元素原子序數(shù)關系,側重于考查學生的分析能力.


科目:高中化學 來源: 題型:解答題
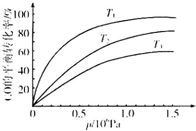 鐵及其化合物在日常生活、生產(chǎn)中應用廣泛,研究鐵及其化合物的應用意義重大.回答下列問題:
鐵及其化合物在日常生活、生產(chǎn)中應用廣泛,研究鐵及其化合物的應用意義重大.回答下列問題:| 溫度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 微粒組 | 加人試劑 | 發(fā)生反應的離子方程式 |
| A | Fe3+、I-、Cr- | NaOH溶液 | Fe3++30H-═Fe(0H)3↓ |
| B | K+、NH3•H20、CO32- | 通人少量CO2 | 20H-+C02═CO32-+H20 |
| C | H+,F(xiàn)e2+、SO42- | Ba(NO3)2溶液 | SO42-+Ba2+═BaSO4↓ |
| D | Na+、Al3+、Cl- | 少量澄淸石灰水 | Al3++30H-═Al(OH)3↓ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應①和②都是離子反應 | B. | 反應①和②都吸收熱量 | ||
| C. | 反應①和②都放出熱量 | D. | 反應③既不吸收熱量也不放出熱量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 47.87是豐度最高的鈦原子的相對原子質量 | |
| B. | 鈦原子的M層上共有10個電子 | |
| C. | 從價電子構型看,鈦屬于某主族元素 | |
| D. | 22為鈦原子的質量數(shù) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含大量Al3+的溶液中:K+、Na+、NO3-、CO32-不能大量共存,因有Al2(CO3)3沉淀生成 | |
| B. | 含大量Fe3+的溶液中:K+Mg2+、I-、Br2-不能大量共存,因2Fe3++2I-=2Fe2++I2 | |
| C. | 由水電離的c(H+)=1×10-14mol/L的溶液中:Ca2+、NO3-、HCO3-、Cl-不能大量共存,因溶液呈酸性,與HCO3-反應產(chǎn)生CO2氣體 | |
| D. | 在NH4Fe(SO4)2溶液中:Na+、K+、S2-、SCN-不能大量共存,只是因Fe3+和S2-反應產(chǎn)生淡黃色的S沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
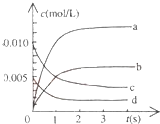 在2L密閉容器內,800℃時反應:2NO(g)+O2(g)?2NO2(g)體系中,n(NO)隨時間的變化如表:
在2L密閉容器內,800℃時反應:2NO(g)+O2(g)?2NO2(g)體系中,n(NO)隨時間的變化如表:| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
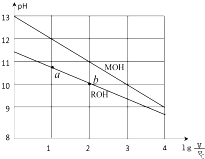 室溫下,將濃度均為0.10mol/L體積均為V0的MOH和ROH溶液,分別加水稀釋至體積V,pH隨$lg\frac{V}{V_0}$的變化如圖所示,下列敘述錯誤的是( )
室溫下,將濃度均為0.10mol/L體積均為V0的MOH和ROH溶液,分別加水稀釋至體積V,pH隨$lg\frac{V}{V_0}$的變化如圖所示,下列敘述錯誤的是( )| A. | ③⑤ | B. | ①⑤ | C. | ①③ | D. | ②④ |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com