
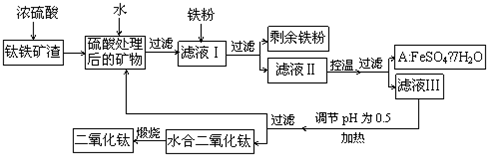
四川攀枝花蘊藏豐富的釩、鈦、鐵資源。用鈦鐵礦渣(主要成分為TiO2、FeO、Fe2O3,Ti的最高化合價為+4)作原料,生產白色顏料二氧化鈦的主要步驟如下:

請回答下列問題:
硫酸與二氧化鈦反應的化學方程式是____________________________________。
向濾液I中加入鐵粉,發生反應的離子方程式為:_________________________、_______________________________________。
(3)在實際生產過程中,向沸水中加入濾液Ⅲ,使混合液pH達0.5,鈦鹽開始水解。水解過程中不斷通入高溫水蒸氣,維持溶液沸騰一段時間,鈦鹽充分水解析出水合二氧化鈦沉淀。請用所學化學平衡原理分析通入高溫水蒸氣的作用:_______________________________________________。
過濾分離出水合二氧化鈦沉淀后,將濾液返回的主要目的是充分利用濾液中的鈦鹽、___________、______________、_______________________(填化學式),減少廢物排放。
(4)A可用于生產紅色顏料(Fe2O3),其方法是:將556a kg A(摩爾質量為278 g/mol)溶于水中,加入適量氫氧化鈉溶液恰好完全反應,鼓入足量空氣攪拌,產生紅褐色膠體;再向紅褐色膠體中加入3336b kg A和112c kg鐵粉,鼓入足量空氣攪拌,反應完成后,有大量Fe2O3附著在膠體粒子上以沉淀形式析出;過濾后,沉淀經高溫灼燒得紅色顏料。若所得濾液中溶質只有硫酸鈉和硫酸鐵,則理論上可生產紅色顏料_______________________kg。
(1) ![]() 或
或![]()
(2)![]()
![]()
(3) 加水促進鈦鹽水解,加熱促進鈦鹽水解,降低![]() 濃度促進鈦鹽水解
濃度促進鈦鹽水解
![]()
![]()
![]()
(4) ![]()
本題考查元素化合物知識、鹽類水解知識和工藝流程分析能力。該工藝流程過程是:濃硫酸溶解礦為Ti4+、Fe2+和Fe3+鹽濾去礦渣得濾液I→加入過量鐵粉濾液中的Fe3+被還原為Fe2+,消耗溶液中的H+,過濾得濾液II→降溫、過濾后得到綠礬和濾液III→調整pH促進Ti4+水解,過濾→濾液中的H+、H2O和Fe2+仍能循環使用。(3)水解為吸熱反應,高溫水蒸氣能夠促進Ti4+的水解。(4)明確該制備過程的目的和作用,才能得出量的關系。第一階段FeSO4與NaOH恰好完全反應:FeSO4+2NaOH=Fe(OH)2+Na2SO4,鼓入空氣后該部分的鐵元素最終都轉化為Fe2O3,則生成的Fe2O3的質量(m1)為
2FeSO4~4NaOH~Fe2O3
556 160
556akg m1
m1=160akg
鐵粉用于消耗溶液的酸性,根據題意在氧氣作用下,最終加入的FeSO4和Fe,也轉化為Fe2(SO4)3和Fe2O3。根據鐵元素守恒,可有如下轉化關系:
6FeSO4~2Fe2(SO4)3~Fe2O3
278×6 160
3336bkg m2
m 2=320bkg
2Fe ~ Fe2O3
112 160
112ckg m3
m 3=160ckg。
【技巧點撥】本題利用了守恒法和關系式法,使計算省去了繁瑣的過程,當然守恒法和關系式法是建立在對所涉及到的反應數量關系熟練的基礎之上的。常用的守恒法有質量守恒、電荷守恒、質子守恒、電子守恒等。


 學而優暑期銜接南京大學出版社系列答案
學而優暑期銜接南京大學出版社系列答案 Happy holiday歡樂假期暑假作業廣東人民出版社系列答案
Happy holiday歡樂假期暑假作業廣東人民出版社系列答案科目:高中化學 來源: 題型:閱讀理解
查看答案和解析>>
科目:高中化學 來源: 題型:
四川攀枝花蘊藏豐富的釩、鈦、鐵資源。用鈦鐵礦渣(主要成分為TiO2、FeO、Fe2O3,Ti的最高化合價為+4)作原料,生產白色顏料二氧化鈦的主要步驟如下:![]()
![]()
![]() w_w w. k#s5_u.c o*m
w_w w. k#s5_u.c o*m

請回答下列問題:![]()
![]()
![]() w_w w. k#s5_u.c o*m
w_w w. k#s5_u.c o*m
(1) 硫酸與二氧化鈦反應的化學方程式是____________________________________。
(2) 向濾液I中加入鐵粉,發生反應的離子方程式為:_________________________、_______________________________________。
(3) 在實際生產過程中,向沸水中加入濾液Ⅲ,使混合液pH達0.5,鈦鹽開始水解。水解過程中不斷通入高溫水蒸氣,維持溶液沸騰一段時間,鈦鹽充分水解析出水合二氧化鈦沉淀。請用所學化學平衡原理分析通入高溫水蒸氣的作用:_______________________________________________。
過濾分離出水合二氧化鈦沉淀后,將濾液返回的主要目的是充分利用濾液中的鈦鹽、___________、______________、_______________________(填化學式),減少廢物排放。
(4)A可用于生產紅色顏料(Fe2O3),其方法是:將556a kgA(摩爾質量為278 g/mol)溶于水中,加入適量氫氧化鈉溶液恰好完全反應,鼓入足量空氣攪拌,產生紅褐色膠體;再向紅褐色膠體中加入3336b kg A和112c kg鐵粉,鼓入足量空氣攪拌,反應完成后,有大量Fe2O3附著在膠體粒子上以沉淀形式析出;過濾后,沉淀經高溫灼燒得紅色顏料。若所得濾液中溶質只有硫酸鈉和硫酸鐵,則理論上可生產紅色顏料_______________________kg。
查看答案和解析>>
科目:高中化學 來源:2010-2011學年廣東省中山市高三化學模擬試卷(八) 題型:填空題
(16分)四川攀枝花蘊藏豐富的釩、鈦、鐵資源。用鈦鐵礦渣(主要成分為TiO2、FeO、Fe2O3,Ti的最高化合價為+4)作原料,生產白色顏料二氧化鈦的主要步驟如下:

請回答下列問題:

(1) 硫酸與二氧化鈦反應的化學方程式是____________________________________。
(2) 向濾液I中加入鐵粉,發生反應的離子方程式為:_________________________、_______________________________________。
(3) 在實際生產過程中,向沸水中加入濾液Ⅲ,使混合液pH達0.5,鈦鹽開始水解。水解過程中不斷通入高溫水蒸氣,維持溶液沸騰一段時間,鈦鹽充分水解析出水合二氧化鈦沉淀。請用所學化學平衡原理分析通入高溫水蒸氣的作用:_______________________________________________。
過濾分離出水合二氧化鈦沉淀后,將濾液返回的主要目的是充分利用濾液中的鈦鹽、___________、______________、_______________________(填化學式),減少廢物排放。
(4)A可用于生產紅色顏料(Fe2O3),其方法是:將556a kgA(摩爾質量為278 g/mol)溶于水中,加入適量氫氧化鈉溶液恰好完全反應,鼓入足量空氣攪拌,產生紅褐色膠體;再向紅褐色膠體中加入3336b kg A和112c kg鐵粉,鼓入足量空氣攪拌,反應完成后,有大量Fe2O3附著在膠體粒子上以沉淀形式析出;過濾后,沉淀經高溫灼燒得紅色顏料。若所得濾液中溶質只有硫酸鈉和硫酸鐵,則理論上可生產紅色顏料_______________________kg。
查看答案和解析>>
科目:高中化學 來源:2010-2011學年寧夏高三第三次月考(理科綜合)化學卷 題型:填空題
四川攀枝花蘊藏豐富的釩、鈦、鐵資源。用鈦鐵礦渣(主要成分為TiO2、FeO、Fe2O3,Ti的最高化合價為+4)作原料,生產白色顏料二氧化鈦的主要步驟如下:

請回答下列問題:
(1)硫酸與二氧化鈦反應的化學方程式是____________________________(2分)
(2)向濾液I中加入鐵粉,發生反應的離子方程式為:______________________、
________________________________。(各2分)
(3)在實際生產過程中,向沸水中加入濾液Ⅲ,使混合液pH達0.5,鈦鹽開始水解。水解過程中不斷通入高溫水蒸氣,維持溶液沸騰一段時間,鈦鹽充分水解析出水合二氧化鈦沉淀。請用所學化學平衡原理分析通入高溫水蒸氣的作用:__________________________(2分)
(4)過濾分離出水合二氧化鈦沉淀后,將濾液返回的主要目的是充分利用濾液中的鈦鹽、___________、_____________、___________________(填化學式,各2分),減少廢物排放。
(5)A可用于生產紅色顏料(Fe2O3),其方法是:將556a kgA(摩爾質量為278 g/mol)溶于水中,加入適量氫氧化鈉溶液恰好完全反應,鼓入足量空氣攪拌,產生紅褐色膠體;再向紅褐色膠體中加入3336b kg A和112c kg鐵粉,鼓入足量空氣攪拌,反應完成后,有大量Fe2O3附著在膠體粒子上以沉淀形式析出;過濾后,沉淀經高溫灼燒得紅色顏料。若所得濾液中溶質只有硫酸鈉和硫酸鐵,則理論上可生產紅色顏料_____________kg(1分)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com