


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
| A、保持容器容積和溫度不變,向容器內補充了NO2 |
| B、保持容器壓強和溫度不變,向容器內補充了N2O4 |
| C、保持容器容積和溫度不變,向容器內補充了N2 |
| D、保持容器的容積不變,升高了溫度 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
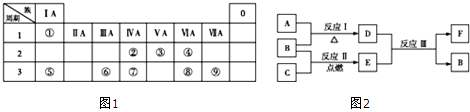
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、海南島四面環海,水資源豐富,不必節約用水 |
| B、明礬既能沉降水中的懸浮物,又能殺菌消毒 |
| C、可通過長期飲用含Ca2+濃度較高的水來補鈣 |
| D、長期飲用純凈水,有可能引起一些微量元素缺乏癥 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、1mol甲醇中含有C-H鍵的數目為4NA |
| B、25℃,pH=13的NaOH溶液中含有OH-的數目為0.1NA |
| C、常溫下,18g重水(D2O)所含的電子數為10NA |
| D、一定條件下,2.3g的Na完全與O2反應生成3.6g產物時失去的電子數為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:
| ||
| A、NaAlH4中氫元素為+1價 |
| B、每生成11.2 L(標準狀況下)H2,轉移2NA個電子 |
| C、在反應中有50%的氫被氧化 |
| D、反應中氧化產物與還原產物的物質的量之比為1:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:
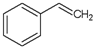 )的敘述,錯誤的是( )
)的敘述,錯誤的是( )| A、可以與溴水反應 |
| B、能夠使酸性高錳酸鉀溶液褪色 |
| C、分子式C8H8 |
| D、1mol苯乙烯可以和1molH2發生加成反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com