
【題目】已知:Fe(OH)3的Ksp=2.79×10-39,Al(OH)3的Ksp=1.3×10-31。現將20 mL 0.05 mol/L FeCl3和20 mL 0.05 mol/L AlCl3混合,再向溶液中逐滴加入0.10 mol/L NaOH溶液,測定溶液的pH變化如圖所示,則下列說法不正確的是( )
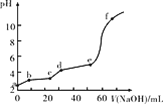
A.a點處,Al3+水解程度比Fe3+水解程度大
B.bc段主要產生Fe(OH)3沉淀
C.de段主要反應:Al3++3OH-=Al(OH)3↓
D.向f點所得溶液中通入足量CO2,沉淀的質量會變大
【答案】A
【解析】
Fe3+水解平衡Fe3++3H2OFe(OH)3+3H+,水解平衡常數Kh(Fe3+)=c3(H+)÷c(Fe3+)=K3w÷Ksp[Fe(OH)3],同理可得Kh(Al3+)=K3w÷Ksp[Al(OH)3]。
A.由于Ksp[Al(OH)3]>Ksp[Fe(OH)3],即Kh(Fe3+)>Kh(Al3+),故a點處Fe3+水解程度比Al3+水解程度大,故A錯誤;
B.隨著NaOH溶液的滴加,Fe3+先沉淀,Al3+后沉淀,bc段主要產生Fe(OH)3沉淀,故B正確;
C.de段主要產生Al(OH)3沉淀,故C正確;
D.f點的pH>10,故Al(OH)3已經全部溶解生成AlO2,沉淀只為Fe(OH)3,此時若通入足量CO2,發生反應AlO2+CO2+2H2O=Al(OH)3↓+HCO3,重新生成Al(OH)3沉淀,碳酸酸性很弱,并不能溶解Fe(OH)3和Al(OH)3,則沉淀總質量增加,故D正確;
故選:A。


科目:高中化學 來源: 題型:
【題目】已知前四周期A、B、C、D、E五種元素的原子序數依次增大,其中A原子所處的周期數、族序數都與其原子序數相等;B原子核外電子有6種不同的運動狀態;D原子L電子層上有2對成對電子;E基態原子有6個未成對電子:
請填寫下列空白:
(1)E元素在元素周期表的位置是______,E元素基態原子的價電子排布式為_____;
(2)C基態原子的價層電子的軌道表達式______;
(3)B2A4是重要的基本石油化工原料。1molB2A4分子中含_____molσ鍵;
(4)BD2電子式為_____,此分子鍵角為_______;
(5)BD32-中心原子孤電子對數為______,離子的立體構型為______;
(6)B、C、D三種元素的第一電離能由小到大的順序為______(填元素符號),其原因為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】近年來流行喝蘋果醋。蘋果醋是一種由蘋果發酵而成的具有解毒、降脂、減肥和止瀉等作用的保健食品。蘋果酸(α羥基丁二酸)是這種飲料的主要酸性物質,其結構如下圖所示:

下列相關說法正確的是( )
A. 蘋果酸在一定條件下能發生消去反應
B. 蘋果酸在一定條件下能催化氧化生成醛
C. 蘋果酸在一定條件下能發生加聚反應生成高分子化合物
D. 1 mol蘋果酸與NaHCO3溶液反應最多消耗3 mol NaHCO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由于具有超低耗電量、壽命長的特點,LED產品越來越受人歡迎。下圖是氫氧燃料電池驅動LED發光的裝置。下列有關敘述正確的是( )
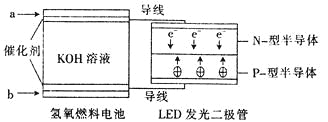
A.a處通人氧氣,b處通人氫氣
B.該裝置中只涉及兩種形式的能量轉化
C.電池正極電極反應式為O2+2H2O+4e-﹦4OH-
D.P一型半導體連接的是電池負極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H2S水溶液中存在電離平衡:H2S![]() H++HS-和HS-
H++HS-和HS-![]() H++S2-,若向H2S溶液中( )
H++S2-,若向H2S溶液中( )
A.加入硫酸,平衡向右移動,溶液中氫離子濃度增大
B.通入過量SO2氣體,溶液酸性減弱
C.通入氯氣,平衡向左移動,溶液酸性增強
D.加入少量硫酸銅固體(忽略體積變化),溶液中所有離子濃度都減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】煤是重要的能源,也是生產化工產品的重要原料。試用所學知識,解答下列問題:
(1)煤的轉化技術包括煤的氣化技術和液化技術。煤的液化技術又分為________和________。
(2)在煤燃燒前需對煤進行脫硫處理。煤的某種脫硫技術的原理為FeS2![]() Fe2++SO42—
Fe2++SO42—![]() Fe3+這種脫硫技術稱為微生物脫硫技術。該技術的第一步反應的離子方程式為_______________________,第二步反應的離子方程式為________________。
Fe3+這種脫硫技術稱為微生物脫硫技術。該技術的第一步反應的離子方程式為_______________________,第二步反應的離子方程式為________________。
(3)工業煤干餾得到的產品有焦炭、________。
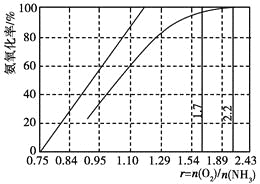
(4)工業上主要采用氨氧化法生產硝酸,如圖是氨氧化率與氨-空氣混合氣中氧氨比的關系。其中直線表示反應的理論值;曲線表示生產實際情況。當氨氧化率達到100%,理論上r[n(O2)/n(NH3)]=________,實際生產要將r值維持在1.7~2.2之間,原因是__________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各項敘述中,正確的是
A.C6H5CH2CH2OH與C6H5OH互為同系物
B.CH3CHO與CH3COOH在一定條件下均能與新制氫氧化銅反應
C.![]() 與
與![]() 互為同分異構體
互為同分異構體
D.H2O與D2O互為同素異形體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】探究草酸(H2C2O4)的性質,室溫下進行以下兩組實驗:(已知:室溫下,H2C2O4的電離平衡常數Ka1=5.0×10-2,Ka2=5.4×10-5)
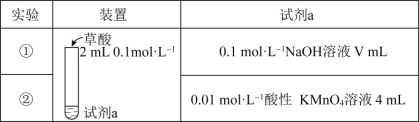
下列有關實驗說法正確的是( )
A.若實驗①中V=2,則混合后溶液中:c(C2O42-)>c(H2C2O4)
B.若實驗①中V=4,則混合后溶液中:c(H+)+c(H2C2O4)+c(HC2O4-)=c(OH-)
C.實驗②反應的離子方程式為5C2O42-+16H++2MnO4-=2Mn2++10CO2↑+8H2O
D.若實驗②測得KMnO4溶液的褪色時間為40s,則這段時間內的平均反應速率v(KMnO4)=2.5×10-4molL-1s-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關電解質溶液的說法中正確的是
A.pH均為5的HCl和NH4Cl溶液中,兩溶液中水的電離程度相同
B.常溫下,在pH=12的氫氧化鈉溶液中加入pH=2的HA溶液至pH剛好等于7,所得溶液中一定存在c(A-)=c(Na+)>c(H+)=c(OH-)
C.等體積、等濃度的NaX溶液和弱酸HX溶液混合后的溶液中一定存在:c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
D.淺綠色的Fe(NO3)2溶液中存在著如下的平衡:Fe2++2H2O![]() Fe(OH)2+2H+,若在此溶液中加入鹽酸, c(H+)增大,平衡左移,溶液的綠色變深
Fe(OH)2+2H+,若在此溶液中加入鹽酸, c(H+)增大,平衡左移,溶液的綠色變深
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com