
| A. | 甲烷的標準燃燒熱為890.3 kJ•mol-1,則甲烷燃燒的熱化學方程式可表示為:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,將0.5mol N2和1.5mol H2置于密閉的容器中充分反應生成NH3(g),放熱19.3 kJ,其熱化學方程式為:N2(g)+3H2(g) $?_{500℃/30MPa}^{催化劑}$2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 相同條件下,2mol氫原子所具有的能量小于1mol氫分子所具有的能量 | |
| D. | 含 1mol NaOH的稀溶液分別和含1mol CH3COOH、1mol HNO3的稀溶液反應,后者比前者放出的熱量多 |
分析 A.燃燒熱是1mol可燃物完全燃燒生成穩定氧化物放出的熱量;
B.0.5molN2和1.5molH2置于密閉容器中充分反應生成NH3(g),放熱19.3kJ,生成的氨氣的物質的量小于1mol;
C.原子結合成分子會釋放能量;
D.弱酸電離吸熱.
解答 解:A.根據燃燒熱的概念:1mol可燃物完全燃燒生成穩定的氧化物,所放出的熱量為燃燒熱,水的狀態應該為液態,故A錯誤;
B.0.5mol N2和1.5molH2置于密閉的容器中充分反應生成NH3(g),放熱19.3kJ,因反應為可逆反應,則1molN2和3molH2置于密閉的容器中充分反應生成NH3(g),放熱不是38.6kJ,則熱化學反應方程式中的反應熱數值錯誤,故B錯誤;
C.原子結合成分子會釋放能量,所以相同條件下,2mol氫原子所具有的能量大于1mol氫分子所具有的能量,故C錯誤;
D.含1mol NaOH的稀溶液分別和含1mol CH3COOH、1mol HNO3的稀溶液反應,醋酸為弱酸電離吸熱,所以醋酸發生中和反應放出的熱量較少,即后者比前者放出的熱量多,故D正確.
故選D.
點評 本題考查學生反應熱的有關知識,注意對中和熱和燃燒熱的概念理解,掌握基礎是關鍵,題目難度不大.


科目:高中化學 來源: 題型:解答題
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 四 | ⑧ |
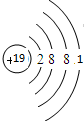 ,最高價氧化物對應的水化物中,酸性最強的是HClO4(用化學式表示).
,最高價氧化物對應的水化物中,酸性最強的是HClO4(用化學式表示). ,
,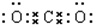 .
.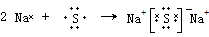 該化合物屬于離子(填“共價”或“離子”)化合物.
該化合物屬于離子(填“共價”或“離子”)化合物.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 同質量的N2和CO2 | B. | 同質量的H2和N2 | ||
| C. | 同體積的O2和N2 | D. | 相同物質的量的N2O和CO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖表示一個電解池,裝有電解質溶液a,X、Y是兩塊電極板,通過導線與直流電源相連.請回答以下問題:
如圖表示一個電解池,裝有電解質溶液a,X、Y是兩塊電極板,通過導線與直流電源相連.請回答以下問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 科學家把C60和鉀摻雜在一起制造了一種富勒烯化合物,其晶胞如圖所示,該物質在低溫時是一種超導體.該物質中K原子和C60分子的個數比為3:1.
科學家把C60和鉀摻雜在一起制造了一種富勒烯化合物,其晶胞如圖所示,該物質在低溫時是一種超導體.該物質中K原子和C60分子的個數比為3:1.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 臭氧層中氧分解歷程如圖所示,下列說法正確的是( )
臭氧層中氧分解歷程如圖所示,下列說法正確的是( )| A. | 催化反應①②均為放熱反應 | |
| B. | 催化劑不能改變該反應的反應熱 | |
| C. | ClO是該反應的催化劑 | |
| D. | 在該反應過程中沒有化學鍵的斷裂與生成 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用水潤濕的pH試紙來測量溶液的pH | |
| B. | 實驗需要480mL 2.0mol•L-1的氫氧化鈉溶液.配制該溶液時先稱量氫氧化鈉固體38.4g,然后再按照溶解、冷卻、移液、洗滌、定容、搖勻的步驟進行操作 | |
| C. | 向溶液中滴加硝酸酸化的Ba(NO3)2溶液出現白色沉淀,說明溶液中一定有SO42- | |
| D. | 用溴水,淀粉、KI溶液比較Br2與I2的氧化性強弱,所需玻璃儀器主要有:試管、膠頭滴管 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com