

分析 白云石煅燒發生反應:CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaO+CO2↑,MgCO3$\frac{\underline{\;高溫\;}}{\;}$MgO+CO2↑,在鍛粉中加入適量的NH4NO3溶液后,鎂化合物幾乎不溶,由于NH4NO3溶液水解顯酸性,與CaO反應生成Ca(NO3)2和NH3•H2O,故過濾后溶液中含Ca(NO3)2和NH3•H2O,將CO2和NH3通入濾液I中后發生反應:Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,據此分析濾液中的陰離子;若濾液Ⅰ中僅通入CO2,會造成CO2過量,廢鋁片加入氫氧化鈉溶液反應生成偏鋁酸鈉溶液,用NaOH溶液可除去廢Al片表面的氧化膜,電解制備Al(OH)3時,電極分別為Al片和石墨,在碳酸鈉溶液中攪拌電解,得到氫氧化鋁,過濾加熱灼燒得到氧化鋁,碳酸鈣和氧化鋁共混加熱1500°C得到七鋁十二鈣,
(1)鍛粉是由白云石高溫煅燒而來;用適量NH4NO3溶液浸取煅粉后,鎂化合物幾乎不溶,即得Mg(OH)2的飽和溶液,CaSO4微溶于水;
(2)在鍛粉中加入適量的NH4NO3溶液后,鎂化合物幾乎不溶,由于NH4NO3溶液水解顯酸性,與CaO反應生成Ca(NO3)2和NH3•H2O,故過濾后溶液中含Ca(NO3)2和NH3•H2O,將CO2和NH3通入濾液I中后發生反應:Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,據此分析濾液中的陰離子;若濾液Ⅰ中僅通入CO2,會造成CO2過量,據此分析產物;
(3)氧化鋁和氫氧化鈉反應生成偏鋁酸鈉和水;
(4)電解制備Al(OH)3時,電極分別為Al片和石墨,鋁被氧化生成氫氧化鋁,陰極生成氫氣.
解答 解:白云石煅燒發生反應:CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaO+CO2↑,MgCO3$\frac{\underline{\;高溫\;}}{\;}$MgO+CO2↑,在鍛粉中加入適量的NH4NO3溶液后,鎂化合物幾乎不溶,由于NH4NO3溶液水解顯酸性,與CaO反應生成Ca(NO3)2和NH3•H2O,故過濾后溶液中含Ca(NO3)2和NH3•H2O,將CO2和NH3通入濾液I中后發生反應:Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,據此分析濾液中的陰離子;若濾液Ⅰ中僅通入CO2,會造成CO2過量,廢鋁片加入氫氧化鈉溶液反應生成偏鋁酸鈉溶液,用NaOH溶液可除去廢Al片表面的氧化膜,電解制備Al(OH)3時,電極分別為Al片和石墨,在碳酸鈉溶液中攪拌電解,得到氫氧化鋁,過濾加熱灼燒得到氧化鋁,碳酸鈣和氧化鋁共混加熱1500°C得到七鋁十二鈣,
(1)鍛粉是由白云石高溫煅燒而來,在煅燒白云石時,發生反應:CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaO+CO2↑,MgCO3$\frac{\underline{\;高溫\;}}{\;}$MgO+CO2↑,故所得鍛粉主要含MgO和CaO;用適量NH4NO3溶液浸取煅粉后,鎂化合物幾乎不溶,即得Mg(OH)2的飽和溶液,CaSO4微溶于水,如果用(NH4)2SO4代替NH4NO3,會生成CaSO4沉淀引起Ca2+的損失,
故答案為:CaO;加入(NH4)2SO4會生成CaSO4微溶物,在過濾時會被除去,造成生成的CaCO3減少.
(2)在鍛粉中加入適量的NH4NO3溶液后,鎂化合物幾乎不溶,由于NH4NO3溶液水解顯酸性,與CaO反應生成Ca(NO3)2和NH3•H2O,故過濾后溶液中含Ca(NO3)2和NH3•H2O,將CO2和NH3通入濾液I中后發生反應:Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,故濾液中的陰離子主要為NO3-,還含有OH-;若濾液Ⅰ中僅通入CO2,會造成CO2過量,則會生成Ca(HCO3)2,從而導致CaCO3產率降低,
故答案為:NO3-、OH-;Ca(HCO3)2;
(3)氧化鋁和氫氧化鈉反應生成偏鋁酸鈉和水,離子反應為Al2O3+2OH-═2AlO2-+H2O,故答案為:Al2O3+2OH-═2AlO2-+H2O;
(4)電解制備Al(OH)3時,電極分別為Al片和石墨,鋁被氧化生成氫氧化鋁,陰極生成氫氣,電解總反應方程式為2Al+6H2O$\frac{\underline{\;通電\;}}{\;}$2Al(OH)3↓+3H2↑,
故答案為:2Al+6H2O$\frac{\underline{\;通電\;}}{\;}$2Al(OH)3↓+3H2↑.
點評 本題綜合考查物質的制備以及分離提純,為高頻考點,側重于學生的分析、實驗能力的考查,注意把握物質的性質以及題給信息,難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | ①④ | B. | ②③④ | C. | ②④ | D. | 全部正確 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
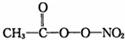 (PAN)等二次污染物.
(PAN)等二次污染物.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1種 | B. | 2種 | C. | 3種 | D. | 4種 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 摩爾質量為126 | |
| B. | 式量為126 | |
| C. | 每個C3H6N6分子含3個N2分子 | |
| D. | 0.1NA個C3H6N6分子含碳原子數為1.806×1023 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
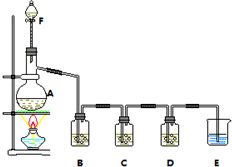 某小組欲探究Cl2與KI溶液的反應,設計實驗裝置如下圖.
某小組欲探究Cl2與KI溶液的反應,設計實驗裝置如下圖.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com