
【題目】乙炔、乙烯均是重要的化工原料。回答下列問題:
(1)1902年,Sabatier首次發現,常壓下過渡金屬可以催化含有雙鍵或叁鍵的氣態烴的加氫反應。
①已知:C2H2(g)+H2(g)═C2H4(g)△H1=-174.3kJ·mol—1
K1(300K)=3.37×1024
C2H2(g)+2H2(g)=C2H6(g)△H2═-311.0kJ·mol一l
K2(300K)═1.19×1042
則反應C2H4(g)+H2(g)═C2H6(g)的△H=___kJ·mol一1,K(300K)=__(保留三位有效數字)。
②2010年Sheth等得出乙炔在Pd表面選擇加氫的反應機理(如圖)。其中吸附在Pd表面上的物種用*標注。

上述吸附反應為____(填“放熱”或“吸熱”)反應,該歷程中最大能壘(活化能)為____kJ·mol-1,該步驟的化學方程式為____。
(2)在恒容密閉容器中充入乙烯,一定條件下發生反應C2H4(g)C2H2(g)+H2(g)。乙烯的離解率為a,平衡時容器內氣體總壓強為P總,則分壓p(C2H4)═___(用p總和a表示)。
(3)用如圖裝置電解含CO2的某酸性廢水溶液,陰極產物中含有乙烯。

該分離膜為___(填“陽”或“陰”)離子選擇性交換膜;生成乙烯的電極反應式為___。
【答案】-136.7 3.53×1017 放熱 +85 C2H3*+H*→C2H4* ![]() 陽 2CO2+12H++12e-=C2H4+4H2O
陽 2CO2+12H++12e-=C2H4+4H2O
【解析】
(1)①根據蓋斯定律,△H2-△H1可得C2H4(g)+H2(g)═C2H6(g)的△H,K=![]() ;
;
②吸附時能量降低,解吸時能量升高,C2H3*+H*→C2H4*的活化能最大,為+85kJ·mol-1;
(2)根據三段式列式求解;平衡分壓:p(C2H4)=n(C2H4)/n總 P總;
(3)陽極發生反應:2H2O一4e-=4H++O2↑,生成的H+向陰極移動,故用陽離子選擇性交換膜,在陽極CO2得到電子結合H+生成一系列燃料,其中生成乙烯的電極反應為2CO2+12H++12e-=C2H4+4H2O。
(1)①C2H4(g)+H2(g)═C2H6(g)的△H=△H2-△H1=-136.7kJ·mol-1,300K時的平衡常數K=![]() =1.19×1042/3.37×1024=3.53×1017。
=1.19×1042/3.37×1024=3.53×1017。
②由圖可知,吸附時能量降低,解吸時能量升高,如C2H4*→C2H4 △H=+82kJ·mol-1,基元反應中,C2H3*+H*→C2H4*的活化能最大,為+85kJ·mol-1。
(2)由反應:C2H4(g)![]() C2H2(g)+H2(g)
C2H2(g)+H2(g)
起始/mol n 0 0
轉化/mol ![]()
![]()
![]()
平衡/mol ![]()
![]()
![]()
平衡時總物質的量:![]() ,
,
平衡分壓:p(C2H4)=![]() 。
。
(3)陽極發生反應:2H2O一4e-=4H++O2↑,生成的H+向陰極移動,故用陽離子選擇性交換膜,在陽極CO2得到電子結合H+生成一系列燃料,其中生成乙烯的電極反應為2CO2+


 A加金題 系列答案
A加金題 系列答案 全優測試卷系列答案
全優測試卷系列答案科目:高中化學 來源: 題型:
【題目】科學家研發出一種新型水溶液鋰電池,采用復合膜包裹的金屬鋰作負極,錳酸鋰(LiMn2O4)作正極,以0.5 mol/Li2SO4 水溶液作電解質溶液。電池充、放電時,LiMn2O4與Li2Mn2O4可以相互轉化。下列有關該電池的說法正確的是
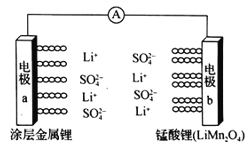
A. 該電池放電時,溶液中的SO42-向電極b移動
B. 該電池負極的電極反應式為:2Li+2H2O==2LiOH+H2↑
C. 電池充電時,外加直流電源的正極與電極a相連
D. 電池充電時,陽極的電極反應式為:Li2Mn2O4-e-==LiMn2O4 +Li+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用酸解法制鈦白粉產生的廢液[含有大量的FeSO4、H2SO4和少量的Fe2(SO4)3、TiOSO4]生產鐵紅和補血劑乳酸亞鐵的工藝流程如圖所示:
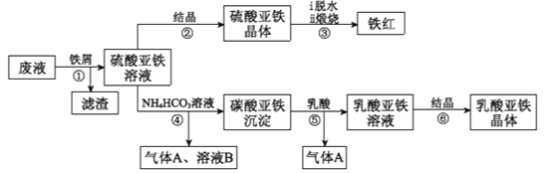
已知:TiOSO4可溶于水,在水中可以電離為TiO2+和SO42-,TiO2+水解成TiO2·xH2O沉淀為可逆反應;乳酸結構簡式為CH3CH(OH)COOH。
回答下列問題:
(1)TiOSO4中鈦元素的化合價是____________,步驟①中分離硫酸亞鐵溶液和濾渣的操作是___________。
(2)濾渣的主要成分為TiO2·xH2O,結合離子方程式解釋得到濾渣的原因:________。
(3)從硫酸亞鐵溶液中得到硫酸亞鐵晶體的操作方法是____________________;硫酸亞鐵在空氣中煅燒生成鐵紅和三氧化硫,該反應的氧化劑和還原劑的物質的量之比為______。
(4)步驟④中發生反應的離子方程式為______________________。
(5)步驟⑥必須控制一定的真空度,原因是有利于蒸發水以及____________________。
(6)實驗室中檢驗溶液B中主要陽離子的方法是______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】四溴化鈦(TiBr4)可用作橡膠工業中烯烴聚合反應的催化劑。已知TiBr4常溫下為橙黃色固體,熔點為38.3℃,沸點為233.5℃,具有潮解性且易發生水解。實驗室利用反應TiO2+C+2Br2![]() TiBr4+CO2制備TiBr4的裝置如圖所示。回答下列問題:
TiBr4+CO2制備TiBr4的裝置如圖所示。回答下列問題:
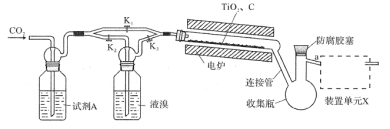
(1)檢查裝置氣密性并加入藥品后,加熱前應進行的操作是__,其目的是__,此時活塞K1,K2,K3的狀態為__;一段時間后,打開電爐并加熱反應管,此時活塞K1,K2,K3的狀態為____。
(2)試劑A為__,裝置單元X的作用是__;反應過程中需用熱源間歇性微熱連接管,其目的是___。
(3)反應結束后應繼續通入一段時間CO2,主要目的是___。
(4)將連接管切斷并熔封,采用蒸餾法提純。此時應將a端的儀器改裝為__、承接管和接收瓶,在防腐膠塞上加裝的儀器是___(填儀器名稱)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電解質溶液電導率越大導電能力越強。常溫下用0.100 mol·L-1鹽酸分別滴定10.00 mL濃度均為0.100 mol·L-1的NaOH溶液和氨水溶液。利用傳感器測得滴定過程中溶液的電導率如圖所示。下列說法正確的是

A. 曲線①代表滴定氫氧化鈉溶液的曲線
B. 滴定氨水的過程應該選擇酚酞作為指示劑
C. b點溶液中:c(H+)>c(OH-)+c(NH4+)+c(NH3·H2O)
D. a、b、c、d四點的溶液中,水的電離程度最大的是c點
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】FeCl2是一種常用的還原劑、媒染劑。某化學實驗小組在實驗室里用如下兩種方法來制備無水FeCl2。有關物質的性質如下:
C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 | |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯,易溶于乙醇,易吸水 | ||
熔點/℃ | -45 | 53 | 易升華 | |
沸點/℃ | 132 | 173 | ---------------------- | -------------------- |
(1)H2還原無水FeCl3制取FeCl2。有關裝置如圖:
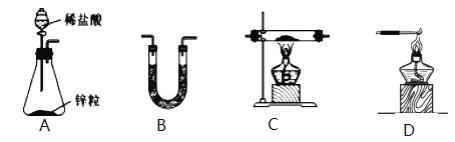
①H2還原無水FeCl3制取FeCl2的化學方程式為_____。
②按氣流由左到右的方向,上述儀器的連接順序為_____。(填字母,裝置可多次使用);B中盛放的試劑是_____。
③該制備裝置的缺點為_____。
(2)利用反應2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取無水FeCl2并測定FeCl3的轉化率。按如圖裝置,在三頸燒瓶中放入32.5g無水氯化鐵和過量的氯苯,控制反應溫度在一定范圍加熱3h,冷卻、分離提純得到粗產品。

①儀器a的作用是_____。
②反應結束后,冷卻實驗裝置A,將三頸燒瓶內物質倒出,經過濾、洗滌、干燥后,得到粗產品。洗滌所用的試劑可以是_____,回收濾液中C6H5C1的操作是_____。
③反應后將錐形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol/L NaOH溶液滴定,終點時消耗NaOH溶液為19.60mL,則氯化鐵的轉化率為_____。
④為了減少實驗誤差,在制取無水FeCl2過程中應采取的措施有:_____(寫出一點即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電爐加熱時用純氧氧化管內樣品,根據產物的質量確定有機物的組成,下列裝置是用燃燒法確定有機物分子式常用的裝置。
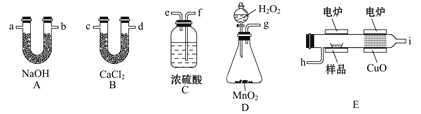
(1)產生的氧氣按從左到右的流向,所選裝置各導管的連接順序是___________。
(2)C裝置中濃H2SO4的作用是________。
(3)D裝置中MnO2的作用是_____________。
(4)燃燒管中CuO的作用是______________。
(5)若準確稱取0.90 g樣品(只含C、H、O三種元素中的兩種或三種),經充分燃燒后,A管質量增加1.32g,B管質量增加0.54 g,則該有機物的實驗式為_______。
(6)要確立該有機物的分子式,還要知道___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三草酸合鐵酸鉀K3[Fe(C2O4)3]·3H2O是一種翠綠色晶體,在日光下照射,會因感光而部分變深藍色,故常用于工程制圖,即“藍圖”。K3[Fe(C2O4)3]·3H2O的制備反應為:2FeC2O4·2H2O + H2O2 + 3K2C2O4 + H2C2O4 = 2K3[Fe(C2O4)3]·3H2O。
回答下列問題:
(1)上述氧化過程中,Fe(II)_____(答簡化電子排布式)變為Fe(III)______(答外圍電子排布圖),基態Fe(III)電子占據______個不同軌道。
(2)對上述反應式中的短周期元素按照電負性由小到大排序為______。
(3)配合物K3[Fe(C2O4)3]的配位數為6,其配體C2O42—中的C的雜化方式為____雜化。
(4) H2O2屬于______(填“極性”或“非極性”)分子。H2O2為二元弱酸,一級電離產物HO2—的立體構型是__________。H2O2沸點(150.2 ℃)比H2S沸點(-60.4 ℃)高,簡要解釋主要原因___________。
(5)將下列晶體的微粒配位數由大到小排序為________(填寫代號)
① 金剛石;② 金屬鉀;③ 干冰
(6)FeO的晶胞結構為NaCl型,測知FeO晶胞邊長為428pm,則此晶體中最近的Fe2+與Fe2+的距離為_________pm。(保留三位有效數字)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】麻黃素M是擬交感神經藥。合成M的一種路線如圖所示:
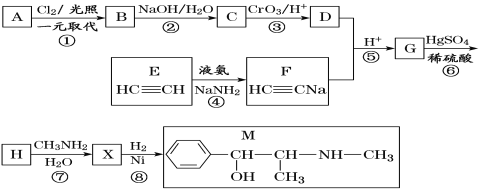
已知:I.R—CH2OH![]() RCHO
RCHO
II.R1-CHO+R-C≡CNa![]()
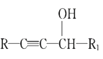
IV.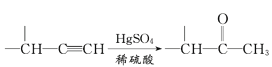
V.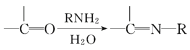
請回答下列問題:
(1)D的名稱是_______;G中含氧官能團的名稱是_______。
(2)反應②的反應類型為_______;A的結構簡式為_______。
(3)寫出反應⑦的化學方程式:______________________________。
(4)X分子中最多有_______個碳原子共平面。
(5)在H的同分異構體中,同時能發生水解反應和銀鏡反應的芳香族化合物中,核磁共振氫譜上有4組峰,且峰面積之比為1∶1∶2∶6的有機物的結構簡式為_________________。
(6)已知:![]() 仿照上述流程,設計以苯、乙醛為主要原料合成某藥物中間體
仿照上述流程,設計以苯、乙醛為主要原料合成某藥物中間體![]() 的路線________________。
的路線________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com