
【題目】在一定溫度下,下列敘述不是可逆反應:A(g)+3B(g)![]() 2C(g)達到平衡狀態標志的是( )
2C(g)達到平衡狀態標志的是( )
①C生成的速率與C分解的速率相等
②單位時間內生成a mol A,同時生成3a mol B
③A、B、C的濃度不再變化
④A的體積分數不再變化
⑤混合氣體的總壓強不再變化
⑥混合氣體的總物質的量不再變化
⑦單位時間內消耗a mol A,同時生成3a mol B
⑧A、B、C的分子數之比為1∶3∶2
A. ②⑧ B. ①⑥ C. ②④ D. ③⑧
【答案】A
【解析】
①C生成的速率相當于v(正),C分解的速率相當于v(逆),且v(正)= v(逆),可以判定反應達到平衡狀態,正確;
②單位時間內生成a mol A,同時生成3a mol B,反應速率同向,不能判斷反應是否達到平衡狀態,錯誤;
③A、B、C的濃度不再變化,可以判定反應達到平衡狀態,正確;
④A的體積分數不再變化,濃度保持不變,可以判定反應達到平衡狀態,正確;
⑤該反應為反應前后氣體體積發生變化的反應,當混合氣體的總壓強不再變化時,可以判定反應達到平衡狀態,正確;
⑥該反應中各物質均為氣體,反應前后氣體的總量發生變化,所以當混合氣體的總物質的量不再變化,可以判斷反應達到平衡狀態,正確;
⑦單位時間內消耗a mol A,相當于v(正),同時生成3a mol B ,相當于v(逆),且速率之比和系數成正比,因此可以判定反應達到平衡狀態,正確;
⑧平衡時各組成成分的含量不再改變,但不一定等于化學式前的系數之比,不能判斷反應是否達到平衡狀態,錯誤;
綜上所述,本題選A。


科目:高中化學 來源: 題型:
【題目】二氯亞砜(SOCl2)是一種無色易揮發液體,劇烈水解生成兩種氣體,常用作脫水劑,其熔點-105℃,沸點79℃,140℃以上時易分解。
(1)用硫黃(S)、液氯和三氧化硫為原料,在一定條件合成二氯亞砜,原子利用率達100%,則三者的物質的量比為______________________。
(2)甲同學設計如圖裝置用ZnCl2·xH2O晶體制取無水ZnCl2,回收剩余的SOCl2(夾持及加熱裝置略)
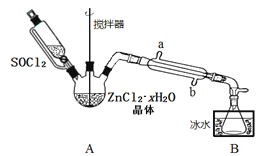
①SOCl2在該實驗中的作用_________________________________;加熱條件下,A裝置中總的化學方程式為_________________________________。
②實驗結束后,為檢測ZnCl2·xH2O晶體是否完全脫水,甲同學設計實驗方案如下,正確的實驗順序為___________(填序號)
a.干燥 b.洗滌; c加入足量硝酸酸化的硝酸銀溶液,充分反應;
d稱取蒸干后的固體m克溶于水;e.過濾; f稱得固體為n克
若m/n=___________(保留小數點后兩位),即可證明晶體已完全脫水。
(3)乙同學認為SOCl2還可用作由FeCl3·6H2O制取無水FeCl3的脫水劑,但丙同學認為該實驗可能發生副反應使最后的產品不純。
①可能發生的副反應的離子方程式_________________________________。
②丙同學設計了如下實驗方案判斷副反應的可能性:
i.取少量FeCl3·6H2O于試管中,加入足量SOCl2振蕩使兩種物質充分反應:
ii.往上述試管中加水溶解,取溶解后的溶液少許于兩支試管,進行實驗驗證,完成表格內容。
供選試劑:AgNO3溶液、稀鹽酸、稀HNO3、酸性KMnO4溶液、KSCN溶液、K3[Fe(CN)6]溶液、溴水)
方案 | 操作 | 現象 | 結論 |
方案一 | 往一支試管中滴加___________ | 若無明顯現象 | 則發生了上述副反應 |
方案二 | 往另一支試管中滴加___________ | ___________ | 則沒有發生上述副反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2017年4月,中國科學院長春應用化學研究所研究員張新波課題組提出并論證了基于反應6Li+N2![]() 2Li3N,通過Li-N2可充電電池直接利用空氣中的氮氣實現人工固氮的可能性。電Li-N2池的結構如圖所示,電解液為LiCF3SO3。下列說法正確的是
2Li3N,通過Li-N2可充電電池直接利用空氣中的氮氣實現人工固氮的可能性。電Li-N2池的結構如圖所示,電解液為LiCF3SO3。下列說法正確的是
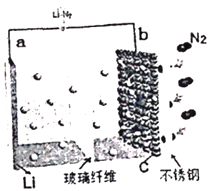
A. b極為電池的負極
B. 電池放電時Li+移向a極
C. b極的電極方程式為N2+6Li++6e- = 2Li3N
D. 金屬鋰在放電過程中發生還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】ClO2是一種殺菌消毒效率高、二次污染小的水處理劑。可通過以下反應制得:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O。有關該反應的說法正確的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O。有關該反應的說法正確的是( )
A. H2C2O4是還原劑B. KClO3在反應中失電子
C. KClO3被還原D. H2SO4發生氧化反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】取100mL的Na2CO3和Na2SO4混合溶液,加入適量Ba(OH)2溶液100 mL后,恰好完全反應,過濾、干燥后得到14.51g白色沉淀和濾液,再用過量稀硝酸處理沉淀,最后減少到4.66g,并有氣體放出。計算:
(1)求原混合液中Na2SO4的物質的量?__________________
(2)產生的氣體在標準狀況下的體積為多少?_________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在實驗室進行物質制備時,下列從原料及有關試劑分解制取相應的最終產物的設計中,理論上有錯誤或操作上不可行或經濟上不合理的是( )
A. FeFe2O3 ![]() Fe2(SO4)3溶液
Fe2(SO4)3溶液
B. C![]() CO
CO![]() CO2
CO2![]() Na2CO3溶液
Na2CO3溶液
C. CuO![]() CuSO4溶液
CuSO4溶液![]() Cu
Cu
D. CaO![]() Ca(OH)2溶液
Ca(OH)2溶液![]() NaOH溶液
NaOH溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列熱化學方程式中△H的含義表示正確的是
A. H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) △H(中和熱)
B. NaOH(aq)+![]() H2SO4(濃)=
H2SO4(濃)=![]() Na2SO4(aq)+H2O(l) △H(中和熱)
Na2SO4(aq)+H2O(l) △H(中和熱)
C. CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H(燃燒熱)
D. 2H2(g)+O2(g)=2H2O(g) △H(燃燒熱)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氧化還原反應在生產、生活中具有廣泛的用途,貫穿古今。
(1)下列生產、生活的事例中發生了氧化還原反應的_________。
A.用石斧解剖 B.早期的農業耕作
B.早期的農業耕作
C.簡單機械織布![]() D.祥云火炬燃燒
D.祥云火炬燃燒![]()
(2)水是人體的重要組成部分,是人體中含量最多的一種物質。“四種基本反應類型與氧化還原反應的關系”也可用如圖表達。
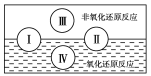
試寫出一個有水生成的屬于類型Ⅲ的化學方程式_________;
有水參加的反應:C+H2O(g)![]() CO+H2,符合圖中反應類型______(填標號)。
CO+H2,符合圖中反應類型______(填標號)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com