
化合物A最早發現于酸牛奶中,它是人體內糖代謝的中間體,可由馬鈴薯、玉米、淀粉等發酵制得。A的鈣鹽是人們喜愛的補鈣劑之一,A在某種催化劑存在下進行氧化,其產物不能發生銀鏡反應。在濃硫酸存在下,A可發生如下反應。

試寫出:
(1)化合物A、B、D的結構簡式:
A____________;B____________;D____________。
(2)化學方程式:A→E___________________ _____________________________________;
_____________________________________;
A→F_____________________________________________________________。
(3)反應類型:A→E____________;A→F____________。
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
下列有關電池的說法不正確的是( )
A.手機上用的鋰離子電池屬于二次電池
B.銅鋅原電池工作時,電子沿外電路從銅電極流向鋅電極
C.甲醇燃料電池可把化學能轉化為電能
D.鋅錳干電池中,鋅電極是負極
查看答案和解析>>
科目:高中化學 來源: 題型:
下列物質中,具有同分異構體的有( )
(1)C3H7Cl (2)C3H8 (3) CH2Cl2
A.(1)(3) B. (1) (2) C.只有(3) D.只有(1)
查看答案和解析>>
科目:高中化學 來源: 題型:
化學用語是學習化學的重要工具,下列用來表示物質變化的化學用語中,不正確的是
A.電解飽和食鹽水時,陽極的電極反應式為:2Cl --2e -= Cl2↑
B.氫氧燃料電池(堿性電解質)的正極反應式:O2 + 2H2O + 4e- = 4OH -
C.粗銅精煉時,與電源負極相連的是純銅,電極反應式為:Cu2+ + 2e- = Cu
D.鋼鐵發生電化學腐蝕的負極反應式:Fe-3e - = Fe3+
查看答案和解析>>
科目:高中化學 來源: 題型:
實驗室用乙酸、乙 醇、濃H2SO4制取乙酸乙酯,加熱蒸餾后,在飽和Na2CO3溶液的液面上得到無色油狀液體,當振蕩混合時,有氣泡產生,原因是( )。
醇、濃H2SO4制取乙酸乙酯,加熱蒸餾后,在飽和Na2CO3溶液的液面上得到無色油狀液體,當振蕩混合時,有氣泡產生,原因是( )。
A.產品中有被蒸餾出的H2SO4
B.有部分未反應的乙醇被蒸餾出來
C.有部分未反 應的乙酸被蒸餾出來
應的乙酸被蒸餾出來
D.有部分乙醇跟濃H2SO4作用生成乙烯
查看答案和解析>>
科目:高中化學 來源: 題型:
下列敘述Ⅰ和Ⅱ均正確并且有因果關系的是
| 選項 | 敘述I | 敘述II |
| A | NaHCO3能與堿反應 | NaHCO3用作糕點的膨松劑 |
| B | 實驗室常用MgSO4溶液與NaOH溶液制備Mg(OH)2沉淀 | Mg(OH)2不溶于強堿 |
| C | Cl2與Fe反應生成FeCl3 | 把FeCl3溶液直接蒸發結晶可以制備出FeCl3固體 |
| D | 銅絲與濃硫酸反應完,冷卻后向試管中加入水來觀察CuSO4溶液的藍色 | 銅與濃硫酸反應生成了CuSO4和SO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
硬質玻璃管是化學實驗中經常使用的一種儀器,請分析下列實驗(固定裝置略)并回答問題。
Ⅰ、下圖是某研究性學習小組對某鐵礦石中鐵的氧化物的化學式進行探究的流程和裝置。
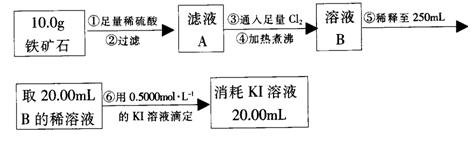
圖1
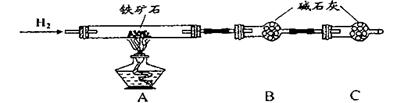
圖2
操作步驟如下:
a.按上圖2組裝儀器(夾持儀器均省略),檢查裝置的氣密性;
b.將5.0g鐵礦石放入硬質玻璃管中;
c.從左端導氣管口處不斷地緩緩通入H2,在C裝置出口處收集H2并 后,點燃A處酒精燈;
d.充分反應后,撤掉酒精燈,再持續通入氫氣至完全冷卻。
e.測得反應后裝置B增重1.35g。
回答下列問題:
(1)步驟c中填空為____________________________________________________
(2)圖1中步驟②和⑤中都要用到的玻璃儀器是______ __。
(3)下列有關圖1中步驟⑥的操作中說法不正確的是_________。
a.滴定管用蒸餾水洗滌后再用待裝液潤洗
b.錐形瓶不需要用待測液潤洗
c.因為碘水為黃色,所以滴定過程中不需加指示劑
(4)由以上實驗得出該鐵礦石中鐵的氧化物的化學式為_____________。
Ⅱ、硬質玻璃管進行微量實驗:如圖所示,將濃硫酸滴入裝有Na2SO3固體的培養皿一段時間后,a、b、c三個棉球變化如下表。
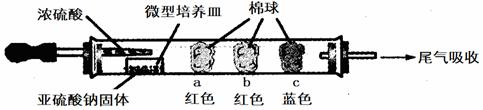
請填寫表中的空白:
| 棉球 | 棉球上滴加的試劑 | 實驗現象 | 解釋和結論 |
| a |
| 棉球變白,微熱后又恢復紅色 |
|
| b | 含酚酞的NaOH溶液 | 棉球變為白色 | 離子方程式:
|
| c |
| 棉球變為白色 | 結論:該氣體具有 性 |
查看答案和解析>>
科目:高中化學 來源: 題型:
下列是某化學研究性學習小組對某無色水樣成分的檢驗過程,已知該水樣中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO 、SO
、SO 、Cl-中的若干種離子,該小組同學取100 mL水樣進行實驗:向樣品中先滴加硝酸鋇溶液,再滴加1 mol·L-1硝酸,實驗過程中沉淀質量的變化如圖所示:
、Cl-中的若干種離子,該小組同學取100 mL水樣進行實驗:向樣品中先滴加硝酸鋇溶液,再滴加1 mol·L-1硝酸,實驗過程中沉淀質量的變化如圖所示:

(1)水樣中一定含有的陰離子是____________,其物質的量濃度之比為________。
(2)寫出BC段曲線所表示反應的離子方程式:________________________________。
(3)由B點到C點變化過程中消耗硝酸的體積為________。
(4)試根據實驗結果推測K+是否存在?____(填“是”或“否”);若存在,K+的物質的量濃度c(K+)的范圍是________________(若K+不存在,則不必回答)。
(5)設計簡單實驗驗證原水樣中可能存在的離子:_____________________________
________________________________________________________________________
________________________________________________________________________。(寫出實驗步驟、現象和結論)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com