
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源:2016-2017學年湖南省長沙市高二下學期第一次月考化學試卷(解析版) 題型:推斷題
據圖示填空。
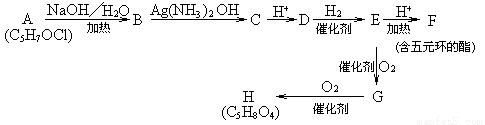
(1)寫出化合物B中含氧官能團的名稱___________。
(2)已知A中不存在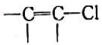 結構,則符合上述轉化關系的A物質可能有_____種(不考慮立體異構),任寫出其中一種A物質的結構簡式_____________。
結構,則符合上述轉化關系的A物質可能有_____種(不考慮立體異構),任寫出其中一種A物質的結構簡式_____________。
(3)根據(2)中所寫A的結構,寫出B→C反應的離子方程式:________________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南省益陽市高二下學期3月月考化學試卷(解析版) 題型:選擇題
下列變化中,由加成反應引起的是( )
A. 乙烯通入酸性高錳酸鉀溶液中,高錳酸鉀溶液褪色
B. 苯在一定溫度、壓強和催化劑的作用下和氫氣反應,生成環己烷
C. 一定條件下,苯滴入濃硝酸和濃硫酸的混合液中,有油狀物生成
D. 苯加入到溴水中,振蕩后溴水層褪色
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河南省漯河市高二3月月考化學試卷(解析版) 題型:選擇題
下列各組有機物中,不論二者以何種比例混合,只要總質量—定,完全燃燒時CO2的質量不變的是
①.CH4、C2H6 ②C3H6、C3H8 ③C2H4、C3H6O ④C2H4、C3H6
A. ①② B. ②③ C. ③④ D. ④
查看答案和解析>>
科目:高中化學 來源:2017屆四川省廣元市高三第二次高考適應性統考理綜化學試卷(解析版) 題型:簡答題
氰化鈉是一種重要的化工原料。泄漏時會導致環境污染,可以通過噴灑雙氧水或硫代硫酸鈉溶液來處理。
(1)NaCN的電子式為_______。
(2)NaCN與雙氧水反應為:NaCN+H2O2+H2O=NaHCO3+NH3↑,用H2O2處理1molNaCN時,反應中轉移電子的物質的量為______mol。
(3)NaCN也能被酸性高錳酸鉀溶液氧化,產生對大氣無污染的氣體和Mn2+,該反應的離子方程式是____________。
(4)某化學興趣小組在實驗室制備硫代硫酸鈉(Na2S2O3),并檢測用硫代硫酸鈉溶液處理后的氰化鈉廢水能否達標排放。
I.實驗室通過下圖裝置制備Na2S2O3。
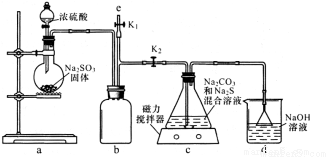
①裝置中盛濃硫酸的儀器是_____,b裝置的作用是________________。
②c裝置中的產物有Na2S2O3和CO2等,d裝置中的溶質有NaOH、Na2CO3,還可能有____________。
③實驗結束后,在e處最好連接盛NaOH溶液的容器,再________________(填具體操作),最防止拆除裝置時污染空氣。
Ⅱ.測定用硫代硫酸鈉溶液處理后的廢水中氰化鈉的含量。
已知:①廢水中氰化鈉的最高排放標準為0.50 mg/L。
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黃色,且CN-優先與Ag+反應。
③實驗如下:取15.00 mL處理后的氰化鈉廢水于錐形瓶中,并滴加幾滴KI溶液作指示劑,用1.000 ×10-4 mol/L的標準AgNO3溶液滴定,消耗AgNO3溶液的體積為1.50 mL。
④滴定終點的判斷方法是_______________。
(7)經計算處理后的廢水中NaCN的濃度為________mg/L(保留兩位小數),處理后的廢水是否達到排放標準____________(填“是”或“否”)。
查看答案和解析>>
科目:高中化學 來源:2017屆四川省廣元市高三第二次高考適應性統考理綜化學試卷(解析版) 題型:選擇題
化學與社會、生活密切相關。對下列現象或事實的解釋正確的選項是
選項 | 現象或事實 | 解釋 |
A | 臭氧能用于殺菌消毒 | 臭氧的還原性使細菌的蛋白質變性 |
B | 鐵能用于治療缺鐵性貧血 | 鐵能與鹽酸生成三氯化鐵 |
C | 過氧化鈉作呼吸面具中的供氧劑 | 過氧化鈉是強氧化劑,能氧化二氧化碳 |
D | 用浸有酸性高錳酸鉀的硅藻土作水果保鮮劑 | 高錳酸鉀能氧化水果釋放的催熟劑乙烯 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河南省高二下學期月考(一)化學試卷(解析版) 題型:選擇題
有關晶體的結構如下圖所示,下列說法中錯誤的是
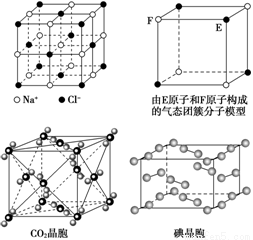
A.在NaCl晶體中,距Na+最近的Cl-形成正八面體
B.該氣態團簇分子的分子式為EF或FE
C.在CO2 晶體中,一個CO2 分子周圍有12個CO2 分子緊鄰
D.在碘晶體中,碘分子的排列有兩種不同的方向
查看答案和解析>>
科目:高中化學 來源:2017屆云南省高三下學期第一次統測理綜化學試卷(解析版) 題型:簡答題
中藥藥劑砒霜(主要成分As2O3,微溶于水)在醫療上用于治療急性白血病。某課題組以一種含砷精礦石粉(主要成份為As4S4、As2S3、FeS2及其它惰性雜質)為原料制取As2O3, 工藝流程簡圖如下:
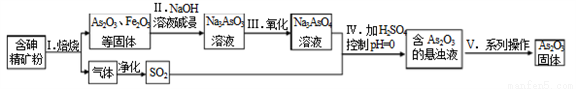
回答下列問題:
(1)過程I中所得SO2氣體可回收再利用,下列有關SO2用途的說法正確的是______。
A.工業制硫酸 B.漂白紙張 C.自來水消毒
(2)過程II中發生的反應______氧化還原反應(填“是”或“不是”)。
(3)過程V中系列操作為_______ (填化學實驗基本操作名稱)。
(4)①過程I中焙燒As2S3的化學反應方程式為_______________。
②過程IV中生成As2O3的離子反應方程式為_______________。
(5)有毒的AsO33-通過電解反應可轉化為無毒的AsO43-。用石墨為電極,在強堿性溶液中
電解含AsO33-的溶液,陽極的電極反應式為______________。
(6)測定某As2O3粗產品(含As2O5雜質)中As2O3的質量分數的實驗過程如下:
a.稱取m g粗產品溶解于NaOH溶液,得到含AsO33-、AsO43-的混合溶液l00mL。
b.分別移取25.00mL上述溶液,用0.02500 mol·L-1的I2標準溶液進行滴定(I2將AsO33-氧化為AsO43-,淀粉溶液為指示劑)。每次滴定開始時液面讀數如圖一所示,三次滴定結束時,I2標準溶液液面讀數如圖二〜圖四所示。
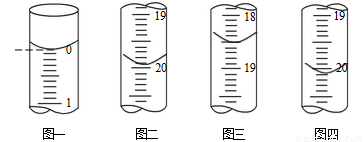
①描述滴定終點的現象_____________________。
②粗產品中As2O3的質量分數為______________ (用含有m的代數式表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com