
分析 根據n=$\frac{V}{{V}_{m}}$計算氫氣的物質的量,再根據反應2Na+2H2O=2NaOH+H2↑計算樣品中Na的質量,進而計算Na2O的質量,根據Na2O中元素質量分數計算含有Na元素的質量,最后根據總質量計算出鈉元素的質量分數.
解答 解:生成的氣體為氫氣,其物質的量為:n(H2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,
2Na+2H2O=2NaOH+H2↑
46g 1mol
m(Na) 0.1mol
m(Na)=$\frac{46g×0.1mol}{1mol}$=4.6g,
故10.8g樣品中含有氧化鈉的質量為:m(Na2O)=10.8g-4.6g=6.2g,
Na2O中Na元素的質量為:6.2g×$\frac{46}{62}$=4.6g,
所以樣品中鈉元素的質量分數為:$\frac{4.6g+4.6g}{10.8g}$×100%≈85.2%,
答:該樣品中鈉元素的質量分數為85.2%.
點評 本題考查了化學方程式的有關計算,題目難度中等,明確發生反應的原理為解答關鍵,注意掌握質量守恒在化學計算中的應用,試題培養了學生的分析能力及靈活應用能力.


科目:高中化學 來源: 題型:多選題
| A. | c ( NH4+)+c ( Na+)=c ( Cl-)+c ( OH-) | |
| B. | c ( NH4+)+c ( NH3•H2O )=0.4mol/L | |
| C. | c ( Cl-)>c ( NH4+)>c ( Na+)>c ( OH-)>c ( H+) | |
| D. | c ( Cl-)>c ( Na+)>c ( NH4+)>c ( H+ )>c ( OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 甲 | 乙 | 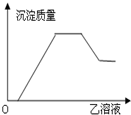 | |
| A | AlCl3、Mg(NO3)2、HNO3 | NaOH | |
| B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 | |
| C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH | |
| D | NaAlO2、氨水、NaOH | H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C60的摩爾質量是720 | |
| B. | 金剛石、石墨和C60互為同位素 | |
| C. | 因石墨具有導電性,可用石墨炸彈破壞輸電線、電廠設備 | |
| D. | 在點燃的條件下,碳可以還原氧化鎂生成鎂和二氧化碳 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 33.3% | B. | 40% | C. | 60% | D. | 75% |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 2NH3+3CuO→3Cu+N2+3H2O | B. | 2Na+2NH3→2NaNH2+H2↑ | ||
| C. | 4NH3+6NO→5N2+6H2O | D. | 3SiH4+4NH3→Si3N4+12H2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com