
【題目】一種雙電子介體電化學生物傳感器,用于檢測水體急性生物毒性,其工作原理如圖。下列說法正確的是( )
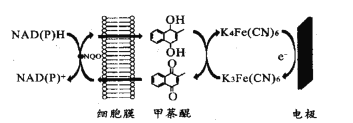
A.圖中所示電極為陽極,其電極反應式為K4Fe(CN6)-e-=K3Fe(CN)6
B.甲荼醌在陰極發生氧化反應
C.工作時K+向圖中所示電極移動
D.NAD(P)H轉化為NAD(P)+的過程失去電子
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】50 mL 0.50 mol·L-1鹽酸與50 mL 0.55 mol·L-1 NaOH溶液在如圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量可計算中和熱。回答下列問題:
(1)從實驗裝置上看,圖中尚缺少的一種玻璃儀器是________。燒杯間填滿碎泡沫塑料的作用是________

(2)大燒杯上如不蓋硬紙板,求得的中和熱數值_______ (填“偏大”、“偏小”或“無影響”)。
(3)實驗中改用60 mL 0.50 mol·L-1鹽酸與50 mL 0.55 mol·L-1 NaOH溶液進行反應,與上述實驗相比,所放出的熱量__________(填“相等”或“不相等”),所求中和熱__________(填“相等”或“不相等”),
(4)用相同濃度和體積的氨水代替NaOH溶液進行上述實驗,測得的中和熱的數值會_____(填“偏大”“偏小”或“無影響”)。
(5)寫出該反應的熱化學方程式:____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】坦桑石的主要化學成分為Ca2Al3(SiO4)3(OH),還可含有V、Cr、Mn等元素。
(1)下列狀態中的鋁微粒,電離最外層的一個電子所需能量最大的是____________。
①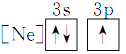 ②
②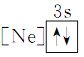 ③
③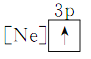 ④
④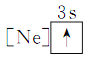
(2)煙酸鉻是鉻的一種化合物,其合成過程如下:
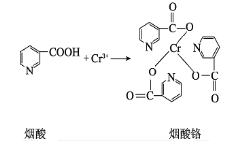
①Cr原子的價層電子排布圖為 _______________。這樣排布電子遵循的原則是 ______________。
②煙酸中所含元素的第一電離能I1(N)_____ I1(O),原因是_________________ 。
③煙酸中碳、氮原子的雜化方式分別為 _________________、__________________。
(3)SiCl4、SiF4都極易水解。二者都屬于______(填“極性”或“非極性”)分子,其熔點關系為SiF4 ______SiCl4(填“>”“<”或“=”)。
(4)將Mn摻入GaAs晶體(圖甲)可得到稀磁性半導體材料(圖乙),圖甲、圖乙晶體結構不變。
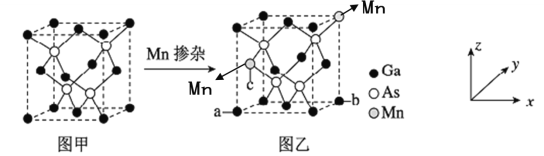
①圖乙中a點和b點的原子坐標參數分別為(0,0,0)和(1,1,0),則c點的原子坐標參數為_______。
②設圖甲晶體的密度為ρg·cm-3,用NA表示阿伏伽德羅常數的數值,則該晶胞中距離最近的兩個砷原子之間的距離為 ___________ pm。(用含ρ、NA的關系式表示最簡化的計算式即可)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】煙氣脫硫能有效減少二氧化硫的排放。實驗室用粉煤灰(主要含Al2O3、SiO2等)制備堿式硫酸鋁[Al2(SO4)3·Al2O3]溶液,并用于煙氣脫硫研究。
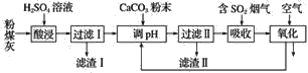
(1)酸浸時反應的化學方程式為_______________________________________________;濾渣Ⅰ的主要成分為________(填化學式)。
(2)濾渣Ⅱ的主要成分為________(填化學式);制備堿式硫酸鋁[Al2(SO4)3·Al2O3]溶液的化學方程式為_________________________________________________________________。
(3)吸收煙氣中SO2的化學方程式為Al2(SO4)3·Al2O3+3SO2=Al2(SO4)3·Al2(SO3)3。通入空氣氧化,發生反應的化學方程式為_______________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)鐵元素的原子結構示意圖為________;它在周期表中的位置是_________。
(2)某煉銅反應為:![]() 上述反應中,氧化劑是________;若反應中轉移15 mol電子,則氧化產物的質量為___________。
上述反應中,氧化劑是________;若反應中轉移15 mol電子,則氧化產物的質量為___________。
(3)氧和硫分別形成的氫化物中比較穩定的是________(寫電子式)。
(4)與明礬相似,![]() 也可用作凈水劑,其凈水的原理是_________。
也可用作凈水劑,其凈水的原理是_________。
(5)![]() 又稱摩爾鹽,它可作凈水劑,還用作化學試劑、醫藥、冶金、電鍍等,請你設計實驗檢驗摩爾鹽中的有色陽離子:_________________。
又稱摩爾鹽,它可作凈水劑,還用作化學試劑、醫藥、冶金、電鍍等,請你設計實驗檢驗摩爾鹽中的有色陽離子:_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙烯、環氧乙院是重要的化工原料,用途廣泛。回答下列問題:
已知:I.2CH2=CH2(g)+O2(g)![]() 2
2![]() (g) △H1=-206.6kJmo1-1
(g) △H1=-206.6kJmo1-1
II.CH2=CH2(g)+3O2(g)=2CO2(g)+2H2O(1) △H2
III.2![]() (g)+5O2(g)=4CO2(g)+4H2O(1) △H3
(g)+5O2(g)=4CO2(g)+4H2O(1) △H3
(1)反應III:△S(填“>”“<”或“=”)___0。
(2)熱值是表示單位質量的燃料完全燃燒時所放出的熱量,是燃料質量的一種重要指標。已知乙烯的熱值為50.4kJg-1,則△H3=___kJmol-1
(3)實驗測得2CH2=CH2(g)+O2(g)![]() 2
2![]() (g)中,v逆=k逆c2(
(g)中,v逆=k逆c2(![]() ),v正=k正c2(CH2=CH2)c(O2)(k正、k逆為速率常數,只與溫度有關)。
),v正=k正c2(CH2=CH2)c(O2)(k正、k逆為速率常數,只與溫度有關)。
①反應達到平衡后,僅降低溫度,下列說法正確的是(________)
A.k正、k逆均增大,且k正增大的倍數更多
B.k正、k逆勻減小,且k正減小的倍數更少
C.k正增大、k逆減小,平衡正向移動
D.k正、k逆均減小,且k逆減小的倍數更少
②若在1L的密閉容器中充入1molCH2=CH2(g)和1molO2(g),在一定溫度下只發生反應I,經過10min反應達到平衡,體系的壓強變為原來的0.875倍,則0~10min內v(O2)=___,![]() =___。
=___。
(4)現代制備乙烯常用乙烷氧化裂解法:
C2H6(g)+![]() O2(g)=C2H4(g)+H2O(g) △H2=-110kJmol-1,反應中還存在CH4、CO、CO2等副產物(副反應均為放熱反應),圖1為溫度對乙烷氧化裂解反應性能的影響。
O2(g)=C2H4(g)+H2O(g) △H2=-110kJmol-1,反應中還存在CH4、CO、CO2等副產物(副反應均為放熱反應),圖1為溫度對乙烷氧化裂解反應性能的影響。
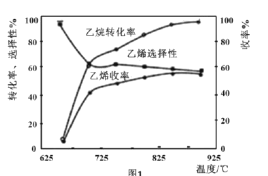
①乙烷的轉化率隨溫度的升高而升高的原因是___;反應的最佳溫度為___(填序號)。
A.650℃ B.700℃ C.850℃ D.900℃
[乙烯選擇性=![]() ;乙烯收率=乙烷轉化率×乙烯選擇性]
;乙烯收率=乙烷轉化率×乙烯選擇性]
②工業上,保持體系總壓恒定為l00kPa的條件下進行該反應,通常在乙烷和氧氣的混合氣體中摻混惰性氣體(惰性氣體的體積分數為70%),摻混惰性氣體的目的是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】次硫酸氫鈉甲醛(aNaHSO2bHCHOcH2O)在印染、醫藥以及原子能工業中應用廣泛。以Na2SO3、SO2、HCHO和鋅粉為原料制備次硫酸氫鈉甲醛的實驗步驟如下:

步驟1:在如圖所示裝置的燒瓶中加入一定量Na2SO3和水,攪拌溶解,緩慢通入SO2,至溶液pH約為4,制得NaHSO3溶液。
步驟2:將裝置A中導氣管換成橡皮塞。向燒瓶中加入稍過量的鋅粉和一定量甲醛溶液,在80~90℃下,反應約3h,冷卻至室溫,抽濾。
步驟3:將濾液真空蒸發濃縮,冷卻結晶。
(1)裝置B的燒杯中應加入的溶液是___。
(2)步驟2中加入鋅粉時有NaHSO2和Zn(OH)2生成。
①寫出加入鋅粉時發生反應的化學方程式:___。
②生成的Zn(OH)2會覆蓋在鋅粉表面阻止反應進行,防止該現象發生的措施是___。
(3)冷凝管中回流的主要物質除H2O外,還有___(填化學式)。
(4)步驟3中次硫酸氫鈉甲醛不在敞口容器中蒸發濃縮的原因是___。
(5)步驟2抽濾所得濾渣的成分為Zn和Zn(OH)2,利用濾渣制備ZnO的實驗步驟為:將濾渣置于燒杯中,___,900℃煅燒。(已知:Zn與鋁類似,能與NaOH溶液反應;Zn2+開始沉淀的pH為5.9,沉淀完全的pH為8.9,pH>11時,Zn(OH)2能生成ZnO22-。實驗中須使用的試劑有1.0molL-1NaOH溶液、1.0molL-1HCl溶液、水)
(6)產物組成測定實驗:
準確稱取1.5400g樣品,溶于水配成l00mL溶液;取25.00mL樣品溶液經AHMT分光光度法測得溶液吸光度A=0.4000(如圖);另取25.00mL樣品溶液,加入過量碘水后,加入BaCl2溶液至沉淀完全,過濾、洗滌、干燥至恒重得到BaSO4固體0.5825g。
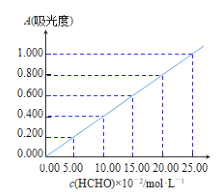
①樣品溶液HCHO濃度為___molL-1。
②通過計算確定aNaHSO2·bHCHOcH2O的化學式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,醋酸的電離常數為1.8×10-5。向20mL2.0mol/LCH3COOH溶液中逐滴加入2.0mol/LNaOH溶液,溶液中水電離出的c(H+)在此滴定過程中變化曲線如圖所示。下列說法正確的是( )
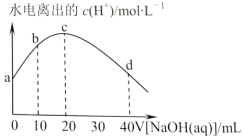
A.a點水電離出的c(H+)=6.0×10-3mol/L
B.b點c(CH3COOH)>c(Na+)>c(CH3COO-)
C.c點恰好完全反應,溶液中無CH3COOH
D.d點c(Na+)=2c(CH3COO-)+2c(CH3COOH)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,則下列難溶鹽的飽和溶液中,Ag+濃度大小順序正確的是( )
A. AgCl>AgI>Ag2CrO4 B. AgCl>Ag2CrO4>AgI
C. Ag2CrO4>AgCl>AgI D. Ag2CrO4>AgI>AgCl
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com