

| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 開始沉淀時的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全時的pH | 9.0 | 4.0 | 5 | 11 |
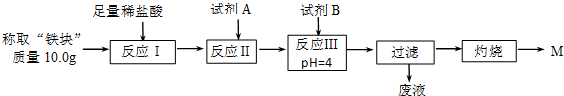
分析 (1)①取反應后的“鐵塊”研碎取樣稱量,加入如圖2裝置滴入足量NaOH溶液充分反應,測量生成氣體體積,可以計算得到反應的鋁的物質的量,得到鐵塊中鋁的含量;
②量氣管的量具部分底部是連接橡膠管,結合實驗量具可知是堿式滴定管的部分結構;
③對量氣管讀數時,首先等實驗裝置恢復到室溫再進行下一步操作,然后調節量氣管使左右液面相平,最后讀數時視線與凹液面最低處相平;
④裝置使用分液漏斗,隨液體流下錐形瓶中壓強增大,在排液過程中會排出的液體增多,導致測定結果偏高;
(2)①根據題意可知,本實驗要定量檢測所得“鐵塊”的成分,故要通過實驗流程,將鐵元素完全沉淀;而根據表格可知,要使鐵元素完全沉淀而鋁和鎂不沉淀,需將Fe2+轉化為Fe3+,然后沉淀.
②灼燒完全的標志是物質前后兩次灼燒質量相差不大于0.1g;
③根據10.0g的鐵塊中的鐵元素最終全到了最終紅色粉未M中,根據鐵原子的守恒來計算;如果對所得過濾固體直接洗滌、烘干、稱量,計算“鐵塊”的純度.
解答 解:(1)①取磁性氧化鐵在如圖1實驗裝置進行鋁熱反應,冷卻后得到“鐵塊”混合物,取反應后的“鐵塊”研碎取樣稱量,加入如圖2裝置滴入足量NaOH溶液充分反應,測量生成氣體體積,可以計算得到反應的鋁的物質的量,得到鐵塊中鋁的含量,該實驗的實驗目的是:測量樣品中鋁的含量;
故答案為:鋁;
②量氣管的量具部分底部是連接橡膠管,結合實驗量具可知是堿式滴定管的部分結構,所以該儀器的名稱為堿式滴定管,故答案為:堿式滴定管;
③根據PV=nRT,為保證測出來的氣體體積是當時大氣壓下的體積,在讀數時應注意:①將實驗裝置恢復到室溫,②使量氣管兩端液面相平,因為相平說明兩邊液面上的壓強是一樣的,這樣測出來的氣體體積才是當時大氣壓下的體積,③視線與凹液面最低處相平,俯視或仰視會造成誤差,量氣管在讀數時調節左右管液面相平之前的步驟是恢復到室溫;
故答案為:恢復到室溫;
④滴液漏斗可以平衡壓強讓液體順利滴入錐形瓶之外還可以起到降低實驗誤差的作用,如果裝置使用分液漏斗,隨液體流下錐形瓶中壓強增大,錐形瓶中排出液體增多,測量出的該物質百分含量將會偏大,
故答案為:偏大;
(3)①根據表格可知,要使鐵元素完全沉淀而鋁離子和鎂離子不沉淀,需將Fe2+轉化為Fe3+,故需要加入H2O2;然后調節4≤pH<4.2即可將Fe3+沉淀而Al3+、Mg2+不沉淀,調節pH選用的試劑不能用氧化鐵,因為會引起紅色粉未M的質量偏大;也不能用MgCO3固體,因為MgCO3固體過量時會引起所得固體M則質量偏大,故應選用氨水,故答案為:C;D;
②灼燒完全的標志是物質前后兩次灼燒質量相差不大于0.1g,故答案為:前后兩次灼燒質量相差不大于0.1g;
③最終紅色粉未M為Fe2O3,根據10.0g的鐵塊中的鐵元素最終全到了12.0gFe2O3中,故鐵原子的質量為:m(Fe)=$\frac{12.0g}{160g/mol}$×2×56gmol=8.4g,故該“鐵塊”的純度=$\frac{8.4g}{10.0g}$×100%=84%,故答案為:84%.
點評 本題綜合考查了鋁熱反應以及亞鐵離子向三價鐵離子的轉化以及離子的沉淀,主要是實驗過程分析判斷,含量的計算適用于,綜合性較強,難度較大.


 文敬圖書課時先鋒系列答案
文敬圖書課時先鋒系列答案科目:高中化學 來源: 題型:選擇題
| A. | 化學反應的過程,本質上是舊化學鍵斷裂和新化學鍵形成的過程 | |
| B. | 化學鍵可以使離子相結合,也可以使原子相結合 | |
| C. | 原子中核外電子排布的周期性變化是產生元素周期律的根本原因 | |
| D. | 核素就是同位素 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
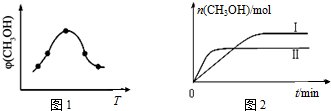
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
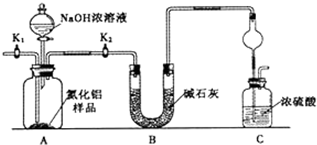
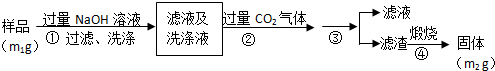
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 N和B元素及其化合物在工農生產中有很重要的應用.
N和B元素及其化合物在工農生產中有很重要的應用.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com