
【題目】在一個不傳熱的固定容積的密閉容器中,可逆反應mA(g)+nB(g)![]() pC(g)+qD(g),當m、n、p、q為任意整數時,一定達到平衡的標志是( )
pC(g)+qD(g),當m、n、p、q為任意整數時,一定達到平衡的標志是( )
①體系的溫度不再改變 ②體系密度不再改變
③各組分的濃度不再改變 ④各組分的質量分數不再改變
⑤反應速率v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q
⑥單位時間內m mol A發生斷鍵反應,同時p mol C也發生斷鍵反應
A.③④⑤⑥B.①③④⑥C.②③④⑥D.①③④⑤
【答案】B
【解析】
①體系的溫度不再改變,正、逆反應速率相等,能據此判斷該反應達到平衡狀態,①正確;
②反應混合物都是氣體,反應在恒容密閉容器內進行,容器的容積不變,因此無論反應是否達到平衡,混合氣體的密度一直不變,不能據此判斷反應是否處于平衡狀態,②錯誤;
③各組分的物質的量濃度不再改變,該反應達到平衡狀態,③正確;
④當該反應達到平衡狀態,各組分的質量分數不再改變,④正確;
⑤當反應速率vA:vB:vC:vD=m:n:p:q,由于未指明是正反應速率還是逆反應速率,所以不能據此判斷該反應是否達到平衡狀態,⑤錯誤;
⑥單位時間內m mol A斷鍵反應等效于pmol C形成,同時pmol C也斷鍵反應,說明任何物質的濃度不變,反應處于平衡狀態,⑥正確;
綜上所述可知,說法正確的是①③④⑥,故合理選項是B。


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:
【題目】實驗室合成乙酸乙酯的步驟如下:在圓底燒瓶內加入乙醇、濃硫酸和乙酸,瓶口豎直安裝通有冷卻水的冷凝管(使反應混合物的蒸氣冷凝為液體流回燒瓶內),加熱回流一段時間后換成蒸餾裝置進行蒸餾(如圖1所示),得到含有乙醇、乙酸和水的乙酸乙酯粗產品。請回答下列問題:(已知:乙醇、乙酸、乙酸乙酯的沸點依次是78.4℃、118℃、77.1℃)
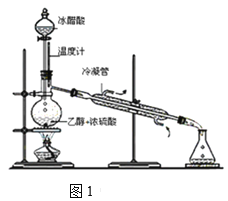
(1)在燒瓶中除了加入乙醇、濃硫酸和乙酸外,還應放入幾塊碎瓷片,其目的是__;
(2)現擬分離含乙酸、乙醇和水的乙酸乙酯粗產品,如圖2所示是分離操作步驟流程圖。
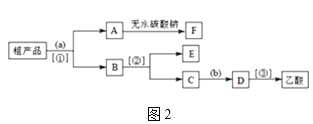
試劑a是__,分離方法①是__;分離方法②是__,試劑b是__;
(3)寫出C→D反應的化學方程式___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在密閉容器中,一定條件下進行如下反應2NO(g)+2CO(g)![]() N2(g)+2CO2(g),△H=-373.2kJ·mol-1,達到平衡后,為提高該反應的速率和NO的轉化率,采取的正確措施是( )
N2(g)+2CO2(g),△H=-373.2kJ·mol-1,達到平衡后,為提高該反應的速率和NO的轉化率,采取的正確措施是( )
A.加催化劑同時升高溫度B.加催化劑同時增大壓強
C.升高溫度同時充入N2D.降低溫度同時增大壓強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨氣具有還原性,能夠被氧化銅氧化,用如圖中的裝置可以實現該反應。已知氨可以與灼熱的氧化銅反應得到氮氣和金屬銅。回答下列問題:
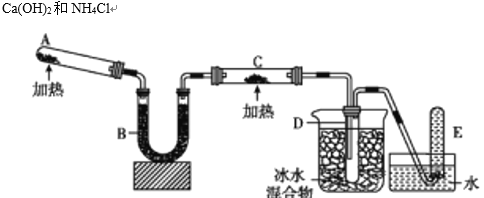
(1)寫出A中反應方程式:________________。
(2)寫出氨氣與灼熱氧化銅的反應方程式:________________。
(3)B中加入的干燥劑是________(填序號)
①濃硫酸 ②無水氯化鈣 ③堿石灰
(4)能證明氨與氧化銅反應的現象是C中________。
(5)D中有無色液體生成。檢驗D中無色液體的成分時會用到下列哪一種藥品________(填序號)
A.![]() B.
B.![]() C.無水硫酸銅
C.無水硫酸銅
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】a、b、c、d、e五種短周期元素的原子序數逐漸增大。a為非金屬元素且原子半徑最小,e為金屬,且a、e同主族,c、d為同周期的相鄰元素。e原子的質子數等于c、d原子最外層電子數之和。b原子最外層電子數是內層電子數的2倍。c的氣態氫化物分子中有3個共價鍵。試推斷:
(1)寫出d元素在周期表中的位置________。
(2)c的單質的分子式為________。
(3)d元素有兩種同素異形體,寫出其中有氣味的一種的分子式________。
(4)b的最簡單氣態氫化物的結構式是________。
(5)d和e組成的常見化合物是淡黃色固體,寫出該化合物電子式________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】水的電離平衡曲線如圖所示,下列說法正確的是
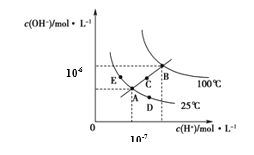
A.圖中五點KW間的關系:B>C>A=D=E
B.若從A點到C點,可采用溫度不變時在水中加入適量H2SO4 的方法
C.若從A點到D點,可采用在水中加入少量NaOH的方法
D.若處在B點溫度時,將pH=2的硫酸與pH=12的KOH等體積混合后,溶液顯中性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物Y具有抗菌、消炎作用,可由X制得。
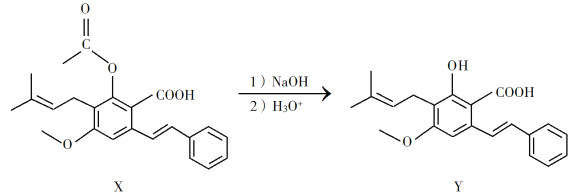
下列有關化合物X、Y的說法正確的是
A. 1 mol X最多能與2 mol NaOH反應
B. Y與乙醇發生酯化反應可得到X
C. X、Y均能與酸性KMnO4溶液反應
D. 室溫下X、Y分別與足量Br2加成的產物分子中手性碳原子數目相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應的離子方程式書寫正確的是( )
A. 鋁粉投入NaOH溶液中:2Al+2OH-===2AlO2-+H2↑
B. Na與CuSO4溶液反應:Cu2++2Na===2Na++Cu
C. 向AlCl3溶液中加入足量的氨水:Al3++3OH-===Al(OH)3↓
D. Ba(OH)2溶液與稀硫酸反應:Ba2++2OH-+2H++SO42-===BaSO4↓+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,下列有關溶液的說法正確的是( )
A.NaHCO3溶液加水稀釋,c(Na+)與c(HCO3-)的比值將減小
B.pH=1的一元酸和pH=13的一元堿等體積混合后溶液不一定呈中性
C.0.1mol/L硫酸銨溶液中:![]()
D.0.1mol/L的硫化鈉溶液中:![]()
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com