
| A. | 藍色逐漸消失的原因是Na2SO3溶液具有漂白性 | |
| B. | 第一步反應的離子方程式ClO-+2I-+2H+═I2+Cl-+H2O | |
| C. | 淀粉KI溶液變藍是因為I-被氧化為I2,I2使淀粉變藍色 | |
| D. | 微粒的氧化性由強到弱的順序是ClO->I2>SO${\;}_{4}^{2-}$ |
分析 第一步中發生:NaClO+2KI+H2SO4═I2+NaCl+K2SO4+H2O,第二步發生:Na2SO3+I2+H2O═Na2SO4+2HI,均為氧化還原反應,結合物質的性質及氧化劑的氧化性大于氧化產物的氧化性來解答.
解答 解:A.由第二步反應可知,S元素的化合價升高,則藍色消失的原因是Na2SO3溶液具有還原性,故A錯誤;
B.由第一步反應可知,淀粉KI溶液變藍是因為I-被氧化為I2,淀粉遇I2變藍,所以反應的方程式為:ClO-+2I-+2H+═I2+Cl-+H2O,故B正確;
C.由第一步反應可知,淀粉KI溶液變藍是因為I-被氧化為I2,淀粉遇I2變藍,故C正確;
D.由NaClO+2KI+H2SO4═I2+NaCl+K2SO4+H2O,ClO-的氧化性大于I2的氧化性,由Na2SO3+I2+H2O═Na2SO4+2HI,I2的氧化性大于SO4 2-的氧化性,所以氧化性強弱為:ClO->I2>SO42-,故D正確;
故選:A.
點評 本題以鹵族元素及化合物的性質考查氧化還原反應,把握發生的化學反應為解答的關鍵,注意利用氧化還原反應中的規律性知識來解答,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | Na2O2是堿性氧化物,SO2是酸性氧化物 | |
| B. | 分別加熱用Cl2、SO2和Na2O2漂白過的品紅溶液都能恢復紅色 | |
| C. | 將Cl2和SO2同時通入水中能生成兩種強電解質 | |
| D. | Cl2、SO2和Na2O2漂白原理相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
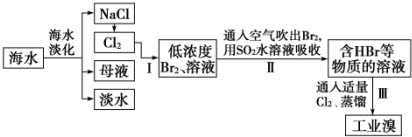
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | +6 | B. | +3 | C. | +2 | D. | 0 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
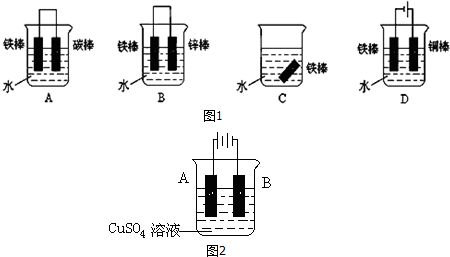
 Ⅰ.按圖裝置進行實驗,并回答下列問題.
Ⅰ.按圖裝置進行實驗,并回答下列問題. Ⅱ.(1)電工經常說的一句口頭禪:“銅接鋁,瞎糊弄”,所以電工操作上規定不能把銅導線與鋁導線連接在一起使用,說明原因:銅與鋁連接會構成原電池,其中鋁為原電池的負極,銅為原電池的正極.構成原電池后,鋁的腐蝕速度大大加快,電阻增大,放熱增多,時間長了,有可能引發火災.
Ⅱ.(1)電工經常說的一句口頭禪:“銅接鋁,瞎糊弄”,所以電工操作上規定不能把銅導線與鋁導線連接在一起使用,說明原因:銅與鋁連接會構成原電池,其中鋁為原電池的負極,銅為原電池的正極.構成原電池后,鋁的腐蝕速度大大加快,電阻增大,放熱增多,時間長了,有可能引發火災.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
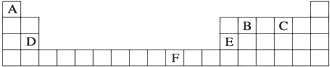
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1molCl2和足量的鐵加熱條件下反應,轉移電子數一定為3NA | |
| B. | 常溫常壓下,8.8g CO2和N2O的混合氣體所含電子數為4.4 NA | |
| C. | 常溫下,PH=13的Ba(OH)2 溶液,0.1L,含OH-,0.02NA | |
| D. | 1 L 1 mol/L的乙醇水溶液中含有氫原子總數為6NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com