
【題目】如圖為教科書中電解飽和食鹽水的實驗裝置.據此,下列敘述不正確的是( ) 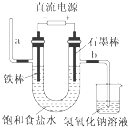
A.裝置中,a管能產生氫氣
B.在石墨棒電極區域有NaOH產物
C.b管導出的是氯氣
D.以食鹽水為基礎原料制取氯氣等產品的工業稱為“氯堿工業”
科目:高中化學 來源: 題型:
【題目】將一定量氨基甲酸銨(NH2COONH4)加入密閉容器中,在一定條件下發生下列反應:NH2COONH4(s) ![]() 2NH3(g)+CO2(g)。該反應的平衡常數的負對數(-lgK)值隨溫度(T)的變化曲線如圖所示,下列說法錯誤的是
2NH3(g)+CO2(g)。該反應的平衡常數的負對數(-lgK)值隨溫度(T)的變化曲線如圖所示,下列說法錯誤的是

A. 該反應的△H>0
B. NH3的體積分數不變時,該反應不一定達到平衡狀態
C. 恒溫恒容,A點時通入CO2,v(正)和v(逆)均增加
D. 30℃時,B點對應狀態的v(正)<v(逆)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電子工業是國民經濟支柱產業之一,也是新興科學技術發展產業.曾經電子工業常用質量分數為30%的FeCl3溶液腐蝕敷有銅箔的絕緣板,制成印刷線路板,發生反應的化學方程式為:2FeCl3+Cu═2FeCl2+CuCl2 .
(1)檢驗腐蝕后的溶液中是否含有Fe3+ , 應選用的試劑是 .
(2)為了從使用過的腐蝕廢液中回收銅,并重新制得純凈的FeCl3溶液,采用如圖所示實驗步驟.請在各空格內填上適當的化學式以使實驗達到預期目的.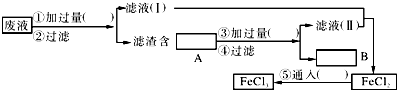
(3)寫出有關化學反應的離子方程式: .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于反應3Cl2+6NaOH ![]() 5NaCl+NaClO3+3H2O,以下敘述正確的是( )
5NaCl+NaClO3+3H2O,以下敘述正確的是( )
A.Cl2是氧化劑,NaOH是還原劑
B.被氧化的氯原子和被還原的氯原子的物質的量之比為5:1
C.Cl2既做氧化劑又做還原劑
D.氧化劑得電子數與還原劑失電子數之比為5:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室需要配制0.1mol/LNaOH溶液480mL,下列敘述正確的是( )
A.需要用托盤天平稱量NaOH固體的質量為1.92g
B.將NaOH固體在小燒杯中加水溶解后立即倒入容量瓶中并進行定容
C.在容量瓶中定容時俯視容量瓶刻度線會使溶液濃度偏高
D.定容后塞上瓶塞反復搖勻,靜置后,液面不到刻度線,再加水至刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,將4molPCl3和2molCl2充入容積不變的密閉容器中,在一定條件下反應:PCl3+Cl2PCl5 , 各物質均為氣態.達平衡后,PCl5為0.8mol.若此時再移走2molPCl3和1molCl2 , 相同溫度下達到平衡,PCl5的物質的量為( )
A.0.8mol
B.0.4mol
C.0.4mol<x<0.8mol
D.<0.4mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】四氯化錫是無色液體,熔點﹣33℃,沸點114℃.氯氣與金屬錫在加熱時反應可以用來制備SnCl4 , SnCl4極易水解,在潮濕的空氣中發煙.實驗室可以通過圖裝置制備少量SnCl4 (夾持裝置略). 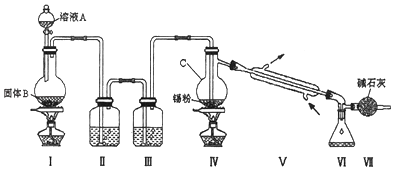
(1)儀器C的名稱為:;
(2)裝置Ⅰ中發生反應的離子方程式為:;
(3)裝置Ⅱ中的最佳試劑為 , 裝置Ⅶ的作用為;
(4)若裝置連接順序為Ⅰ﹣Ⅱ一Ⅳ一Ⅴ一Ⅵ一Ⅶ,在Ⅳ中除生成SnCl4外,還會生成的含錫的化合物的化學式為 .
(5)Ⅳ中加熱的作用之一是促進氯氣與錫粉反應,加熱的另一作用為;
(6)若Ⅳ中用去錫粉11.9g,反應后,Ⅵ中錐形瓶里收集到23.8g SnCl4 , 則SnCl4的產率為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上常利用含硫廢水生產Na2S2O35H2O,實驗室可用如下裝置(略去部分加持儀器)模擬生成過程.
燒瓶C中發生反應如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq) ![]() Na2S2O3(aq) (Ⅲ)
Na2S2O3(aq) (Ⅲ)
(1)裝置A中發生的化學反應方程式為
(2)為提高產品純度,應使燒瓶C中Na2S和Na2SO3恰好完全反應,則燒瓶C中Na2S和Na2SO3物質的量之比為 .
(3)裝置B的作用之一是觀察SO2的生成速率,其中的液體最好選擇a.蒸餾水 b.飽和Na2SO3溶液 c.飽和NaHSO3溶液 d.飽和NaHCO3溶液
實驗中,為使SO2緩慢進入燒瓶C,采用的操作是 .
(4)已知反應(Ⅲ)相對較慢,則燒瓶C中反應達到終點的現象是 , 裝置E的作用為
(5)反應終止后,燒瓶C中的溶液經蒸發濃縮即可析出Na2S2O35H2O,其中可能含有Na2SO3、Na2SO4等雜質.利用所給試劑設計實驗,檢測產品中是否存在Na2SO4 , 簡要說明實驗操作,現象和結論: . 已知:Na2S2O35H2O遇酸易分解:S2O32+2H+=S↓+SO2↑+H2O供選擇的試劑:稀鹽酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com