
【題目】用石灰水保存鮮蛋是一種化學保鮮法。石灰水能保存鮮蛋的原理是
①石灰具有強堿性,殺菌能力強;
②Ca(OH)2能與鮮蛋呼出的CO2反應,生成碳酸鈣薄膜,起保護作用;
③石灰水是電解質溶液,能使蛋白質凝聚;
④石灰水能滲入蛋內中和酸性物質。
A. ①②B. ③④C. ②④D. ①③
科目:高中化學 來源: 題型:
【題目】研究金屬橋墩腐蝕及防護是跨海建橋的重要課題。下列有關判斷中正確的是


A. 用裝置①模擬研究時未見a上有氣泡,說明鐵沒有被腐蝕
B. ②中橋墩與外加電源正極連接能確保橋墩不被腐蝕
C. ③中采用了犧牲陽極的陰極保護法保護橋墩
D. ①②③中海水均是實現化學能與電能相互轉化的電解質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鍺(Ge)是典型的半導體元素,在電子、材料等領域應用廣泛。回答下列問題:
(1)基態Ge原子的核外電子排布式為[Ar]________,有________個未成對電子。
(2)Ge與C是同族元素,C原子之間可以形成雙鍵、叁鍵,但Ge原子之間難以形成雙鍵或叁鍵。從原子結構角度分析,原因是_______________________________。
(3)比較下列鍺鹵化物的熔點和沸點,分析其變化規律及原因_____________________。
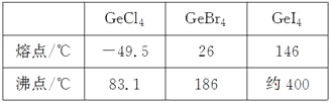
(4)光催化還原CO2制備CH4反應中,帶狀納米Zn2GeO4是該反應的良好催化劑。Zn、Ge、O電負性由大至小的順序是________________。
(5)Ge單晶具有金剛石型結構,其中Ge原子的雜化方式為____________,微粒之間存在的作用力是________________。
(6)晶胞有兩個基本要素:
①原子坐標參數,表示晶胞內部各原子的相對位置,下圖為Ge單晶的晶胞,其中原子坐標參數A為(0,0,0);B為(1/2,0,1/2);C為(1/2,1/2,0)。則D原子的坐標參數為________。
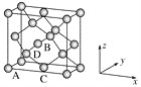
②晶胞參數,描述晶胞的大小和形狀,已知Ge單晶的晶胞參數a=565.76 pm,其密度為________g·cm-3(列出計算式即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碘元素有多種價態,可以形成多種含氧陰離子IxOyn—。由2個IO62—正八面體共用一個面形成的IxOyn- 的化學式為( )
A.I2O94-B.I2O106-C.I2O118-D.I2O1210-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A為淡黃色固體,R和T是兩種生活中常見的金屬單質,C、F是無色無味的氣體。
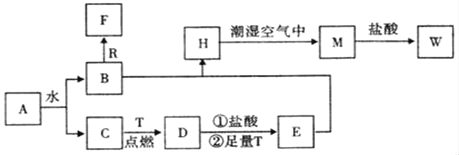
(1)物質A的化學式為_____,D化學式為_____,W的化學式為_____;
(2)B與R反應生成F的離子反應式為___________;
(3)A與CO2反應的化學反應方程式為____________;
(4)H轉化為M的化學反應方程式為_____________;
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分, 針對表中的①~⑧種元素,填寫下列空白:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA[ | 零 |
2 | ① | ② | ③ | |||||
3 | ④[ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)上述元素中,化學性質最不活潑的是 (填元素符號)。
(2)在最高價氧化物的水化物中,酸性最強的化合物的分子式是 (填元素符號)。
(3)元素②的氣態氫化物分子屬于 (填電解質或非電解質);元素⑦與④形成化合物的電子式是 。
(4)元素⑤的最高價氧化物與氫氧化鈉溶液反應的離子方程式為: 。
(5)元素④的某氧化物可作供氧劑,該氧化物中所含的化學鍵類型有 ,寫出其與二氧化碳反應的化學方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將甘油(C3H8O3)轉化成高附加值產品是當前熱點研究方向,如甘油和水蒸氣、氧氣經催化重整或部分催化氧化可制得氫氣,反應主要過程如下:
甘油水蒸氣重整 (SPG) | C3H8O3(1)+3H2O(g) | 反應I |
甘油部分氧化 (POG) | C3H8O3(1)+ | 反應II |
甘油氧化水蒸氣 重整(OSRG) | C3H8O3(1)+ | 反應III |
(1)下列說法正確的是________(填字母序號)。
a. 消耗等量的甘油,反應I的產氫率最高
b. 消耗等量的甘油,反應Ⅱ的放熱最顯著
c. 經過計算得到反應Ⅲ的 △H3=-237.5 kJ·mol-1
d. 理論上,通過調控甘油、水蒸氣、氧氣的用量比例可以實現自熱重整反應,即焓變約為0,這體現了科研工作者對吸熱反應和放熱反應的聯合應用
(2)研究人員經過反復試驗,實際生產中將反應Ⅲ設定在較高溫度(600~700℃)進行,選擇該溫度范圍的原因有:催化劑活性和選擇性高、__________。
(3)研究人員發現,反應I的副產物很多,主要含有:CH4、C2H4、CO、CO2、CH3CHO,CH3COOH等,為了顯著提高氫氣的產率,采取以下兩個措施。
①首要抑制產生甲烷的副反應。從原子利用率角度分析其原因:___________。
②用CaO吸附增強制氫。如圖1所示,請解釋加入CaO的原因:__________。

(4)制備高效的催化劑是這種制氫方法能大規模應用于工業的重要因素。通常將Ni分散在高比表面的載體(SiC、Al2O3、CeO2)上以提高催化效率。分別用三種催化劑進行實驗,持續通入原料氣,在一段時間內多次取樣,繪制甘油轉化率與時間的關系如圖2所示。
①結合圖2分析Ni/SiC催化劑具有的優點是_________。
②研究發現造成催化效率隨時間下降的主要原因是副反應產生的大量碳粉(積碳)包裹催化劑,通過加入微量的、可循環利用的氧化鑭(La2O3)可有效減少積碳。其反應機理包括兩步:
第一步為:La2O3+CO2![]() La2O/span>2CO3
La2O/span>2CO3
第二步為:__________(寫出化學反應方程式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是實驗室進行二氧化硫制備與性質實驗的組合裝置,部分固定裝置未畫出。下列有關說法正確的是

A. 為防止環境污染,裝置C和E中的試劑均取用飽和的石灰水
B. 關閉 K2,打開 K1,滴加硫酸,則裝置 B 中每消耗1mol Na2O2,轉移1mol電子
C. 關閉 K1,打開 K2,試劑 X 是酸性 KMnO4 或 FeCl3 溶液,均可證明 SO2 有還原性
D. 實驗過程中體現了硫酸的酸性、吸水性、難揮發性、強氧化性
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com