
【題目】在一定溫度下,將氣體X和氣體Y各0.16 mol充入10 L恒容密閉容器中,發生反應:X (g) +Y (g)![]() 2Z (g) △H<0。一段時間后達到平衡,反應過程中測定的數據如下表:
2Z (g) △H<0。一段時間后達到平衡,反應過程中測定的數據如下表:
下列說法正確的是
![]()
A. 反應前2 min的平均速率v(Z) =2.0×l0—3mol.L—l·min—l
B. 其他條件不變,降低溫度,反應達到新平衡前:v(逆)>v(正)
C. 保持其他條件不變,起始時向容器中充入0.32 mol氣體X和0.32 moI氣體Y,到達平衡時,C (Z) =0.24 mol·L—l
D. 該溫度下此反應的平衡常數:K=l. 44
【答案】D
【解析】A、V(Y)=(0.16-0.12)/2×10=0.002mol·L-1min-1,則V(Z)= 0.004mol·L-1min-1,A項錯誤;B、降溫,平衡正向移動,則達新平衡前,v(正)>v(逆),B項錯誤;
C、X(g)+Y(g)═2Z(g),圖表數據分析平衡后消耗Y為0.16mol-0.1mol=0.06mol,生成Z為0.12mol,保持其他條件不變,起始時向容器中充入0.32mol氣體X和0.32mol氣體Y,相當于等效為在原平衡基礎上增大壓強,反應前后氣體的體積不變,平衡不移動,到達平衡時,n(Z)=0.24mol,C (Z) =0.24 mol÷10L=0.024 mol·L—l故C錯誤;
D、 X(g) + Y(g)![]() 2Z(g) △H < 0
2Z(g) △H < 0
起始 0.16 0.16 0
變化 0.06 0.06 0.12
平衡 0.10 0.10 0.12
K=0.0122/0.01×0.01=1.44,D項正確。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化學 來源: 題型:
【題目】等質量的CH4和NH3相比較,下列結論中錯誤的是( )
A.兩種氣體的分子個數之比為17:16
B.兩種氣體的原子個數之比為17:16
C.兩種氣體的氫原子個數之比為17:12
D.同溫同壓下,兩種氣體的體積之比為17:16
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
有機物X、Y均為重要的工業原料,可由A和環己烯(![]() )為原料合成,路線如下(部分反應條件省略):
)為原料合成,路線如下(部分反應條件省略):

已知:ⅰ.X的結構簡式是: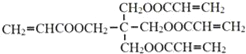
ⅱ.![]()
ⅲ.![]()
(1)X的化學式是____,A中含氧官能團的名稱是_____;第①步反應的類型是___。
(2)下列有關說法正確的是_______。
a.H與苯酚可以用FeCl3溶液區分
b.G、H分別經一步反應都可得到環己烯
c.D的所有同分異構體在紅外光譜儀中顯示的信號(或數據)完全相同
d.試劑a是濃硫酸
e.反應②加高錳酸鉀可以實現
(3)Y的結構簡式是_____________________________________。
(4)已知1mo1W與1mol H2經加成反應生成1molE,寫出W的同分異構體能同時滿足下列條件的結構簡式是_________________________________。
①能與飽和NaHCO3溶液反應產生氣體
②既能發生銀鏡反應,又能發生水解反應
③核磁共振氫譜顯示為3組峰,且峰面積比為6:1:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,純水中的c(H+)=2.0×10-7mol/L,此時溶液的c(OH-)=_______mol/L;若溫度不變,滴入稀鹽酸使c(H+)=5.0×10-4mol/L,則溶液中c(OH-)=________mol/L,由水電離產生的c(H+)=_______mol/L,此時溫度_______25℃(填“高于”、“低于”或“等于”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)銀作為催化劑,主要用于乙烯氧化制環氧乙烷、甲醇氧化制甲醛等。目前銀催化劑的市場需求呈逐年增加的趨勢。請寫出甲醇在銀催化下制備甲醛的化學方程式
________________________________________________________________。
(2)銀催化劑在使用過程中,催化活性逐漸減弱、選擇性降低,一定時間后必須更換。某工廠對失效銀催化劑進行回收并實現再生,工藝流程如下:

已知:銀催化劑主要成分(X射線熒光光譜法分析)
元素 | Al2O3 | Ag | MgO | SiO2 | K2O | Fe2O3 |
含量% | 82 | 14.8 | 1.4 | 0.9 | 0.5 | 0.1 |
資料:經X射線衍射儀檢測,其中氧化鋁的晶型為α型,難于酸。
①操作a和操作b的名稱是_________。
②請寫出過程Ⅰ中銀與稀硝酸反應的離子方程式
________________________________________________________________。
(3)濾液2 中含有多種金屬離子,請簡述檢驗其中K+的實驗方法
____________________________________________________________________。
(4)結合化學用語從平衡移動角度解釋過程Ⅲ中用氨水將氯化銀沉淀溶解的原
因_______________________________________________________________。
(5)過程Ⅳ采用肼(N2H4)作為還原劑,具有不混入金屬雜質、還原性強、得到銀純度高等優點,該過程的化學方程式為:
________________________________________________________。
(6)利用過程Ⅴ實現銀催化劑再生,其簡易裝置圖如下:

寫出催化劑再生的電極反應式:________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有下列變化:①Na2CO3→Na2SiO3,②SiO2→H2SiO3,③Na2SiO3→Na2CO3,④CaO→CaSiO3,其中不能通過一步反應實現的是
A. 只有① B. ②④ C. 只有② D. ③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列電離方程式書寫正確的是( )
A. NaHCO3═Na++H++CO32﹣ B. NaHSO4═Na++H++SO42﹣
C. Fe2(SO4)3═Fe3++SO42﹣ D. NH3H2O═NH4++OH﹣
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com