
(6分)【Ⅰ】將氣體A、B置于固定容積為2L的密閉容器中,發生如下反應:
3A(g) +B(g) 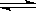 2C(g)+2D(g),
2C(g)+2D(g),
反應進行到10s末,達到平衡,測得A的物質的量為1.8mol,B的物質的量為0.6mol,C的物質的量為0.8mol,則:
(1)用C表示10s 內正反應的化學反應速率為 ;
(2)反應前A的物質的量濃度是 ;
【Ⅱ】某溫度下,在一個體積為2L的固定不變的密閉容器中充入0.3mol SO2和0.2mol O2,發生2 SO2+ O2 2 SO3反應。幾分鐘后反應達到化學平衡狀態,測得容器中氣體壓強變為原來的90% ,則該反應達到平衡時SO2的轉化率為______________。
2 SO3反應。幾分鐘后反應達到化學平衡狀態,測得容器中氣體壓強變為原來的90% ,則該反應達到平衡時SO2的轉化率為______________。
科目:高中化學 來源: 題型:
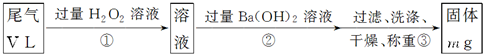
| 22.4m |
| 233V |
| 22.4m |
| 233V |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
(A).【物質結構與性質】
下表是元素周期表的一部分。表中所列的字母分別代表一種化學元素。
| A | |||||||||||||||||
| B | C | ||||||||||||||||
| D | E | ||||||||||||||||
試回答下列問題:
(1)請寫出元素D的基態原子電子排布式 ;
(2)D、E兩元素的部分電離能數據列于下表:
| 元 素 | D | E | |
| 電離能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
比較兩元素的I2、I3可知,氣態D2+再失去一個電子比氣態E2+再失去一個電子難。對此,你的解釋是 ;
(3)A的氫化物的中心原子的雜化形式為 ;C在空氣中燃燒產物的分子構型為 ,與其互為等電子體的單質的分子式為 。
 (4)B單質晶體中原子的堆積方式如右圖甲所示,其晶胞特征如右圖乙所示,原子之間相互位置關系的平面圖如右圖丙所示。晶胞中B原子的配位數為 ,一個晶胞中B原子的數目為 。
(4)B單質晶體中原子的堆積方式如右圖甲所示,其晶胞特征如右圖乙所示,原子之間相互位置關系的平面圖如右圖丙所示。晶胞中B原子的配位數為 ,一個晶胞中B原子的數目為 。
(B).【實驗化學】
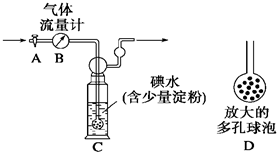
牙膏是生活必需品。下面是牙膏中某些主要成分的檢驗流程圖,。

請回答下列問題:
(1)在①中加水、攪拌、靜置后,接下來的實驗操作名稱是 ,所需要的主要玻璃儀器有 。
(2)在②中用pH試紙測溶液的pH的操作方法是 。
(3)寫出④中發生反應的化學方程
式: 。
(4)將⑤中放出的氣體通入澄清的石灰水中時,未見沉淀出現,則可能的原因是 、
(任答兩條)。
(5)在⑥中檢驗Ca2+的存在,除可用焰色反應外,還可利用Ca2+和 溶液的反應來進行。
查看答案和解析>>
科目:高中化學 來源: 題型:
(14分) 草酸亞鐵可用于合成鋰電池的正極材料硅酸亞鐵鋰(Li2FeSiO4)等,其制備過程主要包括:
a.將硫酸亞鐵銨【(NH4)2Fe(SO4)2·6H2O】晶體溶于適量蒸餾水,加入適量稀硫酸酸化。
b.將上述溶液煮沸,逐滴加入H2C2O4溶液,直至沉淀完全。
c.靜置、傾去上層清液、過濾、洗滌、50℃以下烘干。試回答下列問題:
(1)配制(NH4)2Fe(SO4)2·6H2O溶液時,需加入少量稀硫酸,目的是 。
(2)將制得的產品(FeC2O4·2H2O)在氬氣氣氛中進行熱重分析,結果如圖(TG%表示殘留固體質量占原樣品總質量的百分數)。
① 則A-B發生反應的化學方程式為: 。
② 精確研究表明,B-C實際是分兩步進行的,每步釋放一種氣體,其中第一步釋放的氣體相對分子質量較第二步的小,試寫出B-C兩步反應的方程式: 、
;
(3)Li2CO3、FeC2O4·2H2O和SiO2粉末均勻混合,在800℃. 的氬氣中燒結6小時,即可制成硅酸亞鐵鋰。①合成硅酸亞鐵鋰的化學方程式為: 。
②該鋰電池放電時的總反應式為LiFeSiO4+Li=Li2FeSiO4,寫出相應的電極反應式:
正極 、負極 。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年江蘇省高三元月雙周練習化學試卷 題型:填空題
(14分) 草酸亞鐵可用于合成鋰電池的正極材料硅酸亞鐵鋰(Li2FeSiO4)等,其制備過程主要包括:
a.將硫酸亞鐵銨【(NH4)2Fe(SO4)2·6H2O】晶體溶于適量蒸餾水,加入適量稀硫酸酸化。
b.將上述溶液煮沸,逐滴加入H2C2O4溶液,直至沉淀完全。
c.靜置、傾去上層清液、過濾、洗滌、50℃以下烘干。試回答下列問題:
(1)配制(NH4)2Fe(SO4)2·6H2O溶液時,需加入少量稀硫酸,目的是 。
(2)將制得的產品(FeC2O4·2H2O)在氬氣氣氛中進行熱重分析,結果如圖(TG%表示殘留固體質量占原樣品總質量的百分數)。
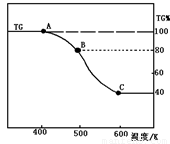
① 則A-B發生反應的化學方程式為: 。
② 精確研究表明,B-C實際是分兩步進行的,每步釋放一種氣體,其中第一步釋放的氣體相對分子質量較第二步的小,試寫出B-C兩步反應的方程式: 、
;
(3)Li2CO3、FeC2O4·2H2O和SiO2粉末均勻混合,在800℃. 的氬氣中燒結6小時,即可制成硅酸亞鐵鋰。①合成硅酸亞鐵鋰的化學方程式為: 。
②該鋰電池放電時的總反應式為LiFeSiO4+Li=Li2FeSiO4,寫出相應的電極反應式:
正極 、負極 。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年江蘇省南京市四校高三12月月考化學試卷 題型:填空題
(14分) 草酸亞鐵可用于合成鋰電池的正極材料硅酸亞鐵鋰(Li2FeSiO4)等,其制備過程主要包括:
a.將硫酸亞鐵銨【(NH4)2Fe(SO4)2·6H2O】晶體溶于適量蒸餾水,加入適量稀硫酸酸化。
b.將上述溶液煮沸,逐滴加入H2C2O4溶液,直至沉淀完全。
c.靜置、傾去上層清液、過濾、洗滌、50℃以下烘干。試回答下列問題:
(1)配制(NH4)2Fe(SO4)2·6H2O溶液時,需加入少量稀硫酸,目的是 ▲ 。
(2)將制得的產品(FeC2O4·2H2O)在氬氣氣氛中進行熱重分析,結果如右圖(TG%表示殘留固體質量占原樣品總質量的百分數)。
① 則A-B發生反應的化學方程式為: ▲ 。
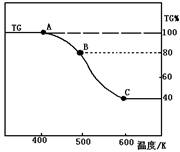
② 精確研究表明,B-C實際是分兩步進行的,每步釋放一種氣體,其中第一步釋放的氣體相對分子質量較第二步的小,試寫出B-C兩步反應的方程式: ▲ 、 ▲ ;
(3)Li2CO3、FeC2O4·2H2O和SiO2粉末均勻混合,在800℃.
的氬氣中燒結6小時,即可制成硅酸亞鐵鋰。①合成硅酸
亞鐵鋰的化學方程式為: ▲ 。
②該鋰電池放電時的總反應式為LiFeSiO4+Li=Li2FeSiO4,
寫出相應的電極反應式:
正極 ▲ 、負極 ▲ 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com