

| ||
| ||
| ||
| ||
| ||
| ||


 一本好題口算題卡系列答案
一本好題口算題卡系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
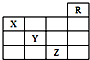 (2007?資陽二模)如圖是元素周期表的一部分,關于元素X、Y、Z的敘述正確的是( )
(2007?資陽二模)如圖是元素周期表的一部分,關于元素X、Y、Z的敘述正確的是( )查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com