
【題目】亞硝酰氯(NOCl,熔點:-64.5 ℃,沸點:-5.5 ℃)是一種黃色氣體,遇水易水解。可用于合成清潔劑、觸媒劑及中間體等。實驗室可由氯氣與一氧化氮在常溫常壓下合成。
(1)甲組的同學擬制備原料氣NO和Cl2,制備裝置如下圖所示:

為制備純凈干燥的氣體,下表中缺少的藥品是:
裝置Ⅰ | 裝置Ⅱ | ||
燒瓶中 | 分液漏斗中 | ||
制備純凈Cl2 | MnO2 | ①___ | ②___ |
制備純凈NO | Cu | ③___ | ④___ |
(2)乙組同學利用甲組制得的NO和Cl2制備NOCl,裝置如圖所示:

①裝置連接順序為a→________(按氣流自左向右方向,用小寫字母表示)。
②裝置Ⅳ、Ⅴ除可進一步干燥NO、Cl2外,另一個作用是____________。
③裝置Ⅶ的作用是____________。
④裝置Ⅷ中吸收尾氣時,NOCl發生反應的化學方程式為________________。
(3)丙組同學查閱資料,查得王水是濃硝酸與濃鹽酸的混酸,一定條件下該混酸可生成亞硝酰氯和氯氣, 該反應的化學方程式為__________________。
【答案】 濃鹽酸 飽和食鹽水 稀硝酸 水 e→f(或f→e)→c→b→d 通過觀察氣泡調節氣體的流速 防止水蒸氣進入裝置Ⅸ中 NOCl+2NaOH=NaCl+NaNO2+H2O HNO3(濃)+3HCl(濃)=NOCl↑+Cl2↑+2H2O
【解析】(1)實驗室加熱制取氯氣是用MnO2與濃鹽酸加熱生成的,所以分液漏斗中裝的是濃鹽酸,裝置Ⅱ是用于吸收氯氣中HCl氣體,所以內裝飽和的食鹽水;實驗室里NO是用Cu和稀硝酸反應制取的,所以分液漏斗中裝的是稀硝酸,裝置Ⅱ是用于吸收NO中HNO3蒸氣的,因此內裝水即可。
(2)已知NOCl沸點為-5.5 ℃,遇水易水解,所以可用冰鹽冷卻收集液體NOCl,再用裝有無水CaCl2的干燥管Ⅶ防止水蒸氣進入裝置Ⅸ中使NOCl變質,由于NO和Cl2都有毒且污染環境,所以用NaOH吸收尾氣,因此①接口順序為a→e→f(或f→e) →c→b→d,②通過觀察洗氣瓶中的氣泡的快慢,調節NO、Cl2氣體的流速,以達到最佳反應比,提高原料的利用率,減少有害氣體的排放,③裝置Ⅶ中裝有的無水CaCl2,是防止水蒸氣進入裝置Ⅸ中使生成的NOCl變質,④NOCl遇水反應生成HCl和HNO2,再與NaOH反應,所以反應的化學方程式為:NOCl+2NaOH![]() NaCl+NaNO2+H2O。
NaCl+NaNO2+H2O。
(3)由題中敘述可知,反應物為濃硝酸和濃鹽酸,生成物為亞硝酰氯和氯氣,所以可寫出反應的化學方程式為HNO3(濃)+3HCl(濃)![]() NOCl↑+Cl2↑+2H2O。
NOCl↑+Cl2↑+2H2O。


科目:高中化學 來源: 題型:
【題目】下列敘述正確的是
A. 常溫下,78 g Na2O2中含有的陰離子數是2NA
B. 標況下,22.4 L CCl4含有的共價鍵數是4NA
C. 2.4g鎂在足量氧氣中燃燒,轉移的電子數是0.1NA
D. 鐵鋁混合物與一定量稀鹽酸反應生成1 mol H2時,轉移電子數是2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,回答下列有關問題:
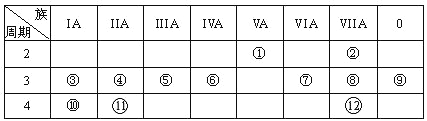
(1)畫出原子的結構示意圖:④______________
(2)在①~12元素中,金屬性最強的元素是______,非金屬性最強的元素是____,最不活潑的元素是_____。(均填元素符號)
(3)元素⑦與元素⑧相比,非金屬性較強的是______(用元素符號表示),下列表述中能證明這一事實的是________。
a.常溫下⑦的單質和⑧的單質狀態不同
b.⑧的氫化物比⑦的氫化物穩定
c.一定條件下⑦和⑧的單質都能與氫氧化鈉溶液反應
(4)元素⑤的最高價氧化物的水化物分別與元素③⑧的最高價氧化物的水化物反應的離子方程式_________, _________
(5)第三周期中原子半徑最大的元素跟它同周期原子半徑最小的元素它們可以形成化合物,用電子式表示其形成過程:__________。
(6)已知某元素原子最外層電子數是其次外層電子數的2倍,該元素可以與⑧形成一種AB4型的化合物,請用電子式表示其形成過程:______________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關物質性質的敘述一定不正確的是
A. 向FeCl2溶液中滴加NH4SCN溶液,溶液顯紅色
B. KAl(SO4) 2·12H2O溶于水可形成 Al(OH)3膠體
C. NH4Cl與Ca(OH)2混合加熱可生成NH3
D. Cu與FeCl3溶液反應可生成CuCl2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】羥基扁桃酸可由苯酚和乙醛酸通過一步反應制得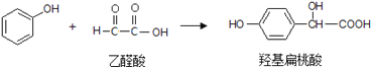
下列有關說法正確的是( )
A. 上述反應屬于取代反應
B. 羥基扁桃酸分子中處于同一平面的原子最多有8個
C. 乙醛酸的核磁共振氫譜中有2個吸收峰
D. 羥基扁桃酸能與FeCl3溶液發生顯色反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用 NA 表示阿伏加德羅常數的值,下列說法中正確的是
A. 1molCH4 與 Cl2 在光照條件下反應生成的 CH3Cl 分子數為 NA
B. 5.6g Fe 和 6.4g Cu 分別與足量 Cl2 反應,轉移的電子數均為 0.2NA
C. 0.1mol/L 的 FeCl3 溶液中,Fe3+的數目為 0.1 NA
D. 3.0 g 葡萄糖和醋酸的混合物中含有的原子總數為 0.4 NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,針對表中的①~⑨種元素,填寫下列空白:
主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1)寫出元素符號和名稱:
①________,②________,⑧________,⑨________。
(2)寫出下列反應的化學方程式:
⑤的氧化物跟④的氫氧化物溶液反應:________________________________
⑥的單質在③的單質中燃燒:_____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含鹵族元素的化合物在科研和生產中有許多重要用途。如:2molSb(CH3)3、2molSb(CH3)2Br和2molSb(CH3)Br2進行重組反應可生成空間位阻最小的離子化合物: [Sb2(CH3)5]2 [Sb2(CH3)2Br6],已知Sb與N同主族。請回答:
(1)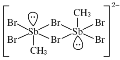 中,H、C、Br的電負性由小到大的順序為________,溴原子的價電子排布式為_____________________。
中,H、C、Br的電負性由小到大的順序為________,溴原子的價電子排布式為_____________________。
(2)[Sb2(CH3)5]+的結構式為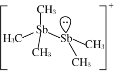 ,Sb原子的雜化軌道類型為_________。寫出一種與CH3-互為等電子體的分子______________。
,Sb原子的雜化軌道類型為_________。寫出一種與CH3-互為等電子體的分子______________。
(3)X射線衍射測定等發現,I3ASF6中存在I3+離子。I3+離子的幾何構型為___________。
(4)一定條件下SbCl3與GaCl3以物質的量之比為l:l混合得到一種固態離子化合物,其結構組成可能為:(a) [GaCl2+][SbCl4—]或(b) [SbCl2+][GaCl4—],該離子化合物最可能的結構組成為______(填“a”或“b”),理由是______________________。
(5)固態PCl5結構中存在PCl4+和PCl6-兩種離子,其晶胞如圖所示。
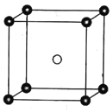
已知晶胞的邊長為a pm,阿伏加德羅常數值用NA表示。則PCl4+和PCl6-之間的最短距離為_______pm,固態PCl5的密度為______gcm-3。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com