
已知反應:
①SO3+H2O=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2↑
④2Na+2H2O=2NaOH+H2↑
⑤2Na2O2+2H2O=4NaOH+O2↑
⑥SiO2+2NaOH=Na2SiO3+H2O
(1)上述反應中不屬于氧化還原反應的有________(填序號,下同).H2O被氧化的是________、H2O被還原的是________.屬于氧化還原反應,但其中的H2O既不被氧化,又不被還原的是________.
(2)寫出方程式②的離子方程式________.
(3)標出方程式④的電子轉移的方向和數目________.
 小題狂做系列答案
小題狂做系列答案科目:高中化學 來源:物理教研室 題型:022
編號 起始狀態/mol 平衡時n(NBr)/mol
H2 Br2 HBr HBr
已知 1 2 0 a
① 2 4 0
② 1 0.5a
③ m n(n³2m)
查看答案和解析>>
科目:高中化學 來源: 題型:022
在一個固定體積的密閉容器中,保持一定溫度,進行以下反應:H2(g)+Br2(g)ƒ2HBr(g),已知加入1mol H2和2mol Br2時,達到平衡后生成amol HBr(見下表“已知”項),在相同條件下,仍保持平衡時各組分的體積分數不變,對下列編號①~③的狀態,填寫表中的空白。
編號 起始狀態/mol 平衡時n(NBr)/mol
H2 Br2 HBr HBr
已知 1 2 0 a
① 2 4 0
② 1 0.5a
③ m n(n³2m)
查看答案和解析>>
科目:高中化學 來源: 題型:022
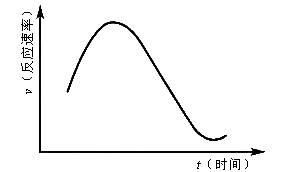
(1)KClO3與NaHSO3間的氧化還原反應生成Cl-和SO42-的速率與時間關系如圖,已知反應速率隨c(H+)的增加而加快,試說明
(1)為什么反應開始時,反應速率增大?________________。
(2)反應后期,反應速率逐漸降低的主要原因是________________。
(2)對于反應:2SO2+O2ƒ2SO3,當其他條件不變時,只改變一個反應條件,將生成SO3的反應速率的變化填入空格里(填寫“增大”、“減小”或“不變”)
編號 改變的條件 生成SO3的速率
① 升高溫度
② 降低溫度
③ 增大O2的濃度
④ 使用V2O3作催化劑
⑤ 壓縮體積
查看答案和解析>>
科目:高中化學 來源: 題型:
(10分)已知醛在一定條件下可以發生如下轉化:
![]()
![]()

![]()
![]()
 物質C是一種可以作為藥物的芳香族化合物,請根據下圖(所有無機產物均已略去)中有機物的轉化關系回答下列問題:
物質C是一種可以作為藥物的芳香族化合物,請根據下圖(所有無機產物均已略去)中有機物的轉化關系回答下列問題:
![]() (1)寫出指定物質的結構簡式:A ,
(1)寫出指定物質的結構簡式:A ,
![]() G 。
G 。
![]() (2)反應①的反應類型是 ,反應②的反應類型是 ,
(2)反應①的反應類型是 ,反應②的反應類型是 ,
![]() 反應⑧的反應類型是 。
反應⑧的反應類型是 。
![]() (3)寫出C與新制Cu(OH)2共熱生成D的化學方程式(有機物寫結構簡式):
(3)寫出C與新制Cu(OH)2共熱生成D的化學方程式(有機物寫結構簡式):
![]() 。
。
![]() 寫出反應⑧的化學方程式(有機物寫結構簡式):
寫出反應⑧的化學方程式(有機物寫結構簡式):
![]() 。
。
![]() (4)H有多種同分異構體,其中能與金屬鈉反應且苯環上只有一個取代基的H的同分異構體結構簡式為:
(4)H有多種同分異構體,其中能與金屬鈉反應且苯環上只有一個取代基的H的同分異構體結構簡式為:
![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
某強酸性反應體系中,反應物和生成物共六種物質:PbO2、PbSO4 (難溶鹽)、Pb(MnO4)2(高錳酸鉛強電解質)、H2O、X(水溶液呈無色)、H2SO4,已知X是一種鹽,且0.1molX在該反應中應失去3.01×1023個電子。下列說法中不正確的是( )
A、若有9.8gH2SO4參加反應,則轉移電子的物質的量為1mol
B、該反應的化學方程式為:5PbO2 + 2MnSO4 + 2H2SO4=== Pb(MnO4)2 + 4PbSO4 + 2H2O
C、Pb(MnO4)2既是氧化產物又是還原產物
D、X是MnSO4
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com