
已知:25℃時,Ksp(AgCl)>Ksp(AgI),下列敘述不正確的是
A.AgI懸濁液中存在平衡:AgI(s)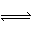 Ag+(aq)+I- (aq)
Ag+(aq)+I- (aq)
B.25℃時,向AgCl的懸濁液中加入NaCl固體,AgCl的溶度積常數不變
C.向含KC1、NaI的混合溶液中滴入AgNO3溶液,一定先析出AgI沉淀
D.用等體積的水和氯化鈉溶液分別洗滌AgCl沉淀,水洗造成的AgCl損耗大
 智能訓練練測考系列答案
智能訓練練測考系列答案科目:高中化學 來源:2015-2016學年天津市高一6月學業調研化學試卷(解析版) 題型:選擇題
氫有三種同位素: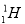 、
、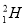 和
和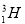 ,它們之間存在差異的是
,它們之間存在差異的是
A.質子數 B.中子數 C.電子數 D.原子序數
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西省高二5月月考文科化學試卷(解析版) 題型:選擇題
合金在生產及科研中具有廣泛的應用。下列物質屬于合金的是
A.水銀 B.石墨 C.硅晶體 D.不銹鋼
查看答案和解析>>
科目:高中化學 來源:2015-2016學年四川省高二4月月考化學試卷(解析版) 題型:填空題
在2 L的密閉容器內,800℃時反應2NO(g)+O2(g)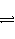

 2NO2(g)體系中,n(NO)隨時間的變化如表:
2NO2(g)體系中,n(NO)隨時間的變化如表:
時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)寫出該反應的平衡常數表達式:K=_____________________。已知:K300℃>K350℃,則該反應是______熱反應。
(2)右圖表示NO2的變化的曲線是_______。用O2表示從0~2 s內該反應的平均速率v=_______________。
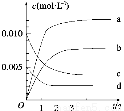
(3)能說明該反應已達到平衡狀態的是________。
a.v(NO2)=2v(O2) b.容器內壓強保持不變
c.v逆(NO)=2v正(O2) d.容器內密度保持不變
(4)為使該反應的反應速率增大,且平衡向正反應方向移動的是________。
a.及時分離出NO2氣體 b.適當升高溫度 c.增大O2的濃度 d.選擇高效催化劑
查看答案和解析>>
科目:高中化學 來源:2015-2016學年四川省高二4月月考化學試卷(解析版) 題型:選擇題
下圖是CO2電催化還原為CH4的工作原理示意圖。
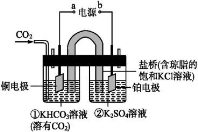
下列說法不正確的是
A.該過程是電能轉化為化學能的過程
B.銅電極的電極反應式為CO2+8H++8e- CH4+2H2O
CH4+2H2O
C.一段時間后,①池中n(KHCO3)不變
D.一段時間后,②池中溶液的pH一定減小
查看答案和解析>>
科目:高中化學 來源:2015-2016學年四川省高二4月月考化學試卷(解析版) 題型:選擇題
下列說法錯誤的是
A.除去MgCl2溶液中少量的FeCl3,可選用MgCO3
B.等物質的量濃度的(NH4)2SO4溶液和(NH4)2CO3溶液中NH4+的濃度前者大于后者
C.NaHS溶液中,滴入少量CuCl2溶液,產生黑色沉淀,HS-的水解程度增大,pH增大
D.用飽和氯化銨溶液可以清洗金屬表面的銹跡
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省高三下學期適應性考試理綜化學試卷(解析版) 題型:填空題
鐵元素不僅可以與SCN-、CN-等離子形成配合物,還可以與CO、NO等分子以及許多有機試劑形成配合物.回答下列問題:
(1)基態鐵原子有_____________個未成對電子;
(2)CN-有毒,含CN-的工業廢水必須處理,用TiO2作光催化劑可將廢水中的CN-轉化為OCN-,并最終氧化為N2、CO2
①C、N、O三種元素的第一電離能由大到小的順序是_____________;
②1molFe(CN)32-中含有σ鍵的數目為_____________;
③鐵與CO形成的配合物Fe(CO)3的熔點為-20.5℃,沸點為103℃,易溶于CCl4,據此可以判斷Fe(CO)3晶體屬于_____________(填晶體類型)
(3)乙二胺四乙酸能和Fe2+形成穩定的水溶性配合物乙二胺四乙酸鐵鈉,原理如圖1:
①乙二胺四乙酸中碳原子的雜化軌道類型是_____________;
②乙二胺(H2NCH2CH2NH2)和三甲胺[N(CH3)2]均屬于胺,但乙二胺比三甲胺的沸點高得多,原因是_____________;
(4)鐵鋁合金的一種晶體屬于面心立方結構,其晶胞可看成由8個小體心立方結構堆砌而成,小立方體如圖2所示,則該合金的化學式為_____________,已知小立方體邊長為acm,此鐵鋁合金的密度為_____________g•cm-3。

查看答案和解析>>
科目:高中化學 來源:2016屆安徽省高三最后一卷理綜化學試卷(解析版) 題型:實驗題
某研究性學習小組以甲酸為原料在實驗室完成了一氧化碳和甲酸銅兩種物質的制備實驗。
實驗一、用甲酸制備一氧化碳
CO的制備原理:HCOOH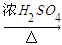 CO↑+H2O,制備裝置如下圖(其中夾持儀器、加熱儀器沒有畫出)
CO↑+H2O,制備裝置如下圖(其中夾持儀器、加熱儀器沒有畫出)
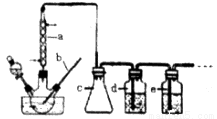
(1)b儀器的名稱為___________,c的作用是___________。
(2)制備CO時,濃硫酸與甲酸的混合方式是___________。
實驗二、用甲酸制備甲酸銅[Cu(HCOO)2•4H2O]
步驟一:堿式碳酸銅的制備
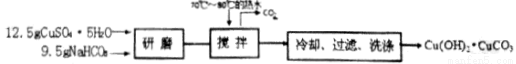
步驟二:甲酸銅的制備
將產品堿式碳酸銅放入燒杯內,加入約20mL蒸餾水,加熱攪拌至323K左右,逐滴加入適量甲酸至沉淀完全溶解,趁熱過濾,濾液在通風櫥下蒸發至原體積的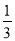 左右,冷卻至室溫,減壓過濾,洗滌,得Cu(HCOO)2•4H2O產品,稱量,計算產率。回答下列問題:
左右,冷卻至室溫,減壓過濾,洗滌,得Cu(HCOO)2•4H2O產品,稱量,計算產率。回答下列問題:
(3)在制備堿式碳酸銅的過程中,如果溫度過高,對產物有何影響?___________。
(4)步驟二中堿式碳酸銅滴入甲酸生成四水合甲酸銅的化學方程式為___________。
(5)本實驗涉及三種固液分離的方法.
①傾析法使用到的儀器有___________;
②采用減壓過濾的裝置對步驟二中溶解后的溶液進行趁熱過濾;
③步驟二的實驗中,需用到下列裝置___________

(6)最終稱量所得的產品為7.91g,則產率為___________。
查看答案和解析>>
科目:高中化學 來源:205-2016學年吉林省高二下學期期中化學試卷(解析版) 題型:選擇題
下列描述正確的是( )
A.甲苯中若混有苯,可通過酸性高錳酸鉀溶液除去
B.乙醇中是否混有水,可用加入金屬鈉是否產生氣體進行檢驗
C.蠶絲和棉花的組成元素相同,分子結構不同,因而性質不同
D.乙酸乙酯是否混有乙酸,可用加石蕊試液是否變紅進行檢測
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com