
某校三個研究性學習小組對“葡萄糖溶液與新制的氫氧化銅懸濁液作用得到的磚紅色沉淀是Cu2O”提出質疑。
(1)甲小組認為紅色沉淀不一定是Cu2O,為此展開了確定紅色沉淀成分的研究。
步驟一:提出假設:__________________________________________________。
步驟二:查閱資料。得出:①+1價的銅在酸性條件下易發生自身氧化還原反應;②在空氣中灼燒氧化亞銅生成氧化銅。
步驟三:設計方案、實驗。
A.取該紅色沉淀溶于足量的稀硝酸中,觀察溶液顏色變化
B.取該紅色沉淀溶于足量的稀硫酸中,觀察是否有殘渣
C.取該紅色沉淀a g,在空氣中充分灼燒至完全變黑,放在干燥器里冷卻,再稱重,反復多次至固體恒重,稱得質量為b g,比較a,b的關系
D.取該紅色沉淀裝入試管里,加入酸化的硝酸銀溶液,觀察是否有銀白色沉淀析出
你認為合理的方案是(填字母)__________。
(2)乙小組對甲小組的假設,另設計如下圖所示裝置進行驗證。
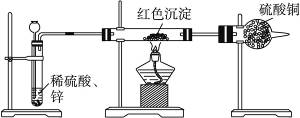
若按乙組裝置定性檢驗上述紅色沉淀部分,可根據__________現象的發生與否即可判斷。
若按乙組裝置測定上述紅色沉淀的成分,你認為理論上應該測定下列哪些物理量__________(填序號)。
①通入氫氣的體積 ②反應前紅色沉淀和硬質玻璃管的總質量
③完全反應后紅色固體和硬質玻璃管的總質量 ④實驗前干燥管質量
⑤硬質玻璃管質量 ⑥鋅粒質量
⑦稀硫酸中含溶質的量 ⑧實驗后干燥管質量
該實驗裝置中距實際可行性方面存在的缺陷有____________________(請寫出兩點)。
(1)假設①:紅色沉淀成分為Cu;假設②:紅色成分為Cu2O;假設③:紅色沉淀成分為Cu與Cu2O的混合物 C
(2)硬質玻璃管有水或干燥管內白色粉末變藍 ②③⑤ 發生裝置產生的氫氣中含有水、硬質玻璃管內水分很難全部被氫氣趕盡、外界空氣中的水蒸氣也會被無水硫酸銅吸收等
(1)可能有三種情況都呈紅色沉淀,Cu或Cu2O或二者混合物。A項,Cu和Cu2O都能被足量稀硝酸溶解;B項,Cu2O和足量的稀硫酸發生反應:Cu2O+2H+ ==== 2Cu++H2O和2Cu+ ==== Cu+Cu2+,也有固體生成;C項,從化學式和固體質量的變化計算可以證明;D項,不能說明有沒有銅單質。(2)由無水硫酸銅是否變藍來證明有無Cu2O;根據質量差所需數據選出②③⑤;實驗裝置的缺陷:從對實驗現象影響考慮,從發生裝置產生的氫氣中含有水、硬質玻璃管內水分很難全部被氫氣趕盡、外界空氣中的水蒸氣也會被無水硫酸銅吸收等考慮。


 一課一練課時達標系列答案
一課一練課時達標系列答案科目:高中化學 來源: 題型:閱讀理解
查看答案和解析>>
科目:高中化學 來源: 題型:
已知:①NO+NO2+2OH-![]() 2
2![]() +H2O
+H2O
②氣體液化溫度:NO2:

(1)現有甲、乙、丙三位同學分別設計了以下三個實驗方案(用儀器的連接順序表示)。
甲:A→C→F→D→B 乙:A→B→C→E 丙:A→F→D→B
甲、乙、丙三位同學提出的實驗方案是否能驗證Cu與適量濃HNO3反應產生的氣體中含有NO(填“能”或“不能”)
甲:_________;乙:_________;丙:_________。
用化學方程式表示不能驗證的主要原因(若三個實驗方案都能驗證,則此小題不用回答):
甲方案:____________________________________;
乙方案:____________________________________;
丙方案:____________________________________。
(2)實驗開始時首先通入足量的N2,其目的是:___________________________。
(3)確認氣體中含NO的現象是:___________________________。
(4)如果O2過量,則裝置B中發生反應的離子方程式是:_____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
1. 醋酸是一種常見的弱酸,為了證明醋酸是弱電解質,某校研究性學習小組開展了題為“醋酸是弱電解質的實驗研究”的探究活動。該校研究性學習小組設計了如下方案:A.先配制一定量的0.10 mol/L CH3COOH溶液,然后測溶液的pH,若pH大于1,則可證明醋酸為弱電解質
B.先測0.10 mol/L CH3COOH溶液的pH,然后將其加熱至40℃,再測pH,如果pH變小,則可證明醋酸為弱電解質
C.先配制一定量0.01 mol/L和0.10 mol/L的CH3COOH溶液,分別測它們的pH,若兩者的pH相差小于1個單位,則可證明醋酸為弱電解質
D.在常溫下,配制一定量的CH3COONa溶液,測其pH,若pH大于7,則可證明醋酸為弱電解質。
你認為上述方案可行的是________________________________。
2. 一定溫度下,有a、鹽酸;b、硫酸;c、醋酸三種酸的稀溶液。(用a、b、c、<、=、>號填寫)
①當其物質的量濃度相同時,c(H+)由大到小的順序是_____ ____,②同體積同物質的量濃度的三種酸,中和同物質的量濃度的NaOH消耗的體積由大到小的順序是_________ ③當c(H+)相同、體積相同時,分別加入足量鋅,相同狀況產生的氣體體積由大到小的順序___________ ④將c(H+)相同的三種酸均稀釋10倍,pH由大到小的順序為_____________
3.某溫度(t ℃)時, KW=10-13,將此溫度下pH=1的硫酸溶液aL與pH=12的氫氧化鋇溶液bL混合。
①若所得混合液為中性,則a:b= 。
②若所得混合液的pH=2,則a:b= 。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年四川樂山一中高二下學期第二階段考試化學卷 (帶解析) 題型:填空題
【小題1】 醋酸是一種常見的弱酸,為了證明醋酸是弱電解質,某校研究性學習小組開展了題為“醋酸是弱電解質的實驗研究”的探究活動。該校研究性學習小組設計了如下方案:
| A.先配制一定量的0.10 mol/L CH3COOH溶液,然后測溶液的pH,若pH大于1,則可證明醋酸為弱電解質 |
| B.先測0.10 mol/L CH3COOH溶液的pH,然后將其加熱至40℃,再測pH,如果pH變小,則可證明醋酸為弱電解質 |
| C.先配制一定量0.01 mol/L和0.10 mol/L的CH3COOH溶液,分別測它們的pH,若兩者的pH相差小于1個單位,則可證明醋酸為弱電解質 |
| D.在常溫下,配制一定量的CH3COONa溶液,測其pH,若pH大于7,則可證明醋酸為弱電解質。 |
查看答案和解析>>
科目:高中化學 來源:2013屆四川樂山一中高二下學期第二階段考試化學卷(解析版) 題型:填空題
1. 醋酸是一種常見的弱酸,為了證明醋酸是弱電解質,某校研究性學習小組開展了題為“醋酸是弱電解質的實驗研究”的探究活動。該校研究性學習小組設計了如下方案:A.先配制一定量的0.10 mol/L CH3COOH溶液,然后測溶液的pH,若pH大于1,則可證明醋酸為弱電解質
B.先測0.10 mol/L CH3COOH溶液的pH,然后將其加熱至40℃,再測pH,如果pH變小,則可證明醋酸為弱電解質
C.先配制一定量0.01 mol/L和0.10 mol/L的CH3COOH溶液,分別測它們的pH,若兩者的pH相差小于1個單位,則可證明醋酸為弱電解質
D.在常溫下,配制一定量的CH3COONa溶液,測其pH,若pH大于7,則可證明醋酸為弱電解質。
你認為上述方案可行的是________________________________。
2. 一定溫度下,有a、鹽酸;b、硫酸;c、醋酸三種酸的稀溶液。(用a、b、c、<、=、>號填寫)
①當其物質的量濃度相同時,c(H+)由大到小的順序是_____ ____,②同體積同物質的量濃度的三種酸,中和同物質的量濃度的NaOH消耗的體積由大到小的順序是_________ ③當c(H+)相同、體積相同時,分別加入足量鋅,相同狀況產生的氣體體積由大到小的順序___________ ④將c(H+)相同的三種酸均稀釋10倍,pH由大到小的順序為_____________
3.某溫度(t ℃)時, KW=10-13,將此溫度下pH=1的硫酸溶液aL與pH=12的氫氧化鋇溶液bL混合。
①若所得混合液為中性,則a:b= 。
②若所得混合液的pH=2,則a:b= 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com