
 小題狂做系列答案
小題狂做系列答案科目:高中化學 來源: 題型:閱讀理解

查看答案和解析>>
科目:高中化學 來源:2013屆河南省扶溝縣高級中學高三第三次考試化學試卷(帶解析) 題型:填空題
(11分)以CO2為碳源制取低碳有機物成為國際研究焦點,下面為CO2加氫制取低碳醇的熱力學數據:
反應I: CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1
CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1
反應II:2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) △H =" —173.6" kJ·mol-1
CH3CH2OH(g)+3H2O(g) △H =" —173.6" kJ·mol-1
(1)寫出由CH3CH2OH+_____ 2CH3OH的熱化學方程式為:__________________。
2CH3OH的熱化學方程式為:__________________。
(2)在一定條件下,對于反應I:在體積恒定的密閉容器中,達到平衡的標志是__ (填字母)
a.CO2和CH3OH 濃度相等 b.H2O的百分含量保持不變
c.H2的平均反應速率為0 d.v正(CO2)=3v逆(H2)
e.混合氣體的密度不再發生改變
f. 混合氣體的平均相對分子質量不再發生改變
如果平衡常數K值變大,該反應 (填字母)
a.一定向正反應方向移動 b.在平衡移動時正反應速率先增大后減小
c.一定向逆反應方向移動 d.在平衡移動時逆反應速率先減小后增大
其他條件恒定,如果想提高CO2的反應速率,可以采取的反應條件是 (填字母) ,
達到平衡后,想提高H2轉化率的是_______________(填字母)
a、降低溫度 b、補充H2 c、移去甲醇 d、加入催化劑
(3)在密閉容器中,對于反應II中,研究員以生產乙醇為研究對象,在5MPa、m= n(H2)/n(CO2)=3時,測得不同溫度下平衡體系中各種物質的體積分數(y%)如圖所示,則表示CH3CH2OH體積分數曲線的是 ;表示CO2的體積分數曲線的是 。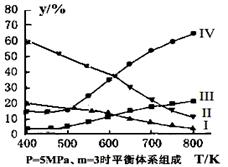
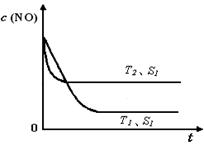
(4)當質量一定時,增大固體催化劑的表面積可提高化學反應速率。上圖是反應:2NO(g) + 2CO(g) 2CO2(g)+ N2(g) 中NO的濃度隨溫度(T)、催化劑表面積(S)和時間(t)的變化曲線,若催化劑的表面積S1>S2 ,在上圖中畫出NO的濃度在T1、S2 條件下達到平衡過程中的變化曲線,并注明條件。
2CO2(g)+ N2(g) 中NO的濃度隨溫度(T)、催化劑表面積(S)和時間(t)的變化曲線,若催化劑的表面積S1>S2 ,在上圖中畫出NO的濃度在T1、S2 條件下達到平衡過程中的變化曲線,并注明條件。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年河南省高三第三次考試化學試卷(解析版) 題型:填空題
(11分)以CO2為碳源制取低碳有機物成為國際研究焦點,下面為CO2加氫制取低碳醇的熱力學數據:
反應I:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)
△H = —49.0 kJ·mol-1
CH3OH(g)+H2O(g)
△H = —49.0 kJ·mol-1
反應II:2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g)
△H = —173.6 kJ·mol-1
CH3CH2OH(g)+3H2O(g)
△H = —173.6 kJ·mol-1
(1)寫出由CH3CH2OH +_____ 2CH3OH的熱化學方程式為:__________________。
2CH3OH的熱化學方程式為:__________________。
(2)在一定條件下,對于反應I:在體積恒定的密閉容器中,達到平衡的標志是__ (填字母)
a.CO2和CH3OH 濃度相等 b.H2O的百分含量保持不變
c.H2的平均反應速率為0 d.v正(CO2)=3v逆(H2)
e.混合氣體的密度不再發生改變
f. 混合氣體的平均相對分子質量不再發生改變
如果平衡常數K值變大,該反應 (填字母)
a.一定向正反應方向移動 b.在平衡移動時正反應速率先增大后減小
c.一定向逆反應方向移動 d.在平衡移動時逆反應速率先減小后增大
其他條件恒定,如果想提高CO2的反應速率,可以采取的反應條件是 (填字母) ,
達到平衡后,想提高H2轉化率的是_______________(填字母)
a、降低溫度 b、補充H2 c、移去甲醇 d、加入催化劑
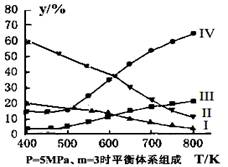
(3)在密閉容器中,對于反應II中,研究員以生產乙醇為研究對象,在5MPa、m= n(H2)/n(CO2)=3時,測得不同溫度下平衡體系中各種物質的體積分數(y%)如圖所示,則表示CH3CH2OH體積分數曲線的是 ;表示CO2的體積分數曲線的是 。
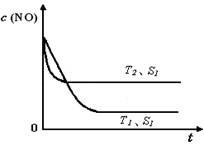
(4)當質量一定時,增大固體催化劑的表面積可提高化學反應速率。上圖是反應:2NO(g)
+ 2CO(g)
 2CO2(g)+ N2(g) 中NO的濃度隨溫度(T)、催化劑表面積(S)和時間(t)的變化曲線, 若催化劑的表面積S1>S2 ,在上圖中畫出NO的濃度在T1、S2 條件下達到平衡過程中的變化曲線,并注明條件。
2CO2(g)+ N2(g) 中NO的濃度隨溫度(T)、催化劑表面積(S)和時間(t)的變化曲線, 若催化劑的表面積S1>S2 ,在上圖中畫出NO的濃度在T1、S2 條件下達到平衡過程中的變化曲線,并注明條件。
查看答案和解析>>
科目:高中化學 來源: 題型:
[s1] ![]() 在一定條件下,當單獨改變可逆反應:N2(g)+3H2(g) 2NH3(g);△H<0的某一條件后,下列敘述中錯誤的是 ( )
在一定條件下,當單獨改變可逆反應:N2(g)+3H2(g) 2NH3(g);△H<0的某一條件后,下列敘述中錯誤的是 ( )
A.加入催化劑,V正、V逆都發生變化,且變化的倍數相等
B.增大壓強,V正、V逆都增大,V正增大的倍數大于V逆增大的倍數
C.降低溫度,V正、V逆都減小,且V正減小的倍數小于V逆減小的倍數
D.加入氬氣,V正、V逆都增大,且V正增大的倍數大于V逆增大的倍數
[s1]7.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com